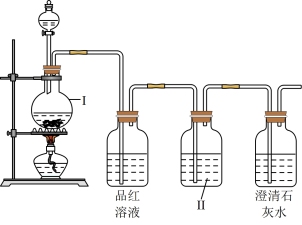
回答下列问题:
(1)写出下列物质的化学式:①钡餐:_____ ;②漂白液的有效成分:_____ 。
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:_____ 。
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是_____ 。
(1)写出下列物质的化学式:①钡餐:
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是
更新时间:2023-05-24 19:25:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.工业上常用氯气与石灰乳反应制漂白粉,但Ca(OH)2与Cl2反应的氧化产物与温度有关。在足量的石灰乳中通入一定量的氯气,充分反应后生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
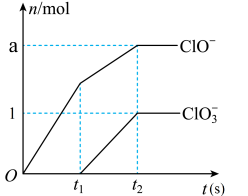
(1)常温时工业制漂白粉的化学方程式为_________________ 。
(2)t1时开始有ClO3-生成的原因是_________________ 。
(3)该石灰乳中参加反应的Ca(OH)2的物质的量是_________________ mol(用含a的代数式来表示)。
Ⅱ.过氧乙酸( )是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对空气与地面进行消毒。
)是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对空气与地面进行消毒。
(4)下列叙述正确的是_________________ (填字母)。
A.过氧乙酸分子中两个氧原子化合价为-1,一个氧原子化合价为-2
B.过氧乙酸溶于水能导电,属于离子化合物,也属于电解质
C.过氧乙酸包装上应贴的危险警告标签应如图所示
D.过氧乙酸应注意密闭、低温保存于棕色细口瓶中
E.过氧乙酸是一种有机物,它可以用于萃取碘水中的碘单质
(5)某学生在实验室用3.00 mol•L−1过氧乙酸配制0.15 mol•L−1过氧乙酸溶液250 mL,该生用量筒量取工业品过氧乙酸的体积为_________________ mL。
(6)如果生产过氧乙酸的原料CH3COONa中混有了SO42-,要想除掉SO42-,请选择下列试剂按照加入先后顺序填空_________________ (试剂不必选完,填序号)。
①醋酸钡溶液;②醋酸;③硝酸钡溶液;④盐酸;⑤碳酸氢钠溶液;⑥碳酸钠溶液。

(1)常温时工业制漂白粉的化学方程式为
(2)t1时开始有ClO3-生成的原因是
(3)该石灰乳中参加反应的Ca(OH)2的物质的量是
Ⅱ.过氧乙酸(
 )是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对空气与地面进行消毒。
)是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对空气与地面进行消毒。(4)下列叙述正确的是
A.过氧乙酸分子中两个氧原子化合价为-1,一个氧原子化合价为-2
B.过氧乙酸溶于水能导电,属于离子化合物,也属于电解质
C.过氧乙酸包装上应贴的危险警告标签应如图所示

D.过氧乙酸应注意密闭、低温保存于棕色细口瓶中
E.过氧乙酸是一种有机物,它可以用于萃取碘水中的碘单质
(5)某学生在实验室用3.00 mol•L−1过氧乙酸配制0.15 mol•L−1过氧乙酸溶液250 mL,该生用量筒量取工业品过氧乙酸的体积为
(6)如果生产过氧乙酸的原料CH3COONa中混有了SO42-,要想除掉SO42-,请选择下列试剂按照加入先后顺序填空
①醋酸钡溶液;②醋酸;③硝酸钡溶液;④盐酸;⑤碳酸氢钠溶液;⑥碳酸钠溶液。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用如图所示的“价-类”二维图,可以从不同角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
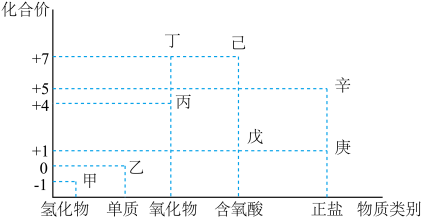
(1)丙的化学式为_____________ ;丁的化学式为_____________ 。
(2)甲、乙、丁、戊中,属于电解质的是__________________________ (填化学式);根据氯元素的化合价判断,乙____________________ (填标号)。
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既能作氧化剂又能作还原剂
(3)庚是漂白粉的有效成分,用乙制取漂白粉的化学方程式为____________________________ 。
(4)辛在 催化下受热分解可制备一种常见的气体,这种气体的化学式是
催化下受热分解可制备一种常见的气体,这种气体的化学式是______________ 。

(1)丙的化学式为
(2)甲、乙、丁、戊中,属于电解质的是
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既能作氧化剂又能作还原剂
(3)庚是漂白粉的有效成分,用乙制取漂白粉的化学方程式为
(4)辛在
 催化下受热分解可制备一种常见的气体,这种气体的化学式是
催化下受热分解可制备一种常见的气体,这种气体的化学式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ______________ 。
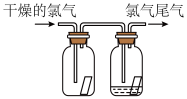
(2)为防止氯气尾气污染空气,可用________ 溶液吸收多余的氯气,原理是(用化学方程式表示)____________________ 。
(3)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO

(2)为防止氯气尾气污染空气,可用
(3)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题.
(1)久置的硅酸钠溶液会出现浑浊现象其原因为________ (用化学方程式表示)
(2)红热的木炭与浓硫酸反应的化学方程式________
(3)SO2催化氧化成SO3的化学方程式:________
(4)写出铜与稀硝酸反应的离子方程式________
(5)实验室制取氨气的化学方程式为________ ,常用________ 来干燥氨气.
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是________ ,还原产物是_______ .
②氧化剂与氧化产物的物质的量比是________ 。
(1)久置的硅酸钠溶液会出现浑浊现象其原因为
(2)红热的木炭与浓硫酸反应的化学方程式
(3)SO2催化氧化成SO3的化学方程式:
(4)写出铜与稀硝酸反应的离子方程式
(5)实验室制取氨气的化学方程式为
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是
②氧化剂与氧化产物的物质的量比是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物。某同学设计了如下图所示的实验。请据此回答下列问题。
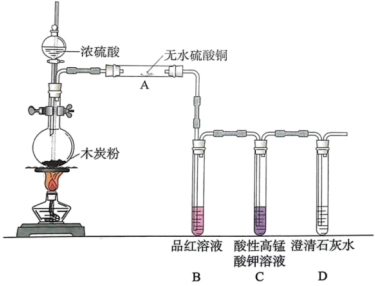
(1)A中的实验现象是_______ ,证明产物中有_______ 。
(2)B中的实验现象是_______ 。
(3)装置C的作用是_______ 。
(4)浓硫酸与木炭在加热条件下发生化学反应的化学方程式_______ 。

(1)A中的实验现象是
(2)B中的实验现象是
(3)装置C的作用是
(4)浓硫酸与木炭在加热条件下发生化学反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
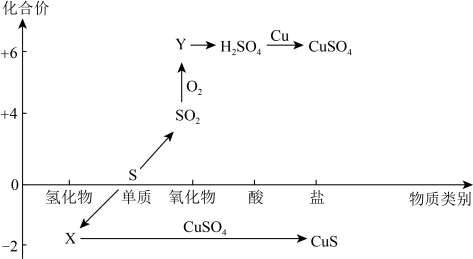
【推荐1】硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)X与 反应的化学方程式是
反应的化学方程式是___________ ,氧化剂是___________ (填化学式)。
(3)
___________ (填“是”、或“不是”)电解质,检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(2)X与
 反应的化学方程式是
反应的化学方程式是(3)

 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是_______ ;属于非电解质的是 _______ 。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物_______ ;
②从硝酸钾和氯化钠的混合液中获得硝酸钾_______ ;
③从溴水中提取溴单质_______ ;
④分离水和煤油的混合物_______ ;
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物_______ ;
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是_______ 。
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。
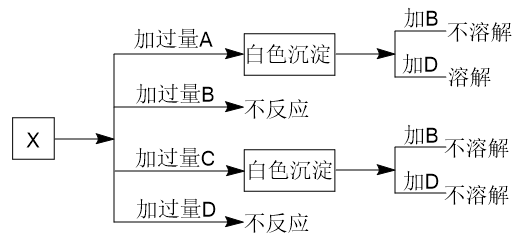
A:_______ B:_______ C:_______ D:_______ X:_______
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物
②从硝酸钾和氯化钠的混合液中获得硝酸钾
③从溴水中提取溴单质
④分离水和煤油的混合物
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。

A:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】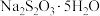 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.
(1)工业上,常用 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:__________________ .理论上,能发生的氧化还原反应都可以设计成原电池.如果将上述反应设计成原电池,则正极反应式为____________ .
(2)已知: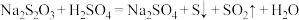
某小组设计实验探究影响化学反应速率的外界因素:
①
_________ ,设计实验I,Ⅱ的目的是_________ .
②实验测得: .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是________________ .
③根据表格信息,__________ (填“能”或“不能”)比较a和d的大小,原因是________ .
(3)已知: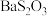 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:__________________ .
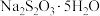 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.(1)工业上,常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:(2)已知:
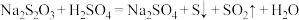
某小组设计实验探究影响化学反应速率的外界因素:
| 序号 | 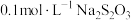 溶液 溶液 | 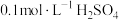 溶液 溶液 | 蒸馏水 | 温度 | 变浑浊时间 |
| I |  |  | 0 | 35℃ | a s |
| II |  | 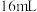 | V mL | 35℃ | b s |
| III |  |  | 0 | 45℃ | c s |
| IV |  |  | 5 mL | 40℃ | d s |

②实验测得:
 .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是③根据表格信息,
(3)已知:
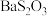 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某待测溶液中可能含有 、
、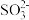 、
、 、
、 、
、 、
、 、
、 中的若干种和一种常见金属阳离子(
中的若干种和一种常见金属阳离子( ),现进行如下图所示实验(每次实验所用试剂均足量,鉴定中某些成分可能没有给出)。
),现进行如下图所示实验(每次实验所用试剂均足量,鉴定中某些成分可能没有给出)。
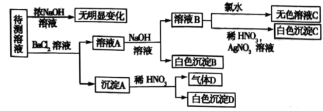
请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填)。
(2)待测溶液中是否有 、
、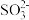 ?
?_______ 。
(3)形成沉淀B时反应的离子方程式为_______ 。
(4)形成沉淀C时反应的离子方程式为_______ 。
(5)若气体D遇空气变红棕色,则该反应的化学方程式为_______ 。
 、
、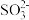 、
、 、
、 、
、 、
、 、
、 中的若干种和一种常见金属阳离子(
中的若干种和一种常见金属阳离子( ),现进行如下图所示实验(每次实验所用试剂均足量,鉴定中某些成分可能没有给出)。
),现进行如下图所示实验(每次实验所用试剂均足量,鉴定中某些成分可能没有给出)。
请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填)。
| 肯定存在的离子 | 肯定没有的离子 | 沉淀D | |
| 化学式或离子符号 |
 、
、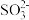 ?
?(3)形成沉淀B时反应的离子方程式为
(4)形成沉淀C时反应的离子方程式为
(5)若气体D遇空气变红棕色,则该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某中学生取纯净的Na2SO3·7H2O50.00g,经600℃以上的强热至恒重,分析及计算表明,恒重后的样品质量相当于无水亚硫酸钠的计算值,而且各元素的组成也符合计算值,但将它溶于水,却发现溶液的碱性大大高于期望值。经过仔细思考,这位同学解释了这种反常现象,并设计了一组实验,验证了自己的解释是正确的。
(1)他对反常现象的解释是:_______ (请用化学方程式表达)
(2)他设计的验证实验是:_______ (请用化学方程式表达)
(1)他对反常现象的解释是:
(2)他设计的验证实验是:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)工业上先用 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液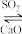 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是___________ 。(用化学方程式表示)
(2)常温下进行“钠碱法”的模拟实验。用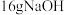 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________  (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了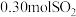 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:___________ 。(写出溶质组成和每种溶质的物质的量)
(3)若用碱液吸收工业尾气中的 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式___________ 。
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)工业上先用
 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液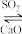 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是(2)常温下进行“钠碱法”的模拟实验。用
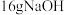 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为 (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了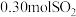 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:(3)若用碱液吸收工业尾气中的
 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式
您最近半年使用:0次