完成下列填空:
(1)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。工业上常用Cl2处理含Fe2+的FeCl3溶液,请写出该反应的离子方程式:_______ 。
(2)2020年突如其来的“新冠肺炎”使人们认识到含氯消毒剂的重要性。
①“84”消毒液(有效成分为次氯酸钠)在此次抗疫中发挥了重要作用,其工业制备的化学方程式_______ 。
②已知KMnO4与浓盐酸反应也可以用来制取氯气:2KMnO4+16HCl=2KCl+ 2MnCl2+ 5Cl2↑+ 8H2O。氧化剂是_______ (填化学式);若有15.8g KMnO4参与反应,反应中转移的电子为_______ mol。请用单线桥法表示电子转移的方向和数目:_______ 。
(3)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。
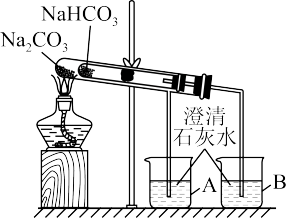
①整个实验过程中,能观察到烧杯B中的现象是_______ 。
②该实验可证明NaHCO3的热稳定性_______ (填“强于”“弱于”或“等于”)Na2CO3;_______ (填“能”或“不能”)将NaHCO3、Na2CO3的位置互换。
(1)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。工业上常用Cl2处理含Fe2+的FeCl3溶液,请写出该反应的离子方程式:
(2)2020年突如其来的“新冠肺炎”使人们认识到含氯消毒剂的重要性。
①“84”消毒液(有效成分为次氯酸钠)在此次抗疫中发挥了重要作用,其工业制备的化学方程式
②已知KMnO4与浓盐酸反应也可以用来制取氯气:2KMnO4+16HCl=2KCl+ 2MnCl2+ 5Cl2↑+ 8H2O。氧化剂是
(3)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。

①整个实验过程中,能观察到烧杯B中的现象是
②该实验可证明NaHCO3的热稳定性
更新时间:2022-01-22 08:05:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)已知: ,反应中氧化剂是
,反应中氧化剂是___________ ;氧化剂与还原剂物质的量之比是___________ ;氧化产物是___________ 。
(2)由 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应中,其中
组成的一个氧化还原反应中,其中 ,据此回答下列问题:
,据此回答下列问题:
①该氧化还原反应中,被还原的元素是___________ 。
②请写出完整的氧化还原反应方程式,并用双线桥法标出电子转移的方向和数目:___________ 。
 ,反应中氧化剂是
,反应中氧化剂是(2)由
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应中,其中
组成的一个氧化还原反应中,其中 ,据此回答下列问题:
,据此回答下列问题:①该氧化还原反应中,被还原的元素是
②请写出完整的氧化还原反应方程式,并用双线桥法标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】分析以下A~D四个涉及H2O2的反应(未配平),填空:
A.
B.
C.
D.
(1)H2O2仅体现氧化性的反应是________ ,H2O2体现还原性的反应是________ ,H2O2既体现氧化性,又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是________ (填字母)。
(2)用单线桥法表示D反应中电子转移的方向和数目:

_______________________________________________ 。
该反应中氧化剂是________ ,氧化产物是________ 。
(3)已知:在一定条件下H2O2能和酸性高锰酸钾溶液反应生成O2,请完成下列缺项方程式的配平:
____ 
____ 
____ ( ) = ____ 
____ 
____ ( )
在该反应中H2O2作________ 剂。
A.

B.

C.

D.

(1)H2O2仅体现氧化性的反应是
(2)用单线桥法表示D反应中电子转移的方向和数目:

该反应中氧化剂是
(3)已知:在一定条件下H2O2能和酸性高锰酸钾溶液反应生成O2,请完成下列缺项方程式的配平:




在该反应中H2O2作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】重铬酸钾( )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
(1) 中Cr的化合价为
中Cr的化合价为_______ 价,属于_______ (填“酸”、“碱”或“盐”)。
(2)当铬酸洗液变绿[溶液中 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 ,粉末氧化、滤去
,粉末氧化、滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的化学方程式为
粉末氧化时发生反应的化学方程式为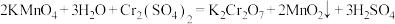 ,用单线桥法标明该反应的电子转移的方向和数目:
,用单线桥法标明该反应的电子转移的方向和数目:_______ ,滤去 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有_______ 。
(3)当铬酸洗液变黑失效时,可在硫酸酸化条件下加入铁屑将残留的 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 ,沉淀,其中铁屑将
,沉淀,其中铁屑将 转化成
转化成 的化学方程式为
的化学方程式为_______ ;若黑色铬酸洗液中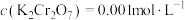 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为_______ g。
 )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:(1)
 中Cr的化合价为
中Cr的化合价为(2)当铬酸洗液变绿[溶液中
 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 ,粉末氧化、滤去
,粉末氧化、滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的化学方程式为
粉末氧化时发生反应的化学方程式为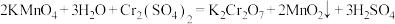 ,用单线桥法标明该反应的电子转移的方向和数目:
,用单线桥法标明该反应的电子转移的方向和数目: 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有(3)当铬酸洗液变黑失效时,可在硫酸酸化条件下加入铁屑将残留的
 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 ,沉淀,其中铁屑将
,沉淀,其中铁屑将 转化成
转化成 的化学方程式为
的化学方程式为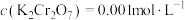 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原科,实验室常用 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个,此时被氧化的物质的物质的量为_______ mol。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)氯气是重要的化工原科,实验室常用
 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求书写下列反应的离子方程式。
(1)通常用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式为_______ ;
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是_______ 。
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是_______ 。
(4)锌粒投入稀H2SO4中,溶液里氢离子的量减少,锌离子的量增加,反应的离子方程式是_______ 。
(5)过氧化钠与水反应会产生氧气,写出该反应的离子方程式_______ 。
(1)通常用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式为
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是
(4)锌粒投入稀H2SO4中,溶液里氢离子的量减少,锌离子的量增加,反应的离子方程式是
(5)过氧化钠与水反应会产生氧气,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO中Cl的化合价为______ ,有较强的______ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式______ 。
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为______ ;
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为______ ;
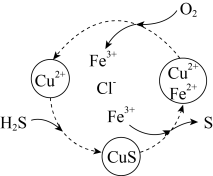
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有______ (写元素符号),Fe2+和Cu2+反应过程中起______ 作用,该图示的总反应的化学方程式为______ 。
(1)NaClO中Cl的化合价为
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列是中学化学中常见的几种物质 ①Ba(OH)2溶液;②乙醇(化学式为C2H6O);③Na2CO3;④干冰;⑤熔融NaHSO4;⑥盐酸;⑦过氧化钠固体;⑧Cu;⑨碳酸氢钠溶液。
(1)上述物质固态能够导电的是_________ (填物质序号,下同),属于氧化物的是__________ ,属于电解质的是__________ ,属于非电解质的是______________ ;
(2)写出NaHSO4在熔融状态下的电离方程式__________________ ;写出碳酸钠溶于水的电离方程式_________________________ ;
(3)向⑥中逐滴滴入⑨,实验现象为_________________________ ;过量⑤溶液与①溶液反应的化学方程式为______________________ ;请写出用⑥鉴别⑨和③溶液的操作方法和现象_________________________ 。
(1)上述物质固态能够导电的是
(2)写出NaHSO4在熔融状态下的电离方程式
(3)向⑥中逐滴滴入⑨,实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】⑴Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法是_________________ ,反应的化学方程式为________________________
⑵若NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的方法是____________________ 。
⑵若NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如Ⅰ~Ⅳ所示(部分夹持装置已略去)
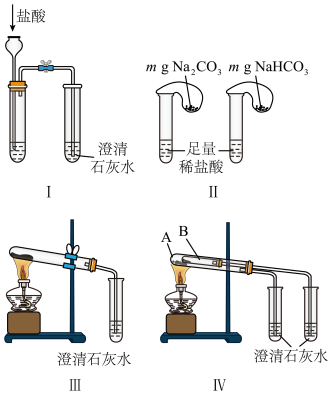
(1)图Ⅰ、Ⅱ所示实验中能够达到实验目的的是_______ (填序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为_______ 。
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是_______ (填化学式)。
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当碳酸氢钠与氢氧化钙的物质的量之比为2:1时,所得溶液中溶质的化学式为_______ ,请设计实验检验所得溶液中溶质的阴离子_______

(1)图Ⅰ、Ⅱ所示实验中能够达到实验目的的是
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当碳酸氢钠与氢氧化钙的物质的量之比为2:1时,所得溶液中溶质的化学式为
您最近一年使用:0次



