完成下列反应的反应方程式:
(1)NaOH溶液吸收氯气的反应:____________________________
(2)铁与水蒸气在高温下的反应:____________________________
(3)氢氧化铁溶于盐酸:____________________________
(4)铝单质溶解在氢氧化钠溶液中:____________________________
(5)过氧化钠与二氧化碳反应:____________________________
(1)NaOH溶液吸收氯气的反应:
(2)铁与水蒸气在高温下的反应:
(3)氢氧化铁溶于盐酸:
(4)铝单质溶解在氢氧化钠溶液中:
(5)过氧化钠与二氧化碳反应:
更新时间:2016-01-06 11:48:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气是一种重要的化工原料,从氯气的发现到氯元素的确认,经历了数位科学家30多年的不懈探索,根据相关信息,回答下列问题:
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的_________ 色气体,完成该反应的化学方程式:_______________ 。
(2)除去氯气中的HCl,可以使用的试剂是_______ ,最合理的氯气发生装置是_______ (填字母)。

(3)化学家贝托莱将Cl2的水溶液露置在阳光下,生成一种无色无味气体,该气体为____ ,写出该反应的化学方程式:__________ 。
(4)化学家泰耐特将Cl2通入石灰乳中得到漂白粉,该混合物具有漂白作用的物质是______ (填化学式)
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的
(2)除去氯气中的HCl,可以使用的试剂是

(3)化学家贝托莱将Cl2的水溶液露置在阳光下,生成一种无色无味气体,该气体为
(4)化学家泰耐特将Cl2通入石灰乳中得到漂白粉,该混合物具有漂白作用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
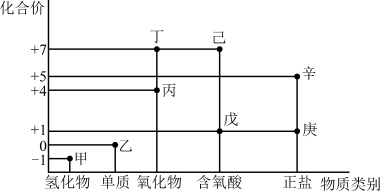
(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是_____ 。
(2)戊的结构式为______ ;甲、乙、丙、戊中,属于非电解质的是______ (填化学式)。
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是_____ (填字母序号)。
a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和NaOH溶液生产此消毒液的离子方程式______ ;该“84消毒液”有效成分的物质的量浓度为_____ (结果保留1位小数)。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为_____ mL(结果保留1位小数).若所配制的稀硫酸浓度大于0.90mol/L,则可能的原因是_____ 。
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容

(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是
(2)戊的结构式为
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
| 84消毒液 有效成分 NaClO 规格 500mL 质量分数 25% 密度 1.19g•cm-3 |
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识填写下列空白。
(1)在标准状况下,1.7g氨气与同条件下_______  含有相同的氢原子数。
含有相同的氢原子数。
(2)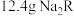 含
含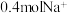 ,则
,则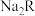 的摩尔质量为
的摩尔质量为_______ 。
(3)过氧化钠可用作制氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下, “人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是_______ 。
(5) 某硫酸盐溶液中含
某硫酸盐溶液中含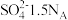 个,含金属离子
个,含金属离子 个,则该硫酸盐溶液的物质的量浓度为
个,则该硫酸盐溶液的物质的量浓度为_______  。
。
(6)下列各溶液中,氯离子的物质的量浓度与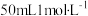 的
的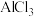 溶液中氯离子物质的量浓度相等的是
溶液中氯离子物质的量浓度相等的是_____ ,(填写符号)氯离子数目与 的
的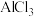 溶液中氯离子数目相等的是
溶液中氯离子数目相等的是____ 。(填写符号)
A.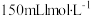 的
的 B.
B.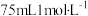 的
的
C.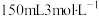 的
的 D.
D.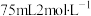 的
的
(1)在标准状况下,1.7g氨气与同条件下
 含有相同的氢原子数。
含有相同的氢原子数。(2)
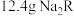 含
含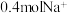 ,则
,则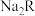 的摩尔质量为
的摩尔质量为(3)过氧化钠可用作制氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,
 “人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是(5)
 某硫酸盐溶液中含
某硫酸盐溶液中含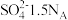 个,含金属离子
个,含金属离子 个,则该硫酸盐溶液的物质的量浓度为
个,则该硫酸盐溶液的物质的量浓度为 。
。(6)下列各溶液中,氯离子的物质的量浓度与
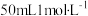 的
的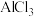 溶液中氯离子物质的量浓度相等的是
溶液中氯离子物质的量浓度相等的是 的
的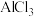 溶液中氯离子数目相等的是
溶液中氯离子数目相等的是A.
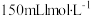 的
的 B.
B.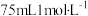 的
的
C.
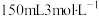 的
的 D.
D.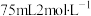 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与人类生产、生活密切相关,按要求回答下列问题。
(1)钠的化合物中,可用作潜水艇中供氧剂的是______ ,其与 发生反应的化学方程式为
发生反应的化学方程式为_____ 。
(2)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_____(填字母)。
(3)高铁酸钾 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: 。
。
①该反应中还原剂是_____ (填化学式,下同),还原产物为_________ 。
②当反应中有 生成,转移电子的物质的量为
生成,转移电子的物质的量为_____  。
。
(4)同温同压下,等体积的NH3和H2S气体的质量之比为_______ ;等物质的量的NH3和H2S中氢原子的个数比为_______ ;将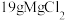 粉末溶于水配制成1L 溶液,从中取出50mL溶液,则Cl-的物质的量浓度为
粉末溶于水配制成1L 溶液,从中取出50mL溶液,则Cl-的物质的量浓度为______ 。
(1)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(2)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_____(填字母)。
A. | B. | C. | D. |
 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: 。
。①该反应中还原剂是
②当反应中有
 生成,转移电子的物质的量为
生成,转移电子的物质的量为 。
。(4)同温同压下,等体积的NH3和H2S气体的质量之比为
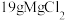 粉末溶于水配制成1L 溶液,从中取出50mL溶液,则Cl-的物质的量浓度为
粉末溶于水配制成1L 溶液,从中取出50mL溶液,则Cl-的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求写出下列方程式。
(1)过量碳酸氢钠溶液与石灰水反应的离子方程式:_______ 。
(2)氢氧化铁胶体制备的离子方程式:_______ 。
(3)氯化铁溶液与硫氰化钾反应的离子方程式:_______ 。
(4)铝与氢氧化钠溶液反应离子方程式:_______ 。
(5)硫酸亚铁与酸性高锰酸钾溶液的离子方程式:_______ 。
(6)足量的氯气与溴化亚铁溶液反应的离子方程式:_______ 。
(7)氯酸钾与浓盐酸混合可生成氯气、氯化钾和水,写出化学方程式:_______ 。其中,氧化产物和还原产物的质量之比为_______ 。
(1)过量碳酸氢钠溶液与石灰水反应的离子方程式:
(2)氢氧化铁胶体制备的离子方程式:
(3)氯化铁溶液与硫氰化钾反应的离子方程式:
(4)铝与氢氧化钠溶液反应离子方程式:
(5)硫酸亚铁与酸性高锰酸钾溶液的离子方程式:
(6)足量的氯气与溴化亚铁溶液反应的离子方程式:
(7)氯酸钾与浓盐酸混合可生成氯气、氯化钾和水,写出化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
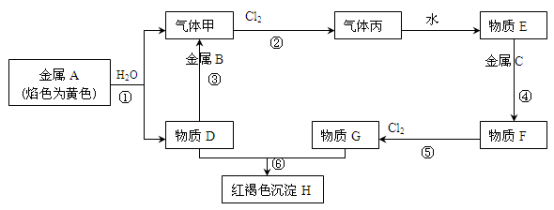
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、镁、铝、铁是四种重要的金属。请回答:
(1)钠的金属活动性比铝的______ (填“强”或“弱”)。
(2)钠与水反应,观察不到的实验现象是______ (填编号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3) 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为______ 。
(4)铁在高温时与水蒸气反应的化学方程式为______ 。
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是______ 。
A.Na+ B.Mg2+ C.OH- D.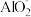
(1)钠的金属活动性比铝的
(2)钠与水反应,观察不到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)
 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为(4)铁在高温时与水蒸气反应的化学方程式为
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是
A.Na+ B.Mg2+ C.OH- D.
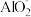
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期律的重要性。如表列出了元期表中短周期的一部分,a~i代表9种短周期元素。
已知c与氢元素能组成生活中最常见的化合物X。回答下列问题:
(1)元素h在周期表中位于第_______ 族,g的原子结构示意图为_______ 。
(2)由元素d与e组成的化合物的电子式为_______ 。
(3)a~i中,非金属性最强的是_______ (填元素符号);f、g、h、i四种元素的最高价氧化物对应的水化物中,酸性最强的化合物的化学式为_______ 。
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为_______ 。
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为_______ 。
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,_______ 。
| a | b | c | d | |||
| e | f | g | h | i |
(1)元素h在周期表中位于第
(2)由元素d与e组成的化合物的电子式为
(3)a~i中,非金属性最强的是
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学学科中由于物质种类和反应的多样性,用分类法对其进行学习是很好的学习方法,通过类别思想和价态规律来分析物质的性质成为重要的学习思路,同时需要将定性和学科知识进行定量的计算。结合所学完成下面问题。
(1)写出Na2O2与水反应的离子方程式_______________________________ 。
(2)碳酸钠溶液中滴加盐酸开始无气泡后缓慢产生气泡的对应的两个离子方程式为_________________ 、____________________ 。
(3)将CO2气体通入事先通入氨气的饱和食盐水中,写出反应的化学方程式_________________ 。
(4)写出Fe与H2O蒸气反应的化学方程式________________ 。反应生成4个氢气时转移电子数为_______________ 。
(5)Fe3+检验所用的试剂名称为________ 。
(1)写出Na2O2与水反应的离子方程式
(2)碳酸钠溶液中滴加盐酸开始无气泡后缓慢产生气泡的对应的两个离子方程式为
(3)将CO2气体通入事先通入氨气的饱和食盐水中,写出反应的化学方程式
(4)写出Fe与H2O蒸气反应的化学方程式
(5)Fe3+检验所用的试剂名称为
您最近一年使用:0次



