现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
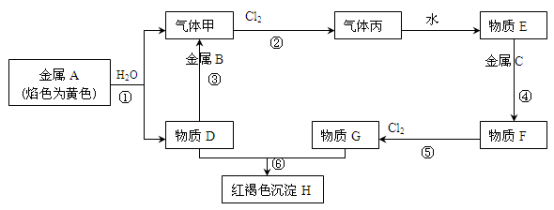
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
14-15高一上·吉林白城·期末 查看更多[2]
更新时间:2016-12-09 07:04:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在一定条件下有以下转化关系,已知A、B、C中均含有同种元素。请回答下列问题。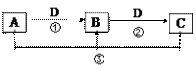
(1)若D为日常生活中最常见的金属单质之一,且以上反应均为氧化还原反应;除以上四种物质外,整个转化过程中没有其它物质参与或生成。
①构成D单质的元素在周期表中的位置是_______ ;
②反应③的离子方程式_______ 。
③试叙述检验物质B中阳离子的实验方法_______ 。
(2)若无反应③的转化过程,C为红棕色气体,试分析:
①A、B、C中含有的共同元素为(写名称):_______ 。
②C与H2O反应的化学方程式为_______ 。
③若A为化合物时其电子式为_______ 。
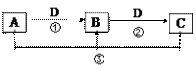
(1)若D为日常生活中最常见的金属单质之一,且以上反应均为氧化还原反应;除以上四种物质外,整个转化过程中没有其它物质参与或生成。
①构成D单质的元素在周期表中的位置是
②反应③的离子方程式
③试叙述检验物质B中阳离子的实验方法
(2)若无反应③的转化过程,C为红棕色气体,试分析:
①A、B、C中含有的共同元素为(写名称):
②C与H2O反应的化学方程式为
③若A为化合物时其电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在无氧的条件下以干燥的钠汞齐(以Na-Hg表示)和干燥的二氧化硫一起振荡,得固态化合物A。已知:A中钠元素的质量分数为26.44%,氧元素的质量分数为36.78%,其余为S元素。1mol A暴露在潮湿空气中易吸收氧气而氧化,其氧化产物需2 mol NaOH反应生成正盐。
(1)试确定A的化学式_______ 。
(2)若将A加热到402K时能产生一种刺激性气味的气体,固体质量减轻了18.39%。分析得到的固体残渣,发现是与A含有相同元素的两种物质(记为B和C)。试写出A分解的化学方程式_______ 。
(1)试确定A的化学式
(2)若将A加热到402K时能产生一种刺激性气味的气体,固体质量减轻了18.39%。分析得到的固体残渣,发现是与A含有相同元素的两种物质(记为B和C)。试写出A分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一块表面已经被部分氧化成氧化钠的钠块,质量为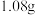 ,投入到
,投入到 水中,完全反应后收集到
水中,完全反应后收集到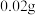 氢气。通过计算回答:
氢气。通过计算回答:
(1)未被氧化的钠的质量是___________ 。
(2)钠块表面被氧化的钠的质量是___________ 。
(3)①若将氧化钠投入紫色石蕊试液中,现象为___________ 。
②若将过氧化钠投入紫色石蕊试液中,现象为___________ 。
(4)若向饱和烧碱溶液中加入一定量过氧化钠,则
___________ (填“变大”“变小”或“不变”,下同),
___________ 。
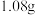 ,投入到
,投入到 水中,完全反应后收集到
水中,完全反应后收集到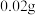 氢气。通过计算回答:
氢气。通过计算回答:(1)未被氧化的钠的质量是
(2)钠块表面被氧化的钠的质量是
(3)①若将氧化钠投入紫色石蕊试液中,现象为
②若将过氧化钠投入紫色石蕊试液中,现象为
(4)若向饱和烧碱溶液中加入一定量过氧化钠,则


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠,铝,铁是三种重要的金属,请回答下列问题:
(1)钠的金属活动性比铝的__________ (填“强”或“弱”)。
(2)将一小块钠投入水中,发生反应的离子方程式为____________________ ;
可观察到的实验现象是_____________ (填序号)
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)将一小块铝投入到饱和氢氧化钠溶液中,发生反应的化学方程式为____________________________
(4)Fe和Cl2 在一定条件下反应,所的产物的化学式是_________ 将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.若向另一支试管中滴加NaOH溶液,现象为_____________________________ ,反应的离子方程式是__________________________________________________________________
(1)钠的金属活动性比铝的
(2)将一小块钠投入水中,发生反应的离子方程式为
可观察到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)将一小块铝投入到饱和氢氧化钠溶液中,发生反应的化学方程式为
(4)Fe和Cl2 在一定条件下反应,所的产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.若向另一支试管中滴加NaOH溶液,现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程:
[提出假设] 假设1 该混合金属粉末中除铝外还含有_____ 元素;
假设2 该混合金属粉末中除铝外还含有_____ 元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
[设计实验方案]基于假设3,设计出实验方案(不要在答题卡上作答)。
[实验过程]根据上述实验方案,完成实验的相关操作、预期现象和结论。
[反思】写出在实验①中发生反应的离子方程式:___________________________________ 。
[提出假设] 假设1 该混合金属粉末中除铝外还含有
假设2 该混合金属粉末中除铝外还含有
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
[设计实验方案]基于假设3,设计出实验方案(不要在答题卡上作答)。
[实验过程]根据上述实验方案,完成实验的相关操作、预期现象和结论。
| 编号 | 实验操作 | 实验现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量 | 有固体剩余,并有气泡产生 | 合金中除铝外还含有Fe、Cu 元素 |
| ② | 往试管A的剩余固体中加过量 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | |
| ③ | 往试管B中加入少量 | ||
| ④ | 往②剩余固体中加入稀硝酸;再滴加 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色;再加某溶液后有蓝色沉淀产生 |
[反思】写出在实验①中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
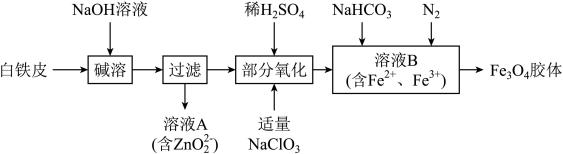
【推荐2】利用废旧白铁皮(含Fe、Zn、Fe2O3、ZnO)制备磁性Fe3O4胶体流程如下:
已知:锌及其化合物的性质与铝及其化合物的性质具有一定的相似性。
(1)碱溶时除了发生反应Zn + 2NaOH = Na2ZnO2 + H2↑以外,还发生的另一反应化学方程式为:___ 。
(2)过滤后得到的滤渣是_______ 。

已知:锌及其化合物的性质与铝及其化合物的性质具有一定的相似性。
(1)碱溶时除了发生反应Zn + 2NaOH = Na2ZnO2 + H2↑以外,还发生的另一反应化学方程式为:
(2)过滤后得到的滤渣是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】正误判断
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
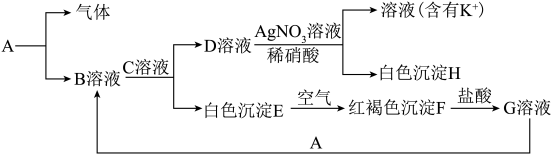
【推荐2】已知存在以下物质之间的相互转化,分别写出下列物质的化学式:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 、F_______ 、G_______ 、H_______ ,并写出每步转化反应的离子方程式_______ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
(1)c(H+)=___________ mol/L。
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O)。
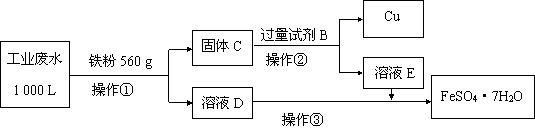
① 工业废水中加入铁粉后,反应的离子方程式为:
Fe + Cu2+= Fe2++ Cu、____________ 、____________ 。
② 试剂B是__________ 。
③ 操作③是蒸发浓缩、冷却结晶、___________ ,最后用少量冷水洗涤晶体,在低温下干燥。
④ 通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是____________ 。
⑤ 获得的FeSO4·7H2O需密闭保存,原因是___________ 。
⑥ 上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是________ mol。
| 离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
| 浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)=
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O)。

① 工业废水中加入铁粉后,反应的离子方程式为:
Fe + Cu2+= Fe2++ Cu、
② 试剂B是
③ 操作③是蒸发浓缩、冷却结晶、
④ 通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是
⑤ 获得的FeSO4·7H2O需密闭保存,原因是
⑥ 上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是
您最近一年使用:0次



