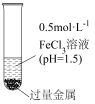
钠,铝,铁是三种重要的金属,请回答下列问题:
(1)钠的金属活动性比铝的__________ (填“强”或“弱”)。
(2)将一小块钠投入水中,发生反应的离子方程式为____________________ ;
可观察到的实验现象是_____________ (填序号)
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)将一小块铝投入到饱和氢氧化钠溶液中,发生反应的化学方程式为____________________________
(4)Fe和Cl2 在一定条件下反应,所的产物的化学式是_________ 将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.若向另一支试管中滴加NaOH溶液,现象为_____________________________ ,反应的离子方程式是__________________________________________________________________
(1)钠的金属活动性比铝的
(2)将一小块钠投入水中,发生反应的离子方程式为
可观察到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)将一小块铝投入到饱和氢氧化钠溶液中,发生反应的化学方程式为
(4)Fe和Cl2 在一定条件下反应,所的产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.若向另一支试管中滴加NaOH溶液,现象为
更新时间:2018-03-29 01:52:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)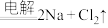 。
。
(1)保存金属钠的正确方法是___________(填字母)。
(2)Na、NaOH久置在空气中最终都是变为___________ (填化学式)。
(3)根据金属钠与水(滴有酚酞)反应的现象,下列有关说法错误的是___________(填字母)。
(4)检验物质所含钠元素的方法___________ 。
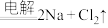 。
。(1)保存金属钠的正确方法是___________(填字母)。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
(3)根据金属钠与水(滴有酚酞)反应的现象,下列有关说法错误的是___________(填字母)。
| A.钠熔化成闪亮的小球,说明钠的熔点低且反应放热 |
| B.反应后溶液的颜色逐渐变红,说明反应生成了碱 |
| C.该反应中每1 mol的Na得到1 mol的电子 |
| D.当火灾现场存放有大量金属钠时不能用水来灭火 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,N常用来杀菌消毒。请按要求填空:
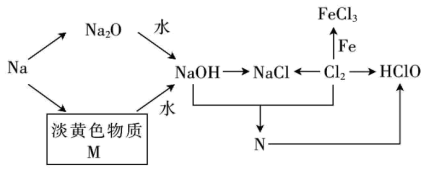
(1)淡黄色物质M是____ ,物质N是____ 。(填化学式)
(2)请描述一小块金属钠投入加酚酞的水中的现象:____ 。相关化学方程式为____ 。
(3)用化学方程式说明为什么M能够作为潜水艇中的供氧剂使用____ 。

(1)淡黄色物质M是
(2)请描述一小块金属钠投入加酚酞的水中的现象:
(3)用化学方程式说明为什么M能够作为潜水艇中的供氧剂使用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知,有一质量分数为40%的NaOH溶液,密度为1.42g/mL,求:
(1)该NaOH溶液的物质的量浓度为___________ ;
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为___________ ;
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克___________ ?(该题请写出相应的计算过程,没过程不得分。)
(1)该NaOH溶液的物质的量浓度为
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮化铝(AlN)是一种新型材料,硬度大、耐高温、耐腐蚀。
(1)Al在周期表中的位置是___ 。与Al同周期,金属性最强的是___ ,它的最高价氧化物对应水化物与Al的化学反应方程式为___ 。
(2)比较原子半径大小:r(N)___ r(F)(填>、<或=),写出F原子的结构示意图:___ ,写出N原子的电子式:___ 。
(3)请写出一条能证明F的非金属性比N强的事实:___ 。
(1)Al在周期表中的位置是
(2)比较原子半径大小:r(N)
(3)请写出一条能证明F的非金属性比N强的事实:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有一块铝铁合金,加入到足量氢氧化钠溶液,滤出不溶物洗涤后再用一定量盐酸恰好完全溶解,继续在溶液中加入足量氨水,在空气中静置至红褐色沉淀不再增加为止,将沉淀滤出再灼烧至恒重,得到残留 固体的质量与原合金的质量相同,则:
(1)合金溶于足量氢氧化钠溶液所得溶液中含有的阴离子有______ 、_______ ;
(2)沉淀滤出再灼烧至恒重,得到残留固体的化学式为____________________ ;
(3)合金中铝的质量分数为__________ 。
(1)合金溶于足量氢氧化钠溶液所得溶液中含有的阴离子有
(2)沉淀滤出再灼烧至恒重,得到残留固体的化学式为
(3)合金中铝的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】填空。
(1)在MgCl2溶液中滴加过量NaOH溶液,现象为_______ ;在AlCl3溶液中滴加过量NaOH溶液,现象为_______ ,写出该现象的离子反应方程式_______ 。
(2)铝制易拉罐中充满CO2,然后往易拉罐中充入足量的浓NaOH溶液,立即用胶布封严罐口,一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪;再过一会儿易拉罐又恢复原样,请根据现象填空。
①易拉罐变瘪是因为_______ ;
②易拉罐恢复原样原因是_______ (写出反应的化学方程式);
(3)有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、Na2SO4。将它们分别与H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。则A是_______ ,B是 _______ ,C是_______ 。
(1)在MgCl2溶液中滴加过量NaOH溶液,现象为
(2)铝制易拉罐中充满CO2,然后往易拉罐中充入足量的浓NaOH溶液,立即用胶布封严罐口,一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪;再过一会儿易拉罐又恢复原样,请根据现象填空。
①易拉罐变瘪是因为
②易拉罐恢复原样原因是
(3)有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、Na2SO4。将它们分别与H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。则A是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用化学变化的递变规律,常可对某些物质的化学性质作出合理的推测,请判断下列各推测是否合理(填合理、不合理或不一定合理),并说明判断的理由。
(1)从红热的铜丝能在氯气中燃烧的事实,推测红热的铁丝也能在氯气中燃烧。
(2)从铁粉和硫粉加热条件下能发生反应的事实,推测铜粉和硫粉在相同加热条件下也一定能发生反应。
(3)从SO2通入Ba(OH)2溶液能产生白色沉淀的事实,推测SO2通入BaCl2溶液也能产生白色沉淀。
(4)从反应2CO2+2Na2O2==2Na2CO3+O2的事实,推测二氧化硫也一定能发生反应:
2SO2 +2Na2O2==2Na2SO3+O2。
(1)从红热的铜丝能在氯气中燃烧的事实,推测红热的铁丝也能在氯气中燃烧。
(2)从铁粉和硫粉加热条件下能发生反应的事实,推测铜粉和硫粉在相同加热条件下也一定能发生反应。
(3)从SO2通入Ba(OH)2溶液能产生白色沉淀的事实,推测SO2通入BaCl2溶液也能产生白色沉淀。
(4)从反应2CO2+2Na2O2==2Na2CO3+O2的事实,推测二氧化硫也一定能发生反应:
2SO2 +2Na2O2==2Na2SO3+O2。
| 题号 | 是否合理 | 理 由 |
| (1) | ||
| (2) | ||
| (3) | ||
| (4) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A、B、C 为中学常见单质,其中一种为金属;通常情况下,A 为固体,B 为液体,C 为气体。D、 E、F、G、H、X 均为化合物,其中 X 是一种无氧强酸、E 为黑色固体,H 在常温下为液体。它们之间的 转化关系如图所示(其中某些反应条件和部分反应物已略去)。
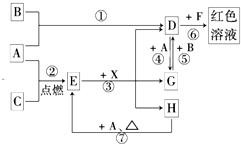
(1)写出化学式:A____________ 、D__________ 、E__________ 、X________ 。
(2) 在反应①~⑦中,不属于氧化还原反应的是__________ (填编号)。
(3) 反应⑥的离子方程式为__________ 。
(4)反应⑦的化学方程式为__________ ,该反应中每消耗 0.3molA,可转移电子__________ mol。

(1)写出化学式:A
(2) 在反应①~⑦中,不属于氧化还原反应的是
(3) 反应⑥的离子方程式为
(4)反应⑦的化学方程式为
您最近一年使用:0次
【推荐3】铁及其化合物与生产、生活关系密切:
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
(2) 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式_______ 。向反应后的溶液加入_______ (填名称),可回收Cu,并得到 溶液。
溶液。
(3)用废铁皮制取( )的部分流程示意图如下:
)的部分流程示意图如下:_______ 。
(4) 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为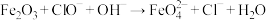 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5) 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。当该反应转移1.2mol电子时,能产生_______ mol 。
。
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
A. | B. | C. | D. |
(2)
 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式 溶液。
溶液。(3)用废铁皮制取(
 )的部分流程示意图如下:
)的部分流程示意图如下: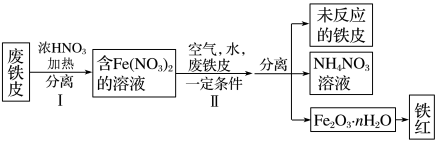
(4)
 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为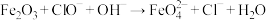 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(5)
 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】以 溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
Ⅰ.金属与 溶液反应
溶液反应
(1)配制 溶液,需要
溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是
将固体先溶于浓盐酸,再稀释至指定浓度,原因是___________ 。
(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过___________ 可以快速判断其是否为胶体。
(3) 溶液与Cu反应的离子方程式为
溶液与Cu反应的离子方程式为___________ ,实验ⅰ和ⅱ均先有气体生成,后有溶液颜色的变化,甲同学认为产生该现象的原因可能是此实验条件下氧化性: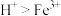 ,乙同学认为可以根据ⅲ判断氧化性:
,乙同学认为可以根据ⅲ判断氧化性: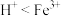 ,理由是
,理由是___________ 。
Ⅱ. 溶液与
溶液与 溶液反应:
溶液反应: ,产生蓝色沉淀,推测
,产生蓝色沉淀,推测 与
与 反应的离子方程式是
反应的离子方程式是___________ 。
(5)另取红棕色溶液少许,检测其为胶体,向其中继续滴加 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是___________ 。
(6)结合(4)、(5),推测 溶液与
溶液与 溶液反应同时存在
溶液反应同时存在__________ 反应和___________ 反应。从下列选项选择:
A.复分解 B.双水解 C.置换 D.氧化还原
 溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:Ⅰ.金属与
 溶液反应
溶液反应| 装置 | 序号 | 金属 | 现象及产物检验 |
| ⅰ | 镁条 | 立即产生大量气体,溶液颜色变红棕色; 片刻后气泡减少,金属表面产生红褐色沉淀。 |
| ⅱ | 锌粒 | 开始时无明显气泡,半分钟后有气体产生,溶液颜色慢慢加深;一段时间后,金属表面产生红棕色沉淀 | |
| ⅲ | 铜粉 | 无气体产生,溶液逐渐变为蓝绿色; |
(1)配制
 溶液,需要
溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是
将固体先溶于浓盐酸,再稀释至指定浓度,原因是(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过
(3)
 溶液与Cu反应的离子方程式为
溶液与Cu反应的离子方程式为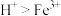 ,乙同学认为可以根据ⅲ判断氧化性:
,乙同学认为可以根据ⅲ判断氧化性: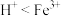 ,理由是
,理由是Ⅱ.
 溶液与
溶液与 溶液反应:
溶液反应: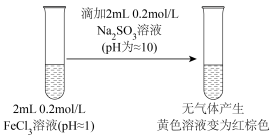
 ,产生蓝色沉淀,推测
,产生蓝色沉淀,推测 与
与 反应的离子方程式是
反应的离子方程式是(5)另取红棕色溶液少许,检测其为胶体,向其中继续滴加
 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是(6)结合(4)、(5),推测
 溶液与
溶液与 溶液反应同时存在
溶液反应同时存在A.复分解 B.双水解 C.置换 D.氧化还原
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)若金属钠等活泼金属着火时,应该用__________ 来灭火。金属钠应保存在__________ 中。
(2)胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:_________________ 。
(3)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作__ 剂,具有_______ 性;
(4)过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是_________ 、___________ 。
(5)Fe与Cl2在一定条件下反应,所得产物的化学式是________ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为________________ ,反应的离子方程式是__________ 。
(6)纯净的H2在Cl2中燃烧发出________ 色火焰。
(1)若金属钠等活泼金属着火时,应该用
(2)胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:
(3)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作
(4)过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是
(5)Fe与Cl2在一定条件下反应,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(6)纯净的H2在Cl2中燃烧发出
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是___ ,证明Fe3+存在的现象是___ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式___ 。
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
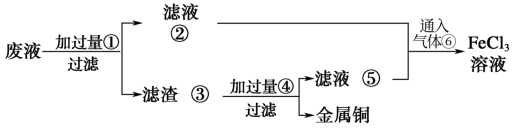
请写出上述实验中加入或生成的有关物质的化学式。
①___ ,④___ 。
(4))写出向②⑤的混合液中通入⑥的离子方程式:___ 。
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为___ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式。
①
(4))写出向②⑤的混合液中通入⑥的离子方程式:
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次