已知,有一质量分数为40%的NaOH溶液,密度为1.42g/mL,求:
(1)该NaOH溶液的物质的量浓度为___________ ;
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为___________ ;
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克___________ ?(该题请写出相应的计算过程,没过程不得分。)
(1)该NaOH溶液的物质的量浓度为
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克
更新时间:2022-12-05 19:43:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室需要使用1.0mol/LNaOH溶液80mL。
(1)配制该NaOH溶液所需容量瓶的规格是_______ 。
(2)用托盘天平称取NaOH固体_______ g。
(3)称量完成后,进行如下操作:
A.将称好的NaOH固体放在烧杯中,用适量蒸馏水溶解。
B.待固体全部溶解后,将溶液立即转移到容量瓶。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也都用玻璃棒引流注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
D.继续向容量瓶加蒸馏水至液面离容量瓶颈刻度线下_______ cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。
E.盖好瓶塞,反复上下颠倒,摇匀。
上述操作不正确的是_______ (填序号)。
(4)若未进行上述操作C,则所得溶液浓度_______ (填“偏高”“偏低”或“无影响”,下同)。若定容时如下图操作,则所得溶液浓度_______ 。

(5)取上述溶液10mL稀释至50mL,所得NaOH溶液的物质的量浓度为_______ 。
(1)配制该NaOH溶液所需容量瓶的规格是
(2)用托盘天平称取NaOH固体
(3)称量完成后,进行如下操作:
A.将称好的NaOH固体放在烧杯中,用适量蒸馏水溶解。
B.待固体全部溶解后,将溶液立即转移到容量瓶。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也都用玻璃棒引流注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
D.继续向容量瓶加蒸馏水至液面离容量瓶颈刻度线下
E.盖好瓶塞,反复上下颠倒,摇匀。
上述操作不正确的是
(4)若未进行上述操作C,则所得溶液浓度

(5)取上述溶液10mL稀释至50mL,所得NaOH溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
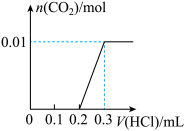
【推荐2】将一定量的NaOH和Na2CO3混合并配成溶液,向溶液中滴加0.1mol•L−1稀盐酸。加入盐酸的体积和生成CO2的物质的量的关系如图所示,请回答下列问题:
(1)该实验需要配制450mL、0.1mol•L−1的稀盐酸。除了需要用到量筒、烧杯、胶头滴管之外,还需要用到的玻璃仪器是___ 。
(2)若用浓度为10mol•L-1的盐酸来配制0.1mol•L-1稀盐酸,需要量取该盐酸___ mL。
(3)据图所示,当加入盐酸体积0.2~0.3L时的离子方程式为___ 。
(4)根据已知数据可知混合溶液中NaOH的物质的量为___ mol。

(1)该实验需要配制450mL、0.1mol•L−1的稀盐酸。除了需要用到量筒、烧杯、胶头滴管之外,还需要用到的玻璃仪器是
(2)若用浓度为10mol•L-1的盐酸来配制0.1mol•L-1稀盐酸,需要量取该盐酸
(3)据图所示,当加入盐酸体积0.2~0.3L时的离子方程式为
(4)根据已知数据可知混合溶液中NaOH的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目___________ 。
(2)该反应氧化剂是(填化学式)___________ ,氧化产物是(填化学式)___________ 。
(3)浓盐酸在反应中显示出来的性质是___________ 。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生10个Cl2,则被氧化的HCl为_______ 个,转移电子的数目为________ 个。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目
(2)该反应氧化剂是(填化学式)
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生10个Cl2,则被氧化的HCl为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高锰酸钾是种常见的氧化剂。能氧化乙烯、乙醇、草酸等有机物。酒后驾车已成为一个社会问题。检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种。早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:3CH3CH2OH+2KMnO4→3CH3CHO(乙醛)+2MnO2↓+2KOH+2H2O。完成下列填空:
(1)写出乙醇所含官能团的电子式:______ 。
(2)在乙醇分子中,3种原子的半径由小到大的顺序为______ (用元素符号表示)。其中C、O两种元素非金属性较强的是______ (填元素名称)。
(3)上述反应中发生氧化反应的过程是______ →______ 。
(4)已知KMnO4在酸性条件下氧化性增强,能得到更多的电子,生成Mn2+。用稀硫酸酸化的KMnO4氧化乙醇可生成乙酸(CH3COOH),则反应中氧化剂与还原剂物质的量之比为______ 。
(5)小张同学想用酸性高锰酸钾溶液来除去乙烷中的乙烯杂质。你会告诉他,若要达到实验目的,还需要用到的试剂是______ (填化学式)。
(6)草酸(H2C2O4)是二元弱酸,它的酸式盐NaHC2O4溶液既能与盐酸反应,又能与NaOH溶液反应。用平衡移动观点解释NaHC2O4溶液能与NaOH溶液反应的原因:______ 。
(1)写出乙醇所含官能团的电子式:
(2)在乙醇分子中,3种原子的半径由小到大的顺序为
(3)上述反应中发生氧化反应的过程是
(4)已知KMnO4在酸性条件下氧化性增强,能得到更多的电子,生成Mn2+。用稀硫酸酸化的KMnO4氧化乙醇可生成乙酸(CH3COOH),则反应中氧化剂与还原剂物质的量之比为
(5)小张同学想用酸性高锰酸钾溶液来除去乙烷中的乙烯杂质。你会告诉他,若要达到实验目的,还需要用到的试剂是
(6)草酸(H2C2O4)是二元弱酸,它的酸式盐NaHC2O4溶液既能与盐酸反应,又能与NaOH溶液反应。用平衡移动观点解释NaHC2O4溶液能与NaOH溶液反应的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.回答下列问题:
(1)人体缺乏某种微量元素将导致血液输送氧气能力下降,人体就无法获得充足的氧气,生理机能就会下降,该微量元素是_____ (填字母)。
a.碘 b.锌 c.铁
(2)抗生素是抑制某些微生物生长或杀灭某些微生物的一类物质,下列属于抗生素的是_____ (填字母)。
a.阿莫西林 b.胃舒平 c.阿司匹林
II.表中是我国部分城市空气质量周报,回答下列问题:(TSP—空气中的飘尘)
(3)最容易出现酸雨的城市是____ 。
(4)NaOH溶液可吸收废气中的氮氧化物,反应方程式:2NO2+2NaOH=NaNO2+NaNO3+H2O。反应时消耗了10L0.1mol•L-1NaOH溶液,则反应中转移电子的数目为:____ 。
III.湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如表:
(5)现有某工厂每日排放的污水中汞的质量分数为(1×10-6)%,镉的质量分数为(2×10-5)%,铅的质量分数为(5×10-5)%(设该污水的密度为1g/cm3)。根据计算该厂三项污染物中____ 超标。
(1)人体缺乏某种微量元素将导致血液输送氧气能力下降,人体就无法获得充足的氧气,生理机能就会下降,该微量元素是
a.碘 b.锌 c.铁
(2)抗生素是抑制某些微生物生长或杀灭某些微生物的一类物质,下列属于抗生素的是
a.阿莫西林 b.胃舒平 c.阿司匹林
II.表中是我国部分城市空气质量周报,回答下列问题:(TSP—空气中的飘尘)
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 城市 | 污染指数 | 首要污染物 | 空气质量级别 |
| 天津 | 82 | TSP | II | 武汉 | 83 | NOx | II |
| 哈尔滨 | 96 | TSP | II | 重庆 | 98 | SOx | II |
(4)NaOH溶液可吸收废气中的氮氧化物,反应方程式:2NO2+2NaOH=NaNO2+NaNO3+H2O。反应时消耗了10L0.1mol•L-1NaOH溶液,则反应中转移电子的数目为:
III.湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如表:
| 污染物 | 汞 | 镉 | 铅 |
| 主要存在形式 | Hg2+ | Cd2+ | Pb2+ |
| 最高允许排放浓度/(mg•dm-3) | 0.05 | 0.1 | 1.0 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】取4.6g金属钠置于一定量的氧气中,加热使其充分反应,得到7.0g淡黄色固体。将7.0g淡黄色固体投入到100.0g水中。求:
(1)确定淡黄色固体的成分及质量为___________ 。
(2)淡黄色固体投入水中,发生反应的化学方程式为___________ 。
(3)最终所得溶液溶质的质量分数为___________ %(保留两位小数)。
(1)确定淡黄色固体的成分及质量为
(2)淡黄色固体投入水中,发生反应的化学方程式为
(3)最终所得溶液溶质的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠、铝、铁是三种重要的金属。请回答:
(1)钠的金属活动性比铝的________ (填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为_________________________ ;可观察到的实验现象是________ (填编号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)铝和氢氧化钠反应的化学方程式为:_____________ 。
(4)Fe跟Cl2在一定条件下反应,所得产物的化学式是________ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为____________________________ 。
(1)钠的金属活动性比铝的
(2)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)铝和氢氧化钠反应的化学方程式为:
(4)Fe跟Cl2在一定条件下反应,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
您最近一年使用:0次



 去除某些有机溶剂中水分的原因:
去除某些有机溶剂中水分的原因: 的用途
的用途

