补齐物质与其用途的连线,并回答问题。

(1)在上图补全用途与性质的连线___________ 。
(2)厨房中的食用碱,其化学成分属于___________ (填“酸”“碱”或“盐”)。
(3)用化学方程式解释 去除某些有机溶剂中水分的原因:
去除某些有机溶剂中水分的原因:___________ 。
(4)用化学方程式解释上图中 的用途
的用途___________ ,利用氧化还原反应理论分析此反应中 所体现的性质是
所体现的性质是___________ 。

(1)在上图补全用途与性质的连线
(2)厨房中的食用碱,其化学成分属于
(3)用化学方程式解释
 去除某些有机溶剂中水分的原因:
去除某些有机溶剂中水分的原因:(4)用化学方程式解释上图中
 的用途
的用途 所体现的性质是
所体现的性质是
更新时间:2024-02-28 15:35:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在反应 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是 ______ ,氧化产物是 ______ ,氧化产物与还原产物的物质的量之比为 ______ ,被氧化与未被氧化的HCl的质量之比为 ______ ,若有73gHCl被氧化,电子转移的总数为 ______ ,产生Cl2的质量为 ______ g.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高锰酸钾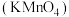 是一种广泛使用的氧化剂和消毒剂。
是一种广泛使用的氧化剂和消毒剂。
(1)测定室内甲醛含量,发生反应如下,配平该方程式,用单线桥标出电子转移方向与数目_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(2)将室内气体通入 酸性
酸性 溶液中,通入10L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为
溶液中,通入10L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为_______ mg/L;上述酸性 是指用硫酸酸化的
是指用硫酸酸化的 溶液,请说明不使用硝酸酸化的理由:
溶液,请说明不使用硝酸酸化的理由:_______ 。
(3)将 气体通入
气体通入 溶液中,溶液会逐渐褪色,体现
溶液中,溶液会逐渐褪色,体现 的性质为
的性质为_______ 。
(4) 溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式:
溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式:_______ 。
(5)0.01% 溶液可用于消毒蔬果和餐具,该溶液一般保存在棕色试剂瓶中,请解释原因:
溶液可用于消毒蔬果和餐具,该溶液一般保存在棕色试剂瓶中,请解释原因:_______ 。
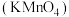 是一种广泛使用的氧化剂和消毒剂。
是一种广泛使用的氧化剂和消毒剂。(1)测定室内甲醛含量,发生反应如下,配平该方程式,用单线桥标出电子转移方向与数目
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(2)将室内气体通入
 酸性
酸性 溶液中,通入10L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为
溶液中,通入10L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为 是指用硫酸酸化的
是指用硫酸酸化的 溶液,请说明不使用硝酸酸化的理由:
溶液,请说明不使用硝酸酸化的理由:(3)将
 气体通入
气体通入 溶液中,溶液会逐渐褪色,体现
溶液中,溶液会逐渐褪色,体现 的性质为
的性质为(4)
 溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式:
溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式:(5)0.01%
 溶液可用于消毒蔬果和餐具,该溶液一般保存在棕色试剂瓶中,请解释原因:
溶液可用于消毒蔬果和餐具,该溶液一般保存在棕色试剂瓶中,请解释原因:
您最近一年使用:0次
【推荐3】I.某反应为:4CuI+Hg═Cu2HgI4+2Cu(反应前后的I均为﹣1价),试回答:
(1)上述反应产物Cu2HgI4中,Hg元素显___________ 价;
(2)CuI发生___________ 反应(填氧化或还原)。
II.某反应为:3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)反应中氧化剂是___________ (填化学式),被氧化的元素___________ (填元素符号);
(4)用单线桥表示出该反应中电子转移的方向和数目___________ 。
III.有下列三个反应:
a.2FeCl2+2KI═2FeCl2+2KCl+I2
b.2FeCl2+Cl2═2FeCl3
c.2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)上述三个反应中氧化剂氧化性强弱关系为___________ ;
(6)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是___________ 。
(1)上述反应产物Cu2HgI4中,Hg元素显
(2)CuI发生
II.某反应为:3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)反应中氧化剂是
(4)用单线桥表示出该反应中电子转移的方向和数目
III.有下列三个反应:
a.2FeCl2+2KI═2FeCl2+2KCl+I2
b.2FeCl2+Cl2═2FeCl3
c.2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)上述三个反应中氧化剂氧化性强弱关系为
(6)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都显黄色,A、B与水反应都有气体放出,A与水的反应放出的气体只具有氧化性,同时都生成溶液C,C与少量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能变成D。
(1)写出下列物质的化学式:A____________ 、C____________ 、E_____________ 。
(2)B与水反应的离子方程式是:______________________________________________ 。
(3)D溶液中通入CO2的离子方程式:__________________________________________ 。
(4)7.8g的A加入到足量的硫酸铜溶液中,标况下,产生气体的体积为________ L, 生成沉淀的质量为________ g。
(1)写出下列物质的化学式:A
(2)B与水反应的离子方程式是:
(3)D溶液中通入CO2的离子方程式:
(4)7.8g的A加入到足量的硫酸铜溶液中,标况下,产生气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某研究性学习小组设计出如图所示的装置,目的是做钠与水反应的实验并验证:①钠的某些物理性质;②钠与水反应的产物。
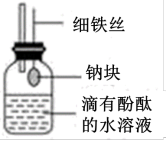
(1)钠与水反应的化学方程式为____ 。
(2)当进行适当操作时,还需要用到_____ 实验仪器。实验室取用一小块钠,若此钠块有极少量被氧化,则测出的相对原子质量会比实际相对原子质量________ (填“偏大”、“偏小”或“不变”)。
(3)钠与水反应的现象很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是________ 。
②能证明钠的熔点低的现象是______ 。
③能证明有氢氧化钠生成的现象是______ 。
(4)有乙同学为避免由于行动不够迅速产生偏差,又建议在集气瓶中再加入一定量煤油,其目的是______ 。
(5)①"84"消毒液在空气中的漂白原理用化学方程式表示_______
②漂白粉的制备化学方程式________
③"吹气“生火的化学方程式_________
④“滴水生火”的化学方程式_________

(1)钠与水反应的化学方程式为
(2)当进行适当操作时,还需要用到
(3)钠与水反应的现象很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
(4)有乙同学为避免由于行动不够迅速产生偏差,又建议在集气瓶中再加入一定量煤油,其目的是
(5)①"84"消毒液在空气中的漂白原理用化学方程式表示
②漂白粉的制备化学方程式
③"吹气“生火的化学方程式
④“滴水生火”的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属钠及其化合物在人类生产、生活中起着重要作用。
(1)Na的轨道表示式为_______ 。
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和 混合盐,制备金属Na,电解的化学方程式为:
混合盐,制备金属Na,电解的化学方程式为: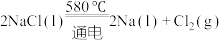 ,加入
,加入 的目的是
的目的是_______ 。
(3)采用空气和Na为原料可直接制备 。空气与熔融的金属Na反应前需依次通过的试剂为
。空气与熔融的金属Na反应前需依次通过的试剂为_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(4) 的电子式为
的电子式为_______ 。
在25℃和101kPa时,Na与 反应生成
反应生成 放出510.9kJ的热量,写出该反应的热化学方程式:
放出510.9kJ的热量,写出该反应的热化学方程式:_______ 。
(5)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生如下反应。
粉末,观察到溶液褪色,发生如下反应。

配平上述离子方程式_______ 。
该反应说明 具有
具有_______ (选填“氧化性”“还原性”或“漂白性”)。
(6)在密闭容器中,将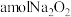 和bmol
和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为
固体混合物加热至250℃,充分反应后,若剩余固体为 和NaOH、排出气体为
和NaOH、排出气体为 和
和 时,
时,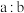 的取值范围为
的取值范围为_______ 。
(1)Na的轨道表示式为
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和
 混合盐,制备金属Na,电解的化学方程式为:
混合盐,制备金属Na,电解的化学方程式为: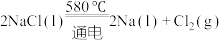 ,加入
,加入 的目的是
的目的是(3)采用空气和Na为原料可直接制备
 。空气与熔融的金属Na反应前需依次通过的试剂为
。空气与熔融的金属Na反应前需依次通过的试剂为a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(4)
 的电子式为
的电子式为在25℃和101kPa时,Na与
 反应生成
反应生成 放出510.9kJ的热量,写出该反应的热化学方程式:
放出510.9kJ的热量,写出该反应的热化学方程式:(5)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生如下反应。
粉末,观察到溶液褪色,发生如下反应。
配平上述离子方程式
该反应说明
 具有
具有(6)在密闭容器中,将
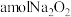 和bmol
和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为
固体混合物加热至250℃,充分反应后,若剩余固体为 和NaOH、排出气体为
和NaOH、排出气体为 和
和 时,
时,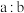 的取值范围为
的取值范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】填空。
(1)有以下几种物质:①空气;②液态氧;③硝酸钾溶液;④硫酸铜晶体(CuSO4·5H2O);⑤二氧化碳;⑥氧化铜;⑦金刚石;⑧甲烷;⑨氢氧化铜。其中:
属于纯净物的是_____________________________________ (填序号,下同);
属于混合物的是_____________________________________ ;
属于氧化物的是____________________________________ ;
属于盐的是___________________________________________ ;
属于有机物的是_________________________________________ ;
属于碱的是____________________________________________ ;
属于单质的是__________________________________________ 。
(2)金属钠着火,应用________________ 灭火;过氧化钠可做呼吸面具的供氧剂,有关化学方程式_____________________________________________________________________ ;除去NaHCO3溶液中的Na2CO3的有关化学方程式为____________________________________________________________________ ;
(3)我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb3O4可写成2PbO·PbO2,结合氧化物的分类可知PbO是碱性氧化物,而PbO2不是碱性氧化物。写出PbO (难溶于水)与盐酸反应的离子方程式__________________________________________________________________ ;已知PbO2与浓盐酸混合后可得到PbCl2、黄绿色气体等物质,请写出相应的化学方程式_____________________________________________________________________ 。
(1)有以下几种物质:①空气;②液态氧;③硝酸钾溶液;④硫酸铜晶体(CuSO4·5H2O);⑤二氧化碳;⑥氧化铜;⑦金刚石;⑧甲烷;⑨氢氧化铜。其中:
属于纯净物的是
属于混合物的是
属于氧化物的是
属于盐的是
属于有机物的是
属于碱的是
属于单质的是
(2)金属钠着火,应用
(3)我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb3O4可写成2PbO·PbO2,结合氧化物的分类可知PbO是碱性氧化物,而PbO2不是碱性氧化物。写出PbO (难溶于水)与盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】学习小组利用如下流程制备过氧化钠,并设计实验验证其相关性质。

回答下列问题:
(1)流程中由Na2O生成淡黄色固体的化学方程式为_______ 。
(2)小组同学取一定量淡黄色固体溶于冷水中。待固体全部反应后,仍可缓慢释放氧气,为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有_______ (填化学式),写出甲中发生反应的化学方程式_______ 。
②向乙中滴入酚酞,溶液变红的原因是_______ (用物质的电离方程式回答)。
(3)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为_______ (填化学式)。
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式_______ 。

回答下列问题:
(1)流程中由Na2O生成淡黄色固体的化学方程式为
(2)小组同学取一定量淡黄色固体溶于冷水中。待固体全部反应后,仍可缓慢释放氧气,为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有
②向乙中滴入酚酞,溶液变红的原因是
(3)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国著名化学家侯德榜发明的“联合制碱法”的反应原理用化学方程式可简要表示为:
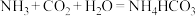 ,
,
 ;
;
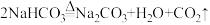 。
。
(1)纯碱属于___________ (填“酸”“碱”或“盐”)。
(2)检验碳酸氢钠中含有碳酸钠的方法是___________ 。
(3) ,请写出该反应能发生的原因
,请写出该反应能发生的原因_________ 。
(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:
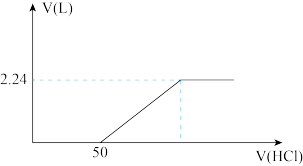
①逐滴滴加盐酸的过程中 物质的量变化趋势是
物质的量变化趋势是___________ ;
②上述混合溶液碳酸氢钠的物质的量是___________ 。
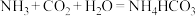 ,
, ;
;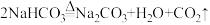 。
。(1)纯碱属于
(2)检验碳酸氢钠中含有碳酸钠的方法是
(3)
 ,请写出该反应能发生的原因
,请写出该反应能发生的原因(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:

①逐滴滴加盐酸的过程中
 物质的量变化趋势是
物质的量变化趋势是②上述混合溶液碳酸氢钠的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)以下物质中属于电解质的是(填序号):_______
A.硝酸钾固体B.纯醋酸C.胆矾(CuSO4∙5H2O)晶体D.熔融的BaCl2E.乙醇F.蔗糖G.氯气H.干冰I.铝J.漂白粉固体K.硫酸钾溶液L.氨水
(2)①向磁性的黑色金属氧化物中加入盐酸,写出发生的离子反应方程式:_______ ;再滴入几滴硫氰化钾溶液,溶液变红原因(用反应方程式表示)_______
②已知在坩埚中灼烧Fe(OH)3最后得到Fe2O3,写出灼烧Fe(OH)2最后得到的固体物质化学式:_______
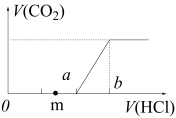
③向含等物质的量的Na2CO3和NaOH混合溶液中逐滴加入盐酸,加入盐酸体积和生成的气体关系如图,写出m点处发生的化学反应方程式_______
(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO 、Na+、CO
、Na+、CO 、H+、NO
、H+、NO 、HCO
、HCO 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是_______ 一定不存在的离子是_______ 。
(1)以下物质中属于电解质的是(填序号):
A.硝酸钾固体B.纯醋酸C.胆矾(CuSO4∙5H2O)晶体D.熔融的BaCl2E.乙醇F.蔗糖G.氯气H.干冰I.铝J.漂白粉固体K.硫酸钾溶液L.氨水
(2)①向磁性的黑色金属氧化物中加入盐酸,写出发生的离子反应方程式:
②已知在坩埚中灼烧Fe(OH)3最后得到Fe2O3,写出灼烧Fe(OH)2最后得到的固体物质化学式:
③向含等物质的量的Na2CO3和NaOH混合溶液中逐滴加入盐酸,加入盐酸体积和生成的气体关系如图,写出m点处发生的化学反应方程式

(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO
 、Na+、CO
、Na+、CO 、H+、NO
、H+、NO 、HCO
、HCO 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列反应的化学方程式或离子方程式:
⑴ 氯化铁溶液中加入铁粉
化学方程式:____________________________________
⑵碳酸氢钠溶液滴入盐酸中
离子方程式:________________________________________
⑶碳酸氢钠溶液和氢氧化钠溶液反应
化学方程式:________________________________________
⑷将二氧化碳通入炽热的炭层
化学方程式:________________________________________
⑴ 氯化铁溶液中加入铁粉
化学方程式:
⑵碳酸氢钠溶液滴入盐酸中
离子方程式:
⑶碳酸氢钠溶液和氢氧化钠溶液反应
化学方程式:
⑷将二氧化碳通入炽热的炭层
化学方程式:
您最近一年使用:0次





