I.某反应为:4CuI+Hg═Cu2HgI4+2Cu(反应前后的I均为﹣1价),试回答:
(1)上述反应产物Cu2HgI4中,Hg元素显___________ 价;
(2)CuI发生___________ 反应(填氧化或还原)。
II.某反应为:3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)反应中氧化剂是___________ (填化学式),被氧化的元素___________ (填元素符号);
(4)用单线桥表示出该反应中电子转移的方向和数目___________ 。
III.有下列三个反应:
a.2FeCl2+2KI═2FeCl2+2KCl+I2
b.2FeCl2+Cl2═2FeCl3
c.2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)上述三个反应中氧化剂氧化性强弱关系为___________ ;
(6)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是___________ 。
(1)上述反应产物Cu2HgI4中,Hg元素显
(2)CuI发生
II.某反应为:3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)反应中氧化剂是
(4)用单线桥表示出该反应中电子转移的方向和数目
III.有下列三个反应:
a.2FeCl2+2KI═2FeCl2+2KCl+I2
b.2FeCl2+Cl2═2FeCl3
c.2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)上述三个反应中氧化剂氧化性强弱关系为
(6)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是
更新时间:2016-12-09 11:10:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某反应体系有反应物和生成物共7种: 、
、 、
、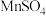 、
、 、
、 、
、 、
、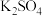 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: ,试回答下列问题:
,试回答下列问题:
(1)该反应中的还原剂是_______ 。
(2)该反应中,发生还原反应的过程是_______ →_______ 。
(3)写出该反应的化学方程式并配平,并用单线桥法标出电子转移的方向和数目_______ 。
 、
、 、
、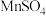 、
、 、
、 、
、 、
、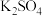 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: ,试回答下列问题:
,试回答下列问题:(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式并配平,并用单线桥法标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列问题:
(1)下列物质属于化合物但不属于电解质的是____ (填标号)。
(2)工业上制取金刚砂的反应为SiO2+3C SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为____ 。
(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是____ (填元素符号)。
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式____ 。
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为_____ 。
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为____ 。
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为____ 。
(1)下列物质属于化合物但不属于电解质的是
| A.石墨 | B.CO2 | C.NH3·H2O | D.CaCO3 |
 SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为
您最近一年使用:0次
【推荐3】中国传统文化是人类文明的瑰宝,古代文献中记载了大量古代化学的研究成果。回答下面问题:
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为______________ 。
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C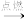 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是_________ ,反应转移4mol电子时,被S氧化的C有____________ mol。
(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式_____________________________________________________ 。
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C
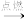 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应是重要的化学反应,在人类的生产和生活中无处不在。
(1)已知反应:BaSO4+C——BaS+CO↑
①配平该反应___ 。
②若有2.33gBaSO4发生反应,则反应过程中转移电子的数目是__ ,标准状况下,生成一氧化碳___ L。
(2)已知反应:Cu+HNO3(稀)——Cu(NO3)2+NO↑+H2O;
①配平并用“双线桥法”表示上述反应中电子转移的方向和数目___ 。
②该反应中氧化剂与还原剂的物质的量之比为__ ;写出该反应的离子方程式__ 。
(1)已知反应:BaSO4+C——BaS+CO↑
①配平该反应
②若有2.33gBaSO4发生反应,则反应过程中转移电子的数目是
(2)已知反应:Cu+HNO3(稀)——Cu(NO3)2+NO↑+H2O;
①配平并用“双线桥法”表示上述反应中电子转移的方向和数目
②该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)工业上常以氨气为原料制备硝酸,其中有一步非常重要的反应为
4NH3+5O2 4NO+6H2O,该反应的氧化剂为
4NO+6H2O,该反应的氧化剂为______ ,还原剂为______ 。用单线桥法表示该氧化还原反应电子转移的方向和数目____________________________________ 。
若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为__________________ (写出含n、V的表达式)。
(2)某一反应体系中有反应物和生成物共5种物质:S、 H2S、HNO3、NO、H2O。已知硝酸是一种反应物,该反应中还原产物是________ ;若反应中转移了0.3mol电子,则氧化产物的质量是_____ g。
(3)按要求填空:
①除去碳酸氢钠溶液中的碳酸钠______________________ (用离子方程式表示原理);
②除去碳酸钠溶液中的碳酸氢钠,应加试剂为________________ ;
③用氢氧化钡除去明矾溶液中的硫酸根__________________ (用离子方程式表示原理)。
4NH3+5O2
 4NO+6H2O,该反应的氧化剂为
4NO+6H2O,该反应的氧化剂为若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为
(2)某一反应体系中有反应物和生成物共5种物质:S、 H2S、HNO3、NO、H2O。已知硝酸是一种反应物,该反应中还原产物是
(3)按要求填空:
①除去碳酸氢钠溶液中的碳酸钠
②除去碳酸钠溶液中的碳酸氢钠,应加试剂为
③用氢氧化钡除去明矾溶液中的硫酸根
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
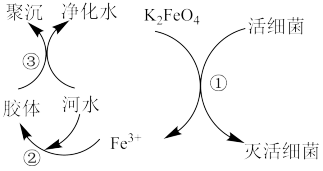
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性,该过程的还原产物是_______ (填离子符号);过程③属于_______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有_______ (填两个)。
(4)制备高铁酸钾常用的反应原理为 (反应未配平)。
(反应未配平)。
①该反应中,Cl元素的化合价由_______ 价变为_______ 价;通过该反应说明:在碱性条件下,氧化性
_______ (填“>”、“=”或“<”) 。
。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ ,将该反应改写为离子方程式:_______ 。
 ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
 (反应未配平)。
(反应未配平)。①该反应中,Cl元素的化合价由

 。
。②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
______ SiO2+_______ C+______ N2
_______ Si3N4+_____ CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是___________ 。
(3)分析反应可推测碳、氮气的氧化性:C________ N2(填“>”“<”“=”)。
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途

根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是
(3)分析反应可推测碳、氮气的氧化性:C
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2 SO42-+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是__________ ,还原剂是___________ ,反应中被还原的元素是________ 。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________________________________________________________ 。
(3)用双线桥法标出反应②电子转移的方向和数目:_____________________________________ 。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O
配平上述反应的化学方程式。________________________ 。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2 SO42-+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是
(3)用双线桥法标出反应②电子转移的方向和数目:
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O
配平上述反应的化学方程式。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.有下列三个在溶液中发生的氧化还原反应:
①
②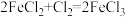
③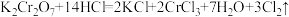
请根据上述反应分析推断后回答下列问题:
(1) 的氧化性由强到弱依次是
的氧化性由强到弱依次是_______ 。
(2) 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?_______ (填“能”或“不能”),理由是_______ 。
Ⅱ. 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: 。
。
(3)反应中_______ 元素被氧化(填元素名称),_______ 是氧化剂(填化学式);
(4)用单线桥标出电子转移方向和数目:_______ 。
(5) 表现的性质是
表现的性质是_______ 。
(6)某厂废液中,含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是_______。
的是_______。
①

②
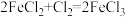
③
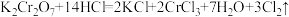
请根据上述反应分析推断后回答下列问题:
(1)
 的氧化性由强到弱依次是
的氧化性由强到弱依次是(2)
 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?Ⅱ.
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: 。
。(3)反应中
(4)用单线桥标出电子转移方向和数目:
(5)
 表现的性质是
表现的性质是(6)某厂废液中,含有2%~5%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是_______。
的是_______。A. | B. | C.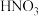 | D.浓 |
您最近一年使用:0次



