补齐物质与其用途的连线,并回答问题。
(1)补齐连线_______ 。
(2) 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:_______ 。
(3)上述 的用途,利用了它的
的用途,利用了它的_______ (填“物理”或“化学”)性质。
(4)上述制取漂白粉的化学方程式是_______ 。
用途 物质 A.去除某些有机溶剂中的水分——————a.  B.84消毒液的有效成分 b.  C.厨房中的食用碱 c.  D.作供氧剂 d.  E.与消石灰反应制取漂白粉 e.  |
(2)
 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:(3)上述
 的用途,利用了它的
的用途,利用了它的(4)上述制取漂白粉的化学方程式是
更新时间:2023-12-26 15:11:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: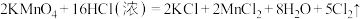 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: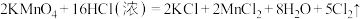 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为_______ ;漂白粉的有效成分是(填化学式)_______ ;漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_______ 。
(2)除去NaHCO3溶液中混有少量的Na2CO3,选用试剂_______ ,化学方程式_______ 。
(3)除去CO2气体中混有少量的HCl,选用试剂_______ ,化学方程式_______ 。
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为
(2)除去NaHCO3溶液中混有少量的Na2CO3,选用试剂
(3)除去CO2气体中混有少量的HCl,选用试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列各题:
(1)实验室保存FeCl2溶液时,为防止被氧化,需加入___________ 。
(2)消毒液(含NaClO)与洁厕剂(含HCl)不能混用,否则会生成有毒的Cl2,请写出反应的离子方程式___________ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,请写出反应的化学方程式___________ 。
(4)用双线桥法表示该反应电子转移的方向和数目: 2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑___________ 。
(5)依据化合价升降守恒配平化学方程式:__________
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
(1)实验室保存FeCl2溶液时,为防止被氧化,需加入
(2)消毒液(含NaClO)与洁厕剂(含HCl)不能混用,否则会生成有毒的Cl2,请写出反应的离子方程式
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,请写出反应的化学方程式
(4)用双线桥法表示该反应电子转移的方向和数目:
 2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑(5)依据化合价升降守恒配平化学方程式:
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列化学用语:
(1)书写电离方程式: NaClO:__________ ,一水合氨:__________ 。
(2)某金属氯化物MCl240.5g含有0.6mlCl-,MCl2的摩尔质量__________ 。
(3)工业上用电解饱和食盐水制Cl2,写出该反应的化学方程式:__________
(4)小块钠投入到水中,写出该反应的化学方程式:__________
(5)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请指出此反应中还原剂为__________ (化学式)。
(6)相同温度和体积的A和B两容器,A容器中充满O2,B容器中充满O3,若密度相同,则氧气和臭氧的物质的量之比为:__________
(1)书写电离方程式: NaClO:
(2)某金属氯化物MCl240.5g含有0.6mlCl-,MCl2的摩尔质量
(3)工业上用电解饱和食盐水制Cl2,写出该反应的化学方程式:
(4)小块钠投入到水中,写出该反应的化学方程式:
(5)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请指出此反应中还原剂为
(6)相同温度和体积的A和B两容器,A容器中充满O2,B容器中充满O3,若密度相同,则氧气和臭氧的物质的量之比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以下是依据一定的分类标准对某些物质与水反应的情况进行分类的分类图。请根据你所学的知识,按要求填空。

(1)上述第一次分类的依据是________________________________________ 。
(2)C组中的某一物质在常温下能与冷水反应,写出该反应的化学方程式:__________________________________________________________________ 。
(3)任选D组中的一种物质,写出1点其重要用途_____________________________________________________________ 。
(4)F组物质中某一物质的水溶液呈弱碱性,原因是________________ (用电离方程式表示)。
(5)D组中某一物质与E组中某一物质在水中发生反应生成两种强酸,写出该反应的化学方程式:________________________________________________________________ 。

(1)上述第一次分类的依据是
(2)C组中的某一物质在常温下能与冷水反应,写出该反应的化学方程式:
(3)任选D组中的一种物质,写出1点其重要用途
(4)F组物质中某一物质的水溶液呈弱碱性,原因是
(5)D组中某一物质与E组中某一物质在水中发生反应生成两种强酸,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
I.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与实验结论匹配:___________ 。
(2)写出钠与水反应的化学方程式___________ 。
II.钠与氧气的反应
(3)钠与氧气反应的产物有多种,其中产物___________ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式___________ 。
III.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(4)下列关于Na2CO3的认识正确的是___________ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(5)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,若面团发得不好,面团内的气孔少,不够膨松。需添加___________ (填“Na2CO3”或“NaHCO3”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其产气原理___________ 。
I.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与实验结论匹配:
| 实验现象 实验结论 A.钠浮在水面上 a.有碱性物质生产生成 B.钠四处游动 b.有气体产生 C.溶液变红 c.反应放热,钠熔点低 D.钠熔成光亮的小球 d.钠的密度比水小 |
II.钠与氧气的反应
(3)钠与氧气反应的产物有多种,其中产物
III.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(4)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(5)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,若面团发得不好,面团内的气孔少,不够膨松。需添加
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融) 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是____ 。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是____ 。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应的化学方程式____________ ,生成物的颜色为____ 。将该试管冷却后直立,滴加几滴水(如图Ⅱ所示),发生反应的化学方程式为____________ ,检验该反应产生的气体的方法是________________ 。
 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:(1)下列各项中属于保存金属钠的正确方法是
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应的化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】mgCH4与ng甲酸(HCOOH)在足量的O2中燃烧,将其产物通过足量的Na2O2充反应,则Na2O2增重多少克___ ?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有以下物质:①钠;② ;③NaOH;④
;③NaOH;④ ;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
(1)以上物质中属于电解质的是
(2)以下两种物质溶于水,书写出相应的电离方程式。
 :
:
次氯酸钙:
(3)①与⑧反应,书写出该反应的总的离子方程式
(4)②与⑩反应,书写出相应的化学方程式
(5)④与少量的⑨反应,书写出相应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某化学兴趣小组对钠及其化合物进行了深度探究。
Ⅰ.“钠在空气中燃烧”实验深度探究
(1)Na在空气中燃烧主要产物是___________ (填化学式)。
(2)钠在空气中燃烧后生成的固体粉末中还含有黑色固体物质。通过查阅文献发现,有一种观点认为该黑色固体物质是C和铁的氧化物。
ⅰ.生成C的原因是CO2和Na在加热条件发生如下反应,请配平该化学方程式,并用单线桥表示出电子转移的方向和数目:___________
___________CO2+___________Na=___________ Na2CO3+___________C
ⅱ.产生铁的氧化物的原因是Na单质中含有0.002%左右的铁元素,在钠燃烧的时候铁被氧化为铁的氧化物。为了检验黑色固体物质中是否含有铁元素,进行了如下实验:
Ⅱ.“纯碱和小苏打”性质实验的深度探究
该组同学利用下图对“碳酸钠溶液与盐酸反应”进行探究

(3)导管P的作用是___________ 。
(4)开始实验;
ⅰ.广口瓶中预先盛放10 mL 1 mol/L的Na2CO3溶液,将分液漏斗中10 mL 1 mol/L的HCl溶液缓缓滴入到广口瓶中,观察到的现象是___________ ,在分液漏斗再加10 mL 1 mol/L的HCl溶液并滴入广口瓶,发生反应的离子方程式为___________ 。
ⅱ.广口瓶中预先盛放10 mL 1 mol/L的HCl溶液,将分液漏斗中的10 mL 1 mol/L Na2CO3溶液中的5 mL溶液快速滴入到广口瓶中,立刻有大量气泡产生,气球膨胀。再将剩余的5 mL 1 mol/L的Na2CO3溶液加入到广口瓶中,几分钟后,气球变扁,变扁的原因是___________ (用化学方程式作答)。
(5)实验结论:
a.Na2CO3与盐酸反应是分步进行的;
b.碳酸钠和碳酸氢钠在一定条件下可以相互转化;
c. 和
和 中结合H+能力较强的是
中结合H+能力较强的是___________ (填离子符号)。
Ⅰ.“钠在空气中燃烧”实验深度探究
(1)Na在空气中燃烧主要产物是
(2)钠在空气中燃烧后生成的固体粉末中还含有黑色固体物质。通过查阅文献发现,有一种观点认为该黑色固体物质是C和铁的氧化物。
ⅰ.生成C的原因是CO2和Na在加热条件发生如下反应,请配平该化学方程式,并用单线桥表示出电子转移的方向和数目:
___________CO2+___________Na=___________ Na2CO3+___________C
ⅱ.产生铁的氧化物的原因是Na单质中含有0.002%左右的铁元素,在钠燃烧的时候铁被氧化为铁的氧化物。为了检验黑色固体物质中是否含有铁元素,进行了如下实验:
| 实验内容 | 实验现象 | 实验结论 |
| ①收集黑色固体物质溶于稀硫酸中 | 少量黑色固体物质不溶解 | |
| ②取上层清液少许于一支试管中,滴入KSCN溶液 | 溶液变为红色 |
Ⅱ.“纯碱和小苏打”性质实验的深度探究
该组同学利用下图对“碳酸钠溶液与盐酸反应”进行探究

(3)导管P的作用是
(4)开始实验;
ⅰ.广口瓶中预先盛放10 mL 1 mol/L的Na2CO3溶液,将分液漏斗中10 mL 1 mol/L的HCl溶液缓缓滴入到广口瓶中,观察到的现象是
ⅱ.广口瓶中预先盛放10 mL 1 mol/L的HCl溶液,将分液漏斗中的10 mL 1 mol/L Na2CO3溶液中的5 mL溶液快速滴入到广口瓶中,立刻有大量气泡产生,气球膨胀。再将剩余的5 mL 1 mol/L的Na2CO3溶液加入到广口瓶中,几分钟后,气球变扁,变扁的原因是
(5)实验结论:
a.Na2CO3与盐酸反应是分步进行的;
b.碳酸钠和碳酸氢钠在一定条件下可以相互转化;
c.
 和
和 中结合H+能力较强的是
中结合H+能力较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的制备是化学学科的基本研究方向。
(1)室温下,将氨水和 溶液混合,可制得
溶液混合,可制得 溶液。
溶液。
①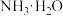 属于
属于___________ (填“电解质”或“非电解质”), 在水中的电离方程式为
在水中的电离方程式为___________ 。
②制得 溶液的化学方程式为
溶液的化学方程式为___________ 。
(2)用 溶液(溶液显碱性)和
溶液(溶液显碱性)和 溶液发生复分解反应制备
溶液发生复分解反应制备 ,在烧杯中制备
,在烧杯中制备 沉淀时,应选用的加料方式是
沉淀时,应选用的加料方式是___________ (填字母),原因是避免生成___________ 沉淀(填物质的化学式)。
A.将 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中
B.将 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中
(3)软锰矿(主要成分 )的水悬浊液可吸收烟气中
)的水悬浊液可吸收烟气中 并同时制备
并同时制备 。
。
①制备 反应的化学方程式为
反应的化学方程式为___________ 。
②质量为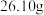 纯净
纯净 最多能吸收
最多能吸收___________  (标准状况)
(标准状况) 。
。
(1)室温下,将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液。
溶液。①
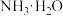 属于
属于 在水中的电离方程式为
在水中的电离方程式为②制得
 溶液的化学方程式为
溶液的化学方程式为(2)用
 溶液(溶液显碱性)和
溶液(溶液显碱性)和 溶液发生复分解反应制备
溶液发生复分解反应制备 ,在烧杯中制备
,在烧杯中制备 沉淀时,应选用的加料方式是
沉淀时,应选用的加料方式是A.将
 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中B.将
 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中(3)软锰矿(主要成分
 )的水悬浊液可吸收烟气中
)的水悬浊液可吸收烟气中 并同时制备
并同时制备 。
。①制备
 反应的化学方程式为
反应的化学方程式为②质量为
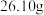 纯净
纯净 最多能吸收
最多能吸收 (标准状况)
(标准状况) 。
。
您最近一年使用:0次



