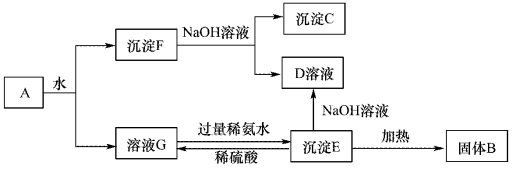
除去下列物质中所含杂质(括号内为杂质),写出除去杂质的化学方程式。
(1)Fe2O3[Fe(OH)3]_______ ;
(2)Fe2O3(Al2O3)_______
(3)Fe(Al)_______
(4)Na2CO3(NaHCO3)_______
(1)Fe2O3[Fe(OH)3]
(2)Fe2O3(Al2O3)
(3)Fe(Al)
(4)Na2CO3(NaHCO3)
更新时间:2022-12-11 22:06:02
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求填空
(1)检验SO42-所需要用的试剂_______________________________ 。
(2)三硅酸镁(Mg2Si3O8·11H2O)用氧化物表示_______________________ 。
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为_________________ 。
(4)用氨气检验氯气泄漏的方程式:_______________ 。
(5)请配平以下化学方程式:
____ Al+____ NaNO3+____ NaOH= ____ NaAlO2+____ N2↑+___ H2O
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_________ L。
(1)检验SO42-所需要用的试剂
(2)三硅酸镁(Mg2Si3O8·11H2O)用氧化物表示
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为
(4)用氨气检验氯气泄漏的方程式:
(5)请配平以下化学方程式:
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.现有一定量含有Na2O杂质的Na2O2试样,用如下图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量。可供选用的反应物:CaCO3固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题。

(1)装置A中反应的离子方程式为___________ 。
(2)写出装置D中反应生成O2的化学方程式,并用双线桥法表示其电子的转移___________ 。
(3)装置E中碱石灰的作用是___________ 。
Ⅱ.纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠,再加热碳酸氢钠即可制得纯碱,查阅资料知:NH3极易溶于水,溶于水呈碱性。部分工艺流程如图1所示。

(4)纯碱属于___________ (填“酸”、“碱”或“盐”)。
(5)为了提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为___________ (选填字母编号)
A.先通CO2再通NH3 B.先通NH3再通CO2
图2中导管b通入___________ (填“NH3”或“CO2”),导管a不能插入液面以下的原因是___________ ,装置c中的试剂为___________ (选填字母编号)。

A.碱石灰 B.浓硫酸 C.五氧化二磷

(1)装置A中反应的离子方程式为
(2)写出装置D中反应生成O2的化学方程式,并用双线桥法表示其电子的转移
(3)装置E中碱石灰的作用是
Ⅱ.纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠,再加热碳酸氢钠即可制得纯碱,查阅资料知:NH3极易溶于水,溶于水呈碱性。部分工艺流程如图1所示。

(4)纯碱属于
(5)为了提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为
A.先通CO2再通NH3 B.先通NH3再通CO2
图2中导管b通入

A.碱石灰 B.浓硫酸 C.五氧化二磷
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答:
(1) 的电子式是
的电子式是______ ;异戊烷的结构简式是______ 。
(2)Al溶于氢氧化钠溶液的离子方程式是______ 。
(3)用1.00mol/LNaCl溶液配制100mL0.50mol/LNaCl溶液,需用______ (填仪器名称)量取______ mL1.00mol/LNaCl溶液。
(1)
 的电子式是
的电子式是(2)Al溶于氢氧化钠溶液的离子方程式是
(3)用1.00mol/LNaCl溶液配制100mL0.50mol/LNaCl溶液,需用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。相互间能发生反应的是___________ 。(填序号)
(2)检验Na2O2其组成中所含阳离子的方法是___________ 。
(3)FeSO4·7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因___________ 。
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。相互间能发生反应的是
(2)检验Na2O2其组成中所含阳离子的方法是
(3)FeSO4·7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铝是一种重要金属:
(1)生产中曾用铝热反应(铝与铁的氧化物反应生成氧化铝和铁)焊接钢轨,则铝与磁性氧化铁发生反应的化学方程式为________________________ 。该反应中氧化剂是_______ ,还原剂是______ ,要得到1mol金属铁,需要铝的质量_____ g。
(2) 铝与NaOH溶液反应的离子方程式为:_________________ 。在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为___ 。
(1)生产中曾用铝热反应(铝与铁的氧化物反应生成氧化铝和铁)焊接钢轨,则铝与磁性氧化铁发生反应的化学方程式为
(2) 铝与NaOH溶液反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有甲、乙和丙三种化合物,关于它们的信息如下表。
(1)甲的化学式为___________ ,它与H2O的反应中,氧化剂和还原剂的物质的量之比是______________ ,若生成的气体在标况下的体积为2.24L,则反应中转移的电子的物质的量为_________
(2)乙的化学式为___________ ,乙溶液中滴加少量 Ba(OH)2也可生成沉淀M,对应的离子方程式为____________________________ 。
(3)丙属于_____________ 。
A.两性氧化物 B.酸式盐 C.非电解质 D.两性氢氧化物
丙溶于化合物甲与H2O反应后的溶液的离子反应方程式为___________________________ 。
| 甲 | 焰色呈黄色,能与H2O剧烈反应产生能使带火星的木条复燃的气体,反应后的溶液遇酚酞变红。 |
| 乙 | 是与小苏打同类的盐,焰色呈紫色(透过蓝色钴玻璃),溶于H2O后溶液呈强酸性,往所得溶液中滴加BaCl2溶液可生成不溶于稀硝酸的白色沉淀M。 |
| 丙 | 属于高熔点物质,常温和高温下都稳定,能够溶解在化合物甲与H2O反应后的溶液中,也能溶解在化合物乙的溶液中;其所含的金属元素在地壳中含量仅次于氧、硅 |
(1)甲的化学式为
(2)乙的化学式为
(3)丙属于
A.两性氧化物 B.酸式盐 C.非电解质 D.两性氢氧化物
丙溶于化合物甲与H2O反应后的溶液的离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铝硅合金材料性能优良。铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:

(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中的金属阳离子有_______ 。
(2)焙烧除铁反应:4(NH4)2SO4 + Fe2O3 2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为______ 。指出气体Ⅰ的用途__________________ (任写一种)。

(3)操作①包括:加水溶解、_______ 。若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为____________________ 。
(4)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3,任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式______________ 。

(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中的金属阳离子有
(2)焙烧除铁反应:4(NH4)2SO4 + Fe2O3
 2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
(3)操作①包括:加水溶解、
(4)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3,任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失.
(1)写出该反应的离子方程式_________________ ,其中钠熔成闪亮小球的原因是__________
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式_____________
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式_________ ;继续将沉淀过滤、洗涤、干燥、灼烧,此时得到的固体为_________ (填化学式)。
(1)写出该反应的离子方程式
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题
(1)CuSO4溶液中含有少量的Fe3+,除杂的方式是加入适当物质调整溶液至pH=3.5,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的___________
(2)常温下,Fe(OH)3的溶度积Ksp=10-38 , Cu(OH)2的溶度积Ksp=3.0×10-20 ,通常认为残留在溶液中的离子浓度小于1×10-5 mol/L时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol/L,则Cu(OH)2开始沉淀时溶液的pH为________ ,Fe3+完全沉淀时溶液的pH为________ ,通过计算确定(1)中的方案________ (填“可行”或“不可行”)。
(1)CuSO4溶液中含有少量的Fe3+,除杂的方式是加入适当物质调整溶液至pH=3.5,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
| A.CuO | B.NH3·H2O | C.NaOH | D.Cu(OH)2 |
您最近一年使用:0次