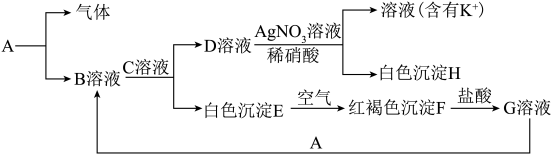
已知存在以下物质之间的相互转化,分别写出下列物质的化学式:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 、F_______ 、G_______ 、H_______ ,并写出每步转化反应的离子方程式_______ 。

更新时间:2022-11-26 09:19:38
|
相似题推荐
【推荐1】I.化学反应按照不同的分类方法,可以分为化合反应,分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。现有下列反应:
①CO2+C 2CO
2CO
②Cu2(OH)2CO3 2Cu+H2O+CO2↑
2Cu+H2O+CO2↑
③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2 2CO2
2CO2
⑤3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑥CuO+CO Cu+CO2
Cu+CO2
⑦2H2O H2↑+O2↑
H2↑+O2↑
⑧CO2+H2O=H2CO3
(1)其中属于化合反应的是___________ (填序号,下同),属于置换反应的是___________ 。
(2)属于氧化还原反应的是___________ 。
Ⅱ.回答下列问题
(3)反应Fe2O3+2Al=Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨。在该反应中___________ (填元素符号)元素的化合价升高,被___________ 。该反应中,___________ (填分子式,下同)是氧化剂,___________ 是氧化产物,___________ 是还原剂,___________ 是还原产物。
(4)写出CuO与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目:___________ 。
①CO2+C
 2CO
2CO ②Cu2(OH)2CO3
 2Cu+H2O+CO2↑
2Cu+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2
 2CO2
2CO2⑤3Fe+4H2O
 Fe3O4+4H2
Fe3O4+4H2 ⑥CuO+CO
 Cu+CO2
Cu+CO2⑦2H2O
 H2↑+O2↑
H2↑+O2↑ ⑧CO2+H2O=H2CO3
(1)其中属于化合反应的是
(2)属于氧化还原反应的是
Ⅱ.回答下列问题
(3)反应Fe2O3+2Al=Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨。在该反应中
(4)写出CuO与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.甘肃马家密遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→∙∙∙∙∙∙→铜”的转化。
,“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→∙∙∙∙∙∙→铜”的转化。
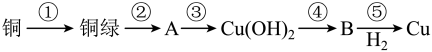
(1)从物质分类标准看,“铜绿”属于___________(填字母)。
(2)上述转化过程中属于置换反应的是___________ (填序号)
(3)请写出铜绿与盐酸反应的化学方程式:___________ 。
Ⅱ.胶体是一种常见的分散系,回答下列问题。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾,向沸水中滴入几滴FeCl3饱和溶液,继续煮沸直至液体呈红褐色,可制得 胶体。写出生成
胶体。写出生成 胶体的化学方程式:
胶体的化学方程式:___________ 。
(5)常用于区分溶液和胶体的方法是___________ 。
III.已知: 。据此回答下列问题:
。据此回答下列问题:
(6)H3PO2中磷元素的化合价是___________ 。
(7)H3PO2属于___________ (选填“一”、“二”或“三”)元酸。NaH2PO2属于___________ (选填“正盐”或“酸式盐”)。
 ,“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→∙∙∙∙∙∙→铜”的转化。
,“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→∙∙∙∙∙∙→铜”的转化。
(1)从物质分类标准看,“铜绿”属于___________(填字母)。
| A.氧化物 | B.酸 | C.碱 | D.盐 |
(2)上述转化过程中属于置换反应的是
(3)请写出铜绿与盐酸反应的化学方程式:
Ⅱ.胶体是一种常见的分散系,回答下列问题。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾,向沸水中滴入几滴FeCl3饱和溶液,继续煮沸直至液体呈红褐色,可制得
 胶体。写出生成
胶体。写出生成 胶体的化学方程式:
胶体的化学方程式:(5)常用于区分溶液和胶体的方法是
III.已知:
 。据此回答下列问题:
。据此回答下列问题:(6)H3PO2中磷元素的化合价是
(7)H3PO2属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.物质的分类是学习化学的一种重要方法,有下列几种物质:①盐酸;② ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:
(1)属于碱性氧化物的是_______ (填序号),属于盐类的是_______ (填序号)。
(2)写出⑦在熔融状态下的电离方程式:_______ 。
(3)写出少量③和④反应的离子方程式:_______ 。
Ⅱ.有以下四个反应:①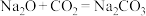 ;②
;② ;③
;③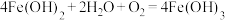 ;④
;④ 。
。
(4)属于复分解反应的是_______ (填序号,下同),既是化合反应又是氧化还原反应的是_______ 。
Ⅲ.单质到盐的转化关系可表示为:A(单质) B(氧化物)
B(氧化物) C
C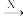 D(盐)。
D(盐)。
(5)若A是碳单质,则C的水溶液呈_______ (填“酸”“碱”或“中”)性。
(6)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是_______ (举一例),D的化学式可能是_______ 。
 ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:(1)属于碱性氧化物的是
(2)写出⑦在熔融状态下的电离方程式:
(3)写出少量③和④反应的离子方程式:
Ⅱ.有以下四个反应:①
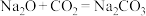 ;②
;② ;③
;③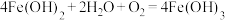 ;④
;④ 。
。(4)属于复分解反应的是
Ⅲ.单质到盐的转化关系可表示为:A(单质)
 B(氧化物)
B(氧化物) C
C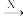 D(盐)。
D(盐)。(5)若A是碳单质,则C的水溶液呈
(6)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】写出符合下列情况的离子方程式。
(1)向 溶液中加入
溶液中加入 溶液生成
溶液生成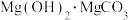 和
和 :
:_____________________ 。
(2)BaS溶液与硫酸锌溶液混合生成立德粉( ):
):_________________________________________ 。
(3)向 溶液中加入
溶液中加入 生成
生成 :
:______________ 。
(4)已知 不溶于水,但可溶于醋酸铵溶液,反应方程式如下:
不溶于水,但可溶于醋酸铵溶液,反应方程式如下: ,将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:
,将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:_________________________ 。
(5)新制的氯水加到 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:
_____________________ 。
(6) 能与热的经硫酸酸化的
能与热的经硫酸酸化的 溶液反应,生成
溶液反应,生成 和
和 ,该反应的离子方程式:
,该反应的离子方程式:
____________________________ 。
(1)向
 溶液中加入
溶液中加入 溶液生成
溶液生成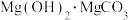 和
和 :
:(2)BaS溶液与硫酸锌溶液混合生成立德粉(
 ):
):(3)向
 溶液中加入
溶液中加入 生成
生成 :
:(4)已知
 不溶于水,但可溶于醋酸铵溶液,反应方程式如下:
不溶于水,但可溶于醋酸铵溶液,反应方程式如下: ,将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:
,将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:(5)新制的氯水加到
 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:(6)
 能与热的经硫酸酸化的
能与热的经硫酸酸化的 溶液反应,生成
溶液反应,生成 和
和 ,该反应的离子方程式:
,该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.SO2在工农业生产中有着重要的应用,请回答下列问题:
(1)工业上用软锰矿(主要成分为MnO2)制备Mn(H2PO4)2•2H2O。常用稀硫酸酸浸软锰矿,同时通入SO2,此时发生反应的离子方程式为_____ ,SO2作_____ (填“氧化剂”或“还原剂”)。
Ⅱ.一定温度下,向容积为2L的恒容密闭容器中通入2molSO2和1molO2,在一定条件下发生反应2SO2(g)+O2(g) 2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
(2)下列说法能够判断上述反应达到化学平衡状态的是_____ (填标号)。
(3)上述反应体系的正反应速率和逆反应速率相等的时间段是_____ (填“0~4”、“4~8”、“8~12”“12~18”或“18~25”)min。
(4)0~8min内,用SO3表示该反应的平均速率为_____ mol•L-1•min-1,12min时,SO2的转化率为_____ 。
(5)若起始时容器内压强为p0MPa,则平衡时,容器内压强约为_____ (用含p0的代数式表示,保留2位有效数字)MPa。
(1)工业上用软锰矿(主要成分为MnO2)制备Mn(H2PO4)2•2H2O。常用稀硫酸酸浸软锰矿,同时通入SO2,此时发生反应的离子方程式为
Ⅱ.一定温度下,向容积为2L的恒容密闭容器中通入2molSO2和1molO2,在一定条件下发生反应2SO2(g)+O2(g)
 2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:| 时间/min | 4 | 8 | 12 | 18 | 25 |
| n(O2)/mol | 0.70 | 0.50 | 0.40 | 0.32 | 0.32 |
| A.v(SO2)=2v(O2) | B.容器内气体的平均摩尔质量不再发生变化 |
| C.SO2和O2的浓度之比为2:1 | D.SO3的百分含量不再发生变化 |
(4)0~8min内,用SO3表示该反应的平均速率为
(5)若起始时容器内压强为p0MPa,则平衡时,容器内压强约为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】常温下,液体A是一种橙色液体,是橡胶硫化的重要试剂。A仅含两种短周期元素,且分子内原子均满足8电子稳定结构。气体C能使品红褪色,溶液B呈酸性。常温下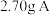 和水反应如图所示:
和水反应如图所示:
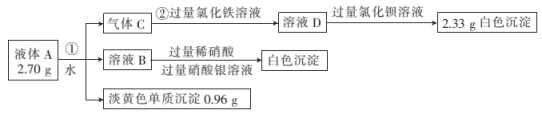
(1)写出A中所含元素的名称:_______ ,A的电子式为_______ 。
(2)写出第①步反应的化学方程式:_______ 。
(3)写出第②步的离子方程式:_______ 。
(4)将气体C通入装有适量品红溶液的试管中,溶液褪色。在该试管口套上气球,将无色溶液加热至恢复红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因:_______ 。
 和水反应如图所示:
和水反应如图所示:
(1)写出A中所含元素的名称:
(2)写出第①步反应的化学方程式:
(3)写出第②步的离子方程式:
(4)将气体C通入装有适量品红溶液的试管中,溶液褪色。在该试管口套上气球,将无色溶液加热至恢复红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2=2Al(OH)3↓ +Na2CO3+H2O
(1)上述五中物质中沸点最低物质的结构式为______________ ,由上述物质中的两种元素按原子个数比1:1形成的离子化合物的电子式为__________________ (写一例)
(2)Al元素的单质有许多不同于其他金属的特性,请列举2例(也可以用化学方程式表示)
______________________ 、__________________________________ .
(3)氢有3种稳定同位素,H氕、D氘、T氚,分别为丰度a、b、c,则计算氢元素的近似相对原子质量的表达式为______________________________________________ .
甲认为H可以排在周期表ⅠA族,也可以排在ⅦA族;而乙同学认为H也可以与碳一样,排在ⅣA族,乙同学的理由是__________________________________________________ 。
(4)已知通入二氧化碳336 L(标准状况下),理论上生成Al(OH)3________________ mol,
实际上生成24 mol Al(OH)3和15 mol Na2CO3,Al(OH)3比理论上要少的原因是:________________________________________________________ .
(1)上述五中物质中沸点最低物质的结构式为
(2)Al元素的单质有许多不同于其他金属的特性,请列举2例(也可以用化学方程式表示)
(3)氢有3种稳定同位素,H氕、D氘、T氚,分别为丰度a、b、c,则计算氢元素的近似相对原子质量的表达式为
甲认为H可以排在周期表ⅠA族,也可以排在ⅦA族;而乙同学认为H也可以与碳一样,排在ⅣA族,乙同学的理由是
(4)已知通入二氧化碳336 L(标准状况下),理论上生成Al(OH)3
实际上生成24 mol Al(OH)3和15 mol Na2CO3,Al(OH)3比理论上要少的原因是:
您最近一年使用:0次
填空题
|
适中
(0.64)
真题
【推荐3】图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁:E是不溶于水的酸性氧化物,能与氢氟酸反应。
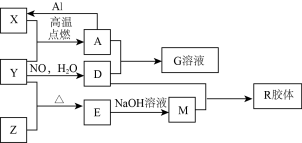
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是_____________________ ;M中存在的化学键类型为_________________ ;R的化学式是_______________________ 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为________________ 。
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体)。放出a kJ热量。写出该反应的热化学方程式:_______________________________________ 。
(4)写出A和D的稀溶液反应生成G的离子方程式:_______________________ 。
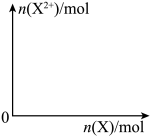
(5)问含4 mol D的稀溶液中,逐渐加入X3粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2-)随n(X)变化的示意图,并标出n(X2-)的最大值_________ 。

回答下列问题:
(1)组成单质Y的元素在周期表中的位置是
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体)。放出a kJ热量。写出该反应的热化学方程式:
(4)写出A和D的稀溶液反应生成G的离子方程式:
(5)问含4 mol D的稀溶液中,逐渐加入X3粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2-)随n(X)变化的示意图,并标出n(X2-)的最大值

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
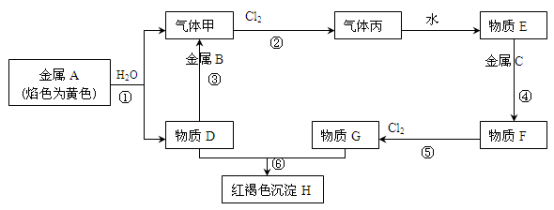
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分析下列相关实验,完成问题:
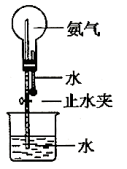
(1)如图进行喷泉实验,反应后烧瓶内的溶液中除含有 外,还含有的分子微粒为
外,还含有的分子微粒为___________ ;向反应后烧瓶内的溶液中滴加酚酞溶液,现象为___________ 。
(2)某兴趣小组探究 气体还原
气体还原 ,他们使用的药品和装置如图所示:
,他们使用的药品和装置如图所示:
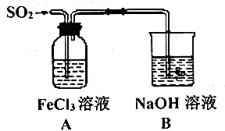
①装置B的作用___________ 。
②为了验证A中是否发生了氧化还原反应,兴趣小组设计了如下方案:取少量A中溶液于试管中,加入用稀盐酸酸化的 溶液,若产生白色沉淀,证明A中发生了氧化还原反应。试分析此方案是否合理
溶液,若产生白色沉淀,证明A中发生了氧化还原反应。试分析此方案是否合理___________ (填合理或不合理),该方案合理或不合理的原因是___________ 。
(1)如图进行喷泉实验,反应后烧瓶内的溶液中除含有
 外,还含有的分子微粒为
外,还含有的分子微粒为
(2)某兴趣小组探究
 气体还原
气体还原 ,他们使用的药品和装置如图所示:
,他们使用的药品和装置如图所示:
①装置B的作用
②为了验证A中是否发生了氧化还原反应,兴趣小组设计了如下方案:取少量A中溶液于试管中,加入用稀盐酸酸化的
 溶液,若产生白色沉淀,证明A中发生了氧化还原反应。试分析此方案是否合理
溶液,若产生白色沉淀,证明A中发生了氧化还原反应。试分析此方案是否合理
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】正误判断
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
您最近一年使用:0次



