某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程:
[提出假设] 假设1 该混合金属粉末中除铝外还含有_____ 元素;
假设2 该混合金属粉末中除铝外还含有_____ 元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
[设计实验方案]基于假设3,设计出实验方案(不要在答题卡上作答)。
[实验过程]根据上述实验方案,完成实验的相关操作、预期现象和结论。
[反思】写出在实验①中发生反应的离子方程式:___________________________________ 。
[提出假设] 假设1 该混合金属粉末中除铝外还含有
假设2 该混合金属粉末中除铝外还含有
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
[设计实验方案]基于假设3,设计出实验方案(不要在答题卡上作答)。
[实验过程]根据上述实验方案,完成实验的相关操作、预期现象和结论。
| 编号 | 实验操作 | 实验现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量 | 有固体剩余,并有气泡产生 | 合金中除铝外还含有Fe、Cu 元素 |
| ② | 往试管A的剩余固体中加过量 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | |
| ③ | 往试管B中加入少量 | ||
| ④ | 往②剩余固体中加入稀硝酸;再滴加 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色;再加某溶液后有蓝色沉淀产生 |
[反思】写出在实验①中发生反应的离子方程式:
11-12高二上·广东惠州·期末 查看更多[1]
(已下线)2010—2011学年广东省惠阳高级中学高二上学期期末考试化学试卷
更新时间:2016-12-09 01:30:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】计算题
(1)含0.4molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是___________ 。
(2)___________ molH2O2所含原子数与0.2molH3PO4所含原子数相等。
(3)把5.4g铝放入过量的烧碱中完全反应:
①写出该反应的离子方程式___________ ;
②计算标况下生成氢气的体积___________ ;
③计算反应消耗烧碱的质量为___________ ;
(1)含0.4molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(2)
(3)把5.4g铝放入过量的烧碱中完全反应:
①写出该反应的离子方程式
②计算标况下生成氢气的体积
③计算反应消耗烧碱的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理.根据所学知识,回答下列问题:
(1)沾有水的铁锅在高温火焰上灼烧会发黑(黑色物质为 ),该反应的化学方程式为
),该反应的化学方程式为____________ .
(2)食用加碘食盐能消除碘缺乏病的困扰,碘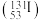 的质量数是
的质量数是____________ .
(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂.
①臭氧和氧气互为____________ (填“同位素”或“同素异形体”).
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是____________
③ 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用.
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用. 中
中 元素的化合价为
元素的化合价为____________ 价.
④高铁酸钠 还是一种新型的净水剂.其净水过程中所发生的化学反应主要为
还是一种新型的净水剂.其净水过程中所发生的化学反应主要为 (胶体)
(胶体)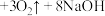 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为____________ .
(4)汽车安全气囊弹出时发生反应: ,该反应中氧化剂为
,该反应中氧化剂为____________ .
(5)铝制器具不宜盛放碱性食物,请写出铝与 溶液反应的离子方程式:
溶液反应的离子方程式:____________ .
(1)沾有水的铁锅在高温火焰上灼烧会发黑(黑色物质为
 ),该反应的化学方程式为
),该反应的化学方程式为(2)食用加碘食盐能消除碘缺乏病的困扰,碘
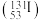 的质量数是
的质量数是(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂.
①臭氧和氧气互为
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
③
 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用.
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用. 中
中 元素的化合价为
元素的化合价为④高铁酸钠
 还是一种新型的净水剂.其净水过程中所发生的化学反应主要为
还是一种新型的净水剂.其净水过程中所发生的化学反应主要为 (胶体)
(胶体)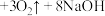 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为(4)汽车安全气囊弹出时发生反应:
 ,该反应中氧化剂为
,该反应中氧化剂为(5)铝制器具不宜盛放碱性食物,请写出铝与
 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国城市为了减少燃煤造成的大气污染,对作民用燃料的煤作了多方面的改进。
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反应:FeS2+14FeCl3+8H2O===2FeSO4+13FeCl2+16HCl。
①该反应中的氧化剂是________ ,若有1 mol FeS2被除去,则发生转移的电子的物质的量是________ 。
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新利用生成FeCl3。请写出这一过程中有关的离子方程式_____________________________ 、_________________________ 。
(2)某城市采用了以油制气代替煤作民用燃料的做法。油制气的主要成分是丙烷,请写出其燃烧的化学方程式:_______________________________ 。
(3)绿色能源是人类的理想能源,不会造成环境污染,下列能源属于绿色能源的是________ 。
A.氢能源 B.太阳能 C.风能 D.石油
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反应:FeS2+14FeCl3+8H2O===2FeSO4+13FeCl2+16HCl。
①该反应中的氧化剂是
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新利用生成FeCl3。请写出这一过程中有关的离子方程式
(2)某城市采用了以油制气代替煤作民用燃料的做法。油制气的主要成分是丙烷,请写出其燃烧的化学方程式:
(3)绿色能源是人类的理想能源,不会造成环境污染,下列能源属于绿色能源的是
A.氢能源 B.太阳能 C.风能 D.石油
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)纯碱的化学式为_______ 。
(2)化学家舍勒将软锰矿与浓盐酸混合加热,制得了氯气。软锰矿的主要成分为_______ (写化学式)。
(3)鉴别AgCl和Ag2CO3所用试剂为_______ ,写出反应的离子方程式_______ 。
(4)在钢铁厂,需要注入铁水的模具必须进行充分干燥处理,不得留有水,请用化学方程式解释其原因_______ 。
(1)纯碱的化学式为
(2)化学家舍勒将软锰矿与浓盐酸混合加热,制得了氯气。软锰矿的主要成分为
(3)鉴别AgCl和Ag2CO3所用试剂为
(4)在钢铁厂,需要注入铁水的模具必须进行充分干燥处理,不得留有水,请用化学方程式解释其原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空
(1)“四种基本反应类型与氧化还原反应的关系”如图所示:

其中I为化合反应,IV是___________ 反应。请写出一个符合IV的化学反应方程式_______________________________________________________ 。
(2)鲜榨苹果汁是人们喜爱的饮料,由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。这个变色过程中的Fe2+被_________ (填“氧化”或“还原”),若榨汁时加入适量的维生素C可有效防止这种现象的发生,这说明维生素C具有_______ 性。(填“氧化”或“还原”)
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_____________________________________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_________ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)“四种基本反应类型与氧化还原反应的关系”如图所示:

其中I为化合反应,IV是
(2)鲜榨苹果汁是人们喜爱的饮料,由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。这个变色过程中的Fe2+被
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组利用废铜屑制备硫酸铜晶体,装置如图所示(夹持装置和加热装置已略去),在实验中将适量硝酸逐滴加入到废铜屑与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶,制得硫酸铜晶体。
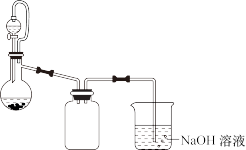
(1)将硝酸逐滴加入到废铜屑与稀硫酸的混合物中的目的是___ 。
(2)实验过程中盛有NaOH溶液的烧杯上方仍然出现了红棕色气体,请对该实验装置提出改进意见:___ 。

(1)将硝酸逐滴加入到废铜屑与稀硫酸的混合物中的目的是
(2)实验过程中盛有NaOH溶液的烧杯上方仍然出现了红棕色气体,请对该实验装置提出改进意见:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3=3Cu(NO3)2+2NO ↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目__________
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是___________ mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________ 。
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是
(3)被还原的硝酸占参加反应硝酸的比例为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。铳(Sc)是一种稀土金属,利用钛尾矿回收金属钪和草酸的工艺流程如图所示。回答下列问题:
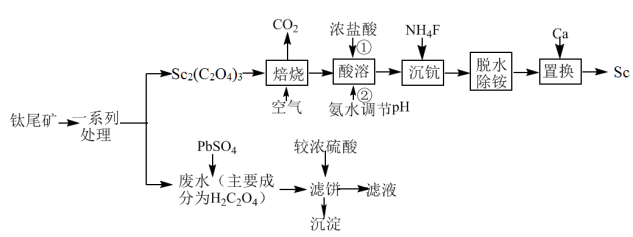
已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
“脱水除铵”过程中固体质量与温度的关系如图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到ScF3,由图中数据可得x:z=_______ 。
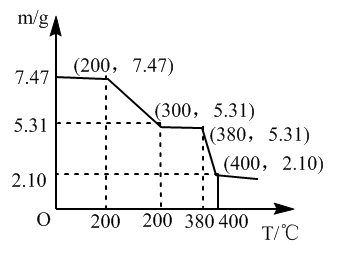

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
“脱水除铵”过程中固体质量与温度的关系如图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到ScF3,由图中数据可得x:z=

您最近一年使用:0次
【推荐2】硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是_______ 。
(2)检查装置气密性后加入药品,打开 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到_______ 时,再打开 。
。
(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是_______ ;装置D中除生成硫脲外,还生成一种碱,写出该过程D中发生反应的化学方程式:_______ 。
实验(二):探究硫脲的性质。
(4)①取少量 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加_______ ,可检验是否有 生成。
生成。
②取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
③取少量 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为_______ 。
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为_______ (用含m、c、V的代数式表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中可先制备 ,然后
,然后 再与
再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。回答下列问题:
,实验装置(夹持及加热装置略)如图所示。回答下列问题: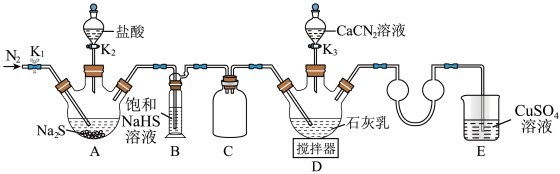
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。实验(一):制备硫脲。
(1)装置B中饱和NaHS溶液的作用是
(2)检查装置气密性后加入药品,打开
 ,通入一段时间
,通入一段时间 ,再打开
,再打开 ,当观察到
,当观察到 。
。(3)完成(2)中操作后,水浴加热装置D,在80℃条件下合成硫脲,控制温度在880℃的原因是
实验(二):探究硫脲的性质。
(4)①取少量
 溶于水,加热至150℃,一段时间后再冷却至室温,滴加
溶于水,加热至150℃,一段时间后再冷却至室温,滴加 生成。
生成。②取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤,洗涤,得到黑色固体,由此推知,
溶液,过滤,洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成③取少量
 溶液通过如图实验验证
溶液通过如图实验验证 被酸性
被酸性 溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性
溶液氧化的产物。关闭K,发现电流计指针偏转;一段时间后,左烧杯中酸性 溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有
溶液褪色,右烧杯中产生两种无毒气体,其溶液经检验有 生成,则石墨电极上的反应式为
生成,则石墨电极上的反应式为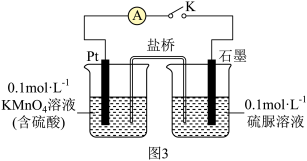
(5)装置D反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:称取mg产品,加水溶解配成250mL溶液,取25mL于锥形瓶中,加入稀硫酸酸化,用cmol/L酸性
 标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
标准溶液滴定,滴定至终点时消耗标准溶液VmL。则样品中硫脲的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】煤是我国重要的化石燃料,煤化工行业中产生的H2S也是一种重要的工业资源.
(1)煤液化是_____ (填“物理”或“化学”)变化过程。
(2)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:
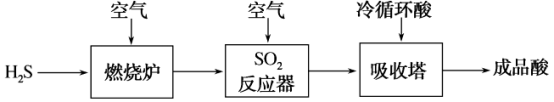
①SO2反应器中的化学方程式是_____ 。
②生产过程中的尾气需要测定SO2的含量符合标准才能排放.已知有V L(已换算成标准状况)尾气,通入足量H2O2吸收再加足量BaCl2溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到b g沉淀。尾气中SO2的含量(体积分数)的计算式是_____ 。
(3)H2S还可用于回收单质硫.含有H2S和空气的尾气按一定流速通入酸性FeCl3溶液,可实现空气脱硫,得到单质硫.FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S) 随时间t的变化如图。
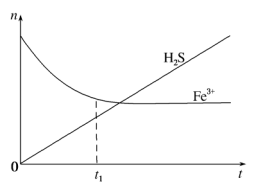
①由图中信息可知,0~t1时,一定发生的反应是_____ (用离子方程式表示)。
②t1以后,溶液中n(Fe3+)保持基本不变,原因是_____ 。
(1)煤液化是
(2)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:

①SO2反应器中的化学方程式是
②生产过程中的尾气需要测定SO2的含量符合标准才能排放.已知有V L(已换算成标准状况)尾气,通入足量H2O2吸收再加足量BaCl2溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到b g沉淀。尾气中SO2的含量(体积分数)的计算式是
(3)H2S还可用于回收单质硫.含有H2S和空气的尾气按一定流速通入酸性FeCl3溶液,可实现空气脱硫,得到单质硫.FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S) 随时间t的变化如图。

①由图中信息可知,0~t1时,一定发生的反应是
②t1以后,溶液中n(Fe3+)保持基本不变,原因是
您最近一年使用:0次



