NaCN超标的电镀废水可用两段氧化法处理:
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为___________ (选填“酸性”、“碱性”或“中性”);原因是___________ 。
(2)写出第二次氧化时发生反应的离子方程式。___________
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成___________ 、___________ 和H2O。
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为
(2)写出第二次氧化时发生反应的离子方程式。
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
更新时间:2021-11-09 20:19:59
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】 是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
(1) 中Cl的化合价为
中Cl的化合价为_________________ 。
(2)可用 还原硫酸酸化的
还原硫酸酸化的 制备
制备 ,产物还有
,产物还有 ,该反应的化学方程式为
,该反应的化学方程式为______________________ 。
(3)有效氯含量可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______________ (计算结果保留两位小数)。
 是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:(1)
 中Cl的化合价为
中Cl的化合价为(2)可用
 还原硫酸酸化的
还原硫酸酸化的 制备
制备 ,产物还有
,产物还有 ,该反应的化学方程式为
,该反应的化学方程式为(3)有效氯含量可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝完成下列填空:
(1)上述烟气处理过程中涉及到的化学物质,其组成元素中属于第三周期元素的是______ ;写出N的核外电子排布式______ 。
(2)已知SO2分子的空间构型折线形,则SO2为______ (选填“极性”、“非极性”)。
(3)将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
①表中y=______ mol•L-1。
②写出NaClO2溶液吸收SO2的离子方程式______ 。
(4)烟气中的SO2还可采用氨法脱硫除去,其反应原理可用如图表示。

①写出SO2跟氨水反应生成NH4HSO3的化学方程式______ 。
②(NH4)2HSO3溶液中浓度最大的离子是______ 。
(1)上述烟气处理过程中涉及到的化学物质,其组成元素中属于第三周期元素的是
(2)已知SO2分子的空间构型折线形,则SO2为
(3)将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
| 离子 | Na+ | SO42- | NO3- | OH- | Cl- |
| 浓度/(mol•L-1) | 5.5×10-3 | 8.5×10-4 | y | 2.0×10-4 | 3.4×10-3 |
②写出NaClO2溶液吸收SO2的离子方程式
(4)烟气中的SO2还可采用氨法脱硫除去,其反应原理可用如图表示。

①写出SO2跟氨水反应生成NH4HSO3的化学方程式
②(NH4)2HSO3溶液中浓度最大的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】“84”消毒液是一种常见的含氯消毒剂。
(1)“84”消毒液的有效成分为_______ (用化学式表示)。
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:_______ 。
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(1)“84”消毒液的有效成分为
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择填充并简述理由。
(1)处理钢瓶的方法正确的是______ ,简述理由______ .
A. 钢瓶推到坡下的小河里
B. 把钢瓶丢到深坑里,用石灰填埋
C. 把钢瓶扔到农田中
(2)钢瓶处理后,工人应立即______
A. 转移到坡下 B、转移到坡上 C、迎风跑 D、逆风跑
(3)若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是______ .
A、NaOH B、NaCl C、Na2O2 D、Na2CO3
(4)利用防毒面具可以有效防护氯气中毒,写出防毒面具产生氧气的化学方程式________________
(5)氯气泄漏可以用NaOH溶液吸收,写出该变化的离子方程式___________
(1)处理钢瓶的方法正确的是
A. 钢瓶推到坡下的小河里
B. 把钢瓶丢到深坑里,用石灰填埋
C. 把钢瓶扔到农田中
(2)钢瓶处理后,工人应立即
A. 转移到坡下 B、转移到坡上 C、迎风跑 D、逆风跑
(3)若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是
A、NaOH B、NaCl C、Na2O2 D、Na2CO3
(4)利用防毒面具可以有效防护氯气中毒,写出防毒面具产生氧气的化学方程式
(5)氯气泄漏可以用NaOH溶液吸收,写出该变化的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明 具有还原性的是实验
具有还原性的是实验_______ (填序号)。
(2)84消毒液的有效成分为 。
。
①NaClO中Cl元素的化合价是_______ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为_______ 。
(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式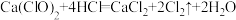 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:_______ 。
②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)_______ (填“能”或“不能”)同时使用,其原因是_______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①NaClO中Cl元素的化合价是
②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式
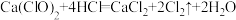 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】三氯氧磷(POCl3)广泛用于农药、医药及阻燃剂的生产工业等,工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。
(1)三氯氧磷可通过氯化水解法制备,由三氯化磷、水、氯气加热反应生成,则该反应中另一产物的化学式为____________ 。
(2)已知H3PO3为二元弱酸。某温度下,0.1 mol·L-1的H3PO3溶液中c(H+) = 2.5×10-2 mol·L-1。则该温度下H3PO3的第一步电离的平衡常数Ka1=_______ (H3PO3的第二步电离忽略不计,保留两位有效数字)。
(3)亚磷酸具有强还原性,可将Cu2+还原为金属单质,亚磷酸与硫酸铜溶液反应的化学方程式为_____________________ 。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中 c(PO43-)=4×10-7 mol·L-1,则溶液中c(Ca2+)=___________ mol·L-1。{已知Ksp=[Ca3(PO4)2]=2×10-29 }
(1)三氯氧磷可通过氯化水解法制备,由三氯化磷、水、氯气加热反应生成,则该反应中另一产物的化学式为
(2)已知H3PO3为二元弱酸。某温度下,0.1 mol·L-1的H3PO3溶液中c(H+) = 2.5×10-2 mol·L-1。则该温度下H3PO3的第一步电离的平衡常数Ka1=
(3)亚磷酸具有强还原性,可将Cu2+还原为金属单质,亚磷酸与硫酸铜溶液反应的化学方程式为
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中 c(PO43-)=4×10-7 mol·L-1,则溶液中c(Ca2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电离平衡常数的表示方法
(1)电离平衡常数表达式:
弱酸的电离平衡常数用______ 表示,弱碱的电离平衡常数用______ 表示。如:
CH3COOH电离常数的表达式:Ka=__________________ ;
NH3·H2O电离常数的表达式:Kb=__________________ 。
(2)多元弱酸的分步电离
H2CO3、H3PO4等多元弱酸在水溶液中分步电离,每步电离都有相应的电离平衡常数,如:
 ,所以Ka1=
,所以Ka1=____________ ,Ka2=___________ 。
一般情况下多步电离时电离平衡常数相差较大。各级电离平衡常数的大小关系是Ka1______ Ka2______ Ka3,所以其酸性主要决定于____________ 。
(1)电离平衡常数表达式:
弱酸的电离平衡常数用
CH3COOH电离常数的表达式:Ka=
NH3·H2O电离常数的表达式:Kb=
(2)多元弱酸的分步电离
H2CO3、H3PO4等多元弱酸在水溶液中分步电离,每步电离都有相应的电离平衡常数,如:

 ,所以Ka1=
,所以Ka1=一般情况下多步电离时电离平衡常数相差较大。各级电离平衡常数的大小关系是Ka1
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过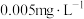 。处理含镉废水可采用化学沉淀法。已知:常温下,
。处理含镉废水可采用化学沉淀法。已知:常温下, ,
,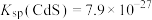 ,
,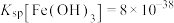 ,
, 。试回答下列问题:
。试回答下列问题:
(1)含浓度均为 的
的 、
、 的废液中,通过调pH的方式将
的废液中,通过调pH的方式将 完全沉淀出来而不损失
完全沉淀出来而不损失 的量(通常认为残留在溶液中的离子浓度小于
的量(通常认为残留在溶液中的离子浓度小于 时即完全沉淀),pH的取值范围为
时即完全沉淀),pH的取值范围为_______ 。
Ⅱ.氯化铁是一种强氧化剂和混凝剂,常用于污水处理、肝素制造、废气净化、雾霾治理等领域。
(2)用离子方程式解释 溶液可以用来净水的原理:
溶液可以用来净水的原理:_______ 。 的
的 溶液甲稀释为
溶液甲稀释为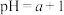 的溶液乙,则
的溶液乙,则
_______ 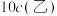 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(3)已知部分弱电解质的电离常数如下表(均为常温下的数据):
①100mL HB溶液中加入50mL等浓度的NaOH溶液,写出溶液中离子浓度大小关系:
HB溶液中加入50mL等浓度的NaOH溶液,写出溶液中离子浓度大小关系:_______ 。
②RA溶液中: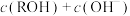
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
③比较结合 能力大小:
能力大小:
_____  (填“>”“=”或“<”),并用一个离子方程式证明:
(填“>”“=”或“<”),并用一个离子方程式证明:____ 。
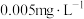 。处理含镉废水可采用化学沉淀法。已知:常温下,
。处理含镉废水可采用化学沉淀法。已知:常温下, ,
, ,
,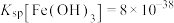 ,
, 。试回答下列问题:
。试回答下列问题:(1)含浓度均为
 的
的 、
、 的废液中,通过调pH的方式将
的废液中,通过调pH的方式将 完全沉淀出来而不损失
完全沉淀出来而不损失 的量(通常认为残留在溶液中的离子浓度小于
的量(通常认为残留在溶液中的离子浓度小于 时即完全沉淀),pH的取值范围为
时即完全沉淀),pH的取值范围为Ⅱ.氯化铁是一种强氧化剂和混凝剂,常用于污水处理、肝素制造、废气净化、雾霾治理等领域。
(2)用离子方程式解释
 溶液可以用来净水的原理:
溶液可以用来净水的原理: 的
的 溶液甲稀释为
溶液甲稀释为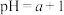 的溶液乙,则
的溶液乙,则
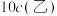 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(3)已知部分弱电解质的电离常数如下表(均为常温下的数据):
| 酸/碱 | 电离常数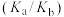 |
| HA |  |
| HB |  |
 | 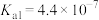 ; ; |
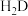 |  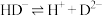 ; ; |
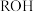 |  |
 HB溶液中加入50mL等浓度的NaOH溶液,写出溶液中离子浓度大小关系:
HB溶液中加入50mL等浓度的NaOH溶液,写出溶液中离子浓度大小关系:②RA溶液中:
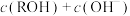
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。③比较结合
 能力大小:
能力大小:
 (填“>”“=”或“<”),并用一个离子方程式证明:
(填“>”“=”或“<”),并用一个离子方程式证明:
您最近一年使用:0次



