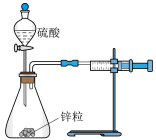
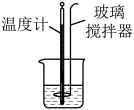
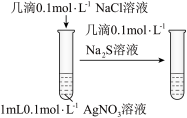
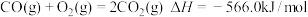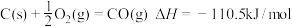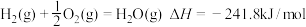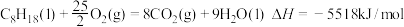已知:①
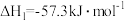 ,②
,②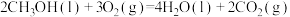
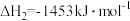 ,下列有关说法正确的是
,下列有关说法正确的是
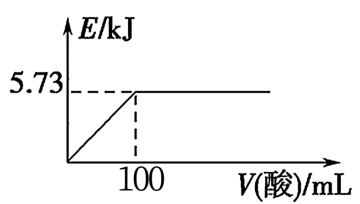

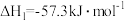 ,②
,②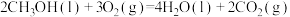
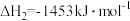 ,下列有关说法正确的是
,下列有关说法正确的是
A.甲醇的燃烧热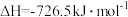 |
B.若反应②中水为气态,则同样条件下的反应热: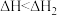 |
C.向含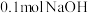 的溶液中加入一定体积 的溶液中加入一定体积 的醋酸,反应中的热量变化如图所示 的醋酸,反应中的热量变化如图所示 |
D.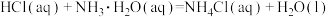 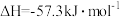 |
更新时间:2021-01-13 10:03:48
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
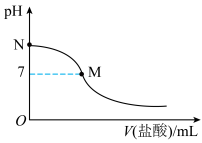
【推荐1】常温下,向25.00mL0.10mol·L-1氨水中滴入 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
| A.用量筒量取25.00mL0.10mol·L-1 氨水 |
| B.可根据该反应过程中放出的热量计算中和反应反应热 |
C.M点对应的盐酸体积为 |
D.N点处的溶液中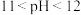 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列叙述中,错误的是
| A.在测定中和热实验中需要使用的仪器有天平、量筒、烧杯、温度计 |
| B.金属和石墨导电均为物理变化,电解质溶液导电是化学变化 |
| C.不能自发进行的氧化还原反应通过电解有可能实现 |
| D.Cu+2Ag+=Cu2++2Ag,反应既可以在原电池中实现,也可以在电解池中实现 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】如表所列的“依据”能推导出后面的“结论”的是
| 依据 | 结论 | |
| A | CH4(g)+2O2(g)= CO2(g)+2H2O(g)ΔH=-801.3kJ·mol-1 | CH4的燃烧热ΔH=-801.3kJ·mol-1 |
| B | Sn(灰,s)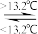 Sn(白,s)ΔH=+2.1kJ·mol-1 Sn(白,s)ΔH=+2.1kJ·mol-1 | 白锡制品在寒冷的冬天因易转化为灰状锡而损坏 |
| C | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1 | 盐酸与氨水反应的中和热为57.3kJ·mol-1 |
| D | C(墨,s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1 C(金刚石,s)+O2(g)=CO2(g)ΔH=-395kJ·mol-1 | 石墨转化为金刚石会放出热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列热化学方程式中,△H能正确表示物质的燃烧热的是
| A.2CO(g) +O2(g) =2CO2(g) △H=—566.0 kJ/mol |
| B.C(s) +1/2O2(g) =CO(g) △H=—110.5 kJ/mol |
| C.CH4(g) +2O2(g)= CO2(g)+2H2O(l) △H=—890.31 kJ/mol |
| D.2C8H18(l) +25O2(g)=16CO2(g)+18H2O(l) △H=—11036 kJ/mol |
您最近一年使用:0次
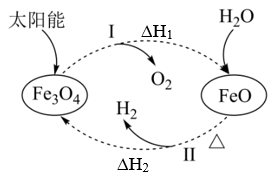
【推荐1】以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述正确的是
的过程如图所示。下列叙述正确的是
 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述正确的是
的过程如图所示。下列叙述正确的是
| A.过程Ⅰ中的能量转化形式是化学能→太阳能 |
B. 的燃烧热 的燃烧热 |
C.过程Ⅱ中3mol FeO(s)的总能量高于1mol  |
D.铁氧化合物循环制 具有节约能源、产物易分离等优点 具有节约能源、产物易分离等优点 |
您最近一年使用:0次
【推荐2】下图为反应:H2(g)+Cl2(g)=2HCl(g)的能量变化示意图,下列说法正确的是


| A.该反应每生成2molHCl,放出183kJ的热量 |
| B.该反应生成液态HCl比生成气态HCl释放的能量少 |
| C.氯气分子中的化学键比氢气分子中的化学键更稳定 |
| D.1 molHCl分子中的化学键形成时吸收431kJ的能量 |
您最近一年使用:0次

 和
和 溶解度大小
溶解度大小