如图是元素周期表的一部分,图中所列的字母分别代表某一化学元素。
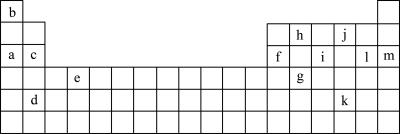
(1)下列______ (填序号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/( )
)
①X可能为图中13种元素中的______ (填字母)。用元素符号表示X和j形成的化合物的化学式:______ 。
②Y是周期表中第______ 族的元素。
③图中13种元素中,______ (填字母)元素原子失去核外第1个电子需要的能量最多。

(1)下列
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/(
 )
)| 元素 | 锂 | X | Y |
| 失去第1个电子 | 519 | 502 | 580 |
| 失去第2个电子 | 7296 | 4570 | 1820 |
| 失去第3个电子 | 11799 | 6920 | 2750 |
| 失去第4个电子 | — | 9550 | 11600 |
②Y是周期表中第
③图中13种元素中,
更新时间:2021-02-06 11:47:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表前四周期部分,针对表中的①~⑨9种元素,用化学用语填写下列空白:
(1)①~⑨中,单质化学性质最不活泼的是__________ ,最高价氧化物对应的水化物的酸性最强的是__________ 。
(2)②、③、④的简单离子按离子半径从小到大排列顺序为_________________ 。
(3)④在③单质中燃烧的产物的电子式为_________________ 。
(4)⑤的原子结构示意图为________ ,从原子结构分析,④比⑤活泼的原因是_________ 。
(5)②和⑦形成一种化合物分子,各原子均达到8电子稳定结构,则该化合物的化学式为_________________ 。
(6)②、③的最简单氢化物中,沸点较高的是_____________ 。
(7)②的简单氢化物与②的最高价氧化物的水化物溶液反应的化学方程式为:________ 。
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | |||||||||||||||||
(1)①~⑨中,单质化学性质最不活泼的是
(2)②、③、④的简单离子按离子半径从小到大排列顺序为
(3)④在③单质中燃烧的产物的电子式为
(4)⑤的原子结构示意图为
(5)②和⑦形成一种化合物分子,各原子均达到8电子稳定结构,则该化合物的化学式为
(6)②、③的最简单氢化物中,沸点较高的是
(7)②的简单氢化物与②的最高价氧化物的水化物溶液反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表中为元素周期表的一部分,请参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)在①~⑧元素中,_______ 原子半径最大;④、⑤、⑥的离子半径由大到小的顺序为_______ 。
(2)②、⑦、⑧的最高价氧化物对应的水化物的酸性由强到弱的顺序是__________ 。
(3)③、④、⑦的气态氢化物的稳定性由强到弱的顺序是________ 。
(4)⑥、⑧的最高价氧化物对应的水化物之间能发生化学反应的离子方程式为_______ 。
(5)往Na2SiO3的水溶液中通入足量的CO2 ,其反应的离子方程式为________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、⑦、⑧的最高价氧化物对应的水化物的酸性由强到弱的顺序是
(3)③、④、⑦的气态氢化物的稳定性由强到弱的顺序是
(4)⑥、⑧的最高价氧化物对应的水化物之间能发生化学反应的离子方程式为
(5)往Na2SiO3的水溶液中通入足量的CO2 ,其反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是___________ (填元素符号)。
(2)用电子式表示元素⑥与⑨的化合物的形成过程:___________
(3)③、⑤、⑦、⑨四种元素形成的离子,离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)表示①与⑨的化合物的化学式为___________ ,该化合物是由___________ (填“极性”或“非极性”)键构成。
(5)①~⑨种元素的最高价氧化物对应的水化物中,碱性最强的化合物是___________ (填化学式),在常温下该化合物和元素⑨的单质反应的离子方程式___________
| 主族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ③ | ④ | ||||
| 第三周期 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)用电子式表示元素⑥与⑨的化合物的形成过程:
(3)③、⑤、⑦、⑨四种元素形成的离子,离子半径由大到小的顺序是
(4)表示①与⑨的化合物的化学式为
(5)①~⑨种元素的最高价氧化物对应的水化物中,碱性最强的化合物是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
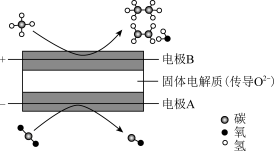
(1)C、N、O三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。
(2)已知相同条件下生成乙烯和乙烷的体积比为2∶1,消耗CH4和CO2的体积比为6∶5,则生成的CO和H2O的物质的量之比为_______ 。
(3)①已知碳和硅的有关化学键键能如表所示:
简要分析乙烷的稳定性大于 的原因:
的原因:_______ 。
②如图表示碳、硅和磷三种元素的四级电离能的变化趋势,其中表示硅的曲线是_______ (填字母),判断的依据是_______ 。

(4)①通常情况下,与乙烯的沸点(-103.7℃)相比,氯乙烯(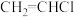 )的沸点更高(-13.9℃),其原因是
)的沸点更高(-13.9℃),其原因是_______ 。
②在乙烯中碳碳双键的键长为134pm,而在氯乙烯中碳碳双键的键长为138pm,请解释原因:____ 。

(1)C、N、O三种元素的第一电离能由大到小的顺序是
(2)已知相同条件下生成乙烯和乙烷的体积比为2∶1,消耗CH4和CO2的体积比为6∶5,则生成的CO和H2O的物质的量之比为
(3)①已知碳和硅的有关化学键键能如表所示:
| 化学键 |  |  |  | 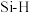 |
键能/( ) ) | 356 | 413 | 226 | 318 |
简要分析乙烷的稳定性大于
 的原因:
的原因:②如图表示碳、硅和磷三种元素的四级电离能的变化趋势,其中表示硅的曲线是

(4)①通常情况下,与乙烯的沸点(-103.7℃)相比,氯乙烯(
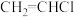 )的沸点更高(-13.9℃),其原因是
)的沸点更高(-13.9℃),其原因是②在乙烯中碳碳双键的键长为134pm,而在氯乙烯中碳碳双键的键长为138pm,请解释原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】如表为长式周期表的一部分,其中的编号代表对应的元素。
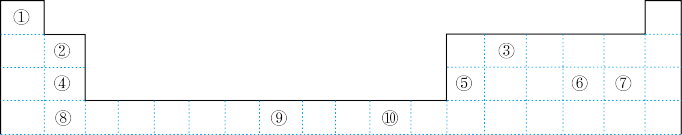
请回答下列问题:
(1)表中属于d区的元素是_______ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_______ 。
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为_______ ;该元素与元素①形成的分子X的立体构型为_______ ,与⑧在同一周期的元素中的未成对电子数目最多的元素的价电子排布式是_______ 。
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(1)基态Fe原子有________ 个未成对电子,Fe3+的电子排布式为 ________ 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________ 。
(2)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍, d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是________ (填元素符号),e的价层电子轨道示意图为________ 。
(3)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。
(4)基态硼原子的电子排布式为______ 。Ga基态原子的核外电子排布式是______ 。Cu+基态核外电子排布式为________ 。
(2)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍, d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是
(3)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。
请回答下列问题:
Y基态原子的电子排布式是
(4)基态硼原子的电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表中的前四周期,回答下列问题:

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①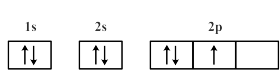 ②
②
另一个电子排布图错误的原因是:它不符合_______ (填标号)。
A.构造原理 B.泡利原理 C.洪特规则
b元素的正二价离子的核外价电子排布图是_______ 。
(2)b、e两种元素的第四电离能大小关系为 ____>
____> _____,
_____,_______ (填元素符号),原因是_______ 。
(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为_______ (填元素符号)
(4)某元素的原子价电子排布式为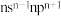 ,该基态原子核外电子空间运动状态有
,该基态原子核外电子空间运动状态有_______ 种。
(5)d元素的下列微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
(6)下列现象与原子核外电子跃迁有关的是_______ (填标号)
a.激光 b.LED灯光 c.金属导电 d.核辐射

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①
 ②
②
另一个电子排布图错误的原因是:它不符合
A.构造原理 B.泡利原理 C.洪特规则
b元素的正二价离子的核外价电子排布图是
(2)b、e两种元素的第四电离能大小关系为
 ____>
____> _____,
_____,(3)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为
(4)某元素的原子价电子排布式为
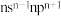 ,该基态原子核外电子空间运动状态有
,该基态原子核外电子空间运动状态有(5)d元素的下列微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. | B. | C. | D. |
a.激光 b.LED灯光 c.金属导电 d.核辐射
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。

(1)a和c的I1大小关系是______ 大于______ 。(填字母)
(2)上述元素中,原子中未成对电子数最多的是______ (填字母),写出该元素基态原子的核外电子排布式:______ 。
(3)根据下表所提供的电离能数据,回答下列问题。
①表中X可能为以上13种元素中的______ (填字母)元素。用元素符号表示 和j形成的一种化合物的化学式:
和j形成的一种化合物的化学式:______ 。
②Y是周期表中第______ 族元素。
③以上13种元素中,______ (填字母)元素原子失去核外第一个电子需要的能量最多。

(1)a和c的I1大小关系是
(2)上述元素中,原子中未成对电子数最多的是
(3)根据下表所提供的电离能数据,回答下列问题。
| 锂 | X | Y | |
| I1 | 520 | 496 | 580 |
| I2 | 7296 | 4570 | 1820 |
| I3 | 11799 | 6920 | 2750 |
| I4 | 9550 | 11600 |
①表中X可能为以上13种元素中的
 和j形成的一种化合物的化学式:
和j形成的一种化合物的化学式:②Y是周期表中第
③以上13种元素中,
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子排布式为_______ ;第一电离能
_______ 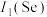 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是_______ 。
(2) 是一种剧毒气体,其中心原子杂化轨道类型
是一种剧毒气体,其中心原子杂化轨道类型_______ 。
(3) 的熔点约为712℃,
的熔点约为712℃, 的熔点约为194℃,其晶体类型分别是
的熔点约为194℃,其晶体类型分别是_______ 、_______ 。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止 刻蚀液与下层GaAs(砷化镓)反应。
刻蚀液与下层GaAs(砷化镓)反应。
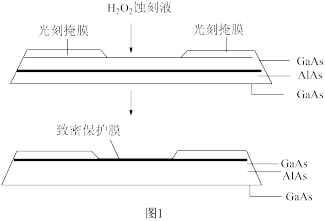
①上述致密保护膜是一种常见的金属氧化物,其化学式为_______ 。
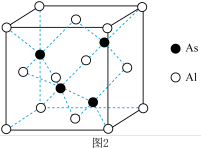
②已知AlAs的立方晶胞如图2所示,其中As的配位数为_______ ;该晶体密度为 ,设
,设 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为_______ pm。
(1)基态As原子的核外价电子排布式为

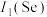 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是(2)
 是一种剧毒气体,其中心原子杂化轨道类型
是一种剧毒气体,其中心原子杂化轨道类型(3)
 的熔点约为712℃,
的熔点约为712℃, 的熔点约为194℃,其晶体类型分别是
的熔点约为194℃,其晶体类型分别是(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止
 刻蚀液与下层GaAs(砷化镓)反应。
刻蚀液与下层GaAs(砷化镓)反应。

①上述致密保护膜是一种常见的金属氧化物,其化学式为
②已知AlAs的立方晶胞如图2所示,其中As的配位数为
 ,设
,设 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为
您最近一年使用:0次



