下列各种溶液中,可能大量共存的离子组是
A.pH=1的溶液中:Fe2+、 、 、 、Cl- 、Cl- |
B.由水电离出的c(OH-)=1×10-13mol·L-1的溶液中:Na+、 、S2-、 、S2-、 |
C.含有大量Fe3+的溶液中:Na+、SCN-、K+、 |
D.c(H+)=10-14mol·L-1的溶液中:Mg2+、 、Fe2+、ClO- 、Fe2+、ClO- |
更新时间:2021-02-21 10:36:15
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在某澄清透明的酸性溶液中,可能大量共存的离子组是( )
| A.Na+、K+、SO32-、SO42- | B.Na+、Fe2+、Cl-、MnO4- |
| C.Na+、K+、SiO32-、NO3- | D.Al3+、NH4+、SO42-、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某溶液中大量存在以下五种离子:  、
、 、Fe3+、H+、M,它们的个数之比为N(
、Fe3+、H+、M,它们的个数之比为N( )∶N(
)∶N( )∶N(Fe3+)∶N(H+)∶N(M)=2∶3∶1∶3∶1,则M可能为(HNO3具有强氧化性)
)∶N(Fe3+)∶N(H+)∶N(M)=2∶3∶1∶3∶1,则M可能为(HNO3具有强氧化性)
 、
、 、Fe3+、H+、M,它们的个数之比为N(
、Fe3+、H+、M,它们的个数之比为N( )∶N(
)∶N( )∶N(Fe3+)∶N(H+)∶N(M)=2∶3∶1∶3∶1,则M可能为(HNO3具有强氧化性)
)∶N(Fe3+)∶N(H+)∶N(M)=2∶3∶1∶3∶1,则M可能为(HNO3具有强氧化性)| A.Mg2+ | B.Fe2+ |
C.  | D.Ba2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用如下实验研究Fe3+与I—的反应。
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
| A.试管①中的现象说明此条件下Fe3+的氧化性大于I2 |
| B.试管②中的现象说明Fe3+与I—的反应为可逆反应 |
| C.步骤4的现象能说明此条件下I2能将Fe2+氧化成Fe3+ |
| D.试管②中红色物质的组成为[Fe(SCN)n(H2O)6—n]3—n,此微粒中心离子的配位数为n |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验现象的描述错误的是
| A.新制氯水使淀粉试纸呈蓝色 |
| B.向NaHCO3固体加入新制氯水,有无色气体产生 |
| C.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色 |
| D.在新制氯水中滴加AgNO3溶液有白色沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】FeCl3的水解方程式可写为FeCl3+3H2O⇌Fe(OH)3+3HCl,若提高水解程度,可采取的方法是
| A.降温 | B.加入饱和食盐水 | C.加入少量盐酸 | D.增加FeCl3的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于盐类水解的说法错误的是
A.在NH4Cl溶液中加入稀盐酸能抑制 水解 水解 |
| B.常温下,醋酸分子不可能存在于pH>7的碱性溶液中 |
| C.实验室配制FeCl3溶液时,常将FeCl3晶体溶于较浓的盐酸中,再加水稀释到所需浓度 |
| D.滴有酚酞的CH3COONa溶液加热,溶液颜色会变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在一定条件下,Na2CO3溶液存在水解平衡: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.稀释溶液,各物质浓度均减小,平衡不移动 |
| B.加入少量NaHCO3固体,平衡向正反应方向移动 |
C.升高温度,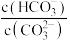 减小 减小 |
| D.加入NaOH固体,溶液pH增大 |
您最近一年使用:0次

 =1013的溶液:Fe2+、Cl-、MnO4-、SO42-
=1013的溶液:Fe2+、Cl-、MnO4-、SO42- 和
和 两种溶液( 焰色反应)
两种溶液( 焰色反应) 两种溶液(激光笔)
两种溶液(激光笔) 溶液
溶液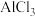 两种溶液(NaOH溶液)
两种溶液(NaOH溶液) 和
和 两种溶液(KSCN溶液)
两种溶液(KSCN溶液)

