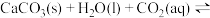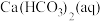FeCl3的水解方程式可写为FeCl3+3H2O⇌Fe(OH)3+3HCl,若提高水解程度,可采取的方法是
| A.降温 | B.加入饱和食盐水 | C.加入少量盐酸 | D.增加FeCl3的浓度 |
更新时间:2017-11-02 16:05:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关说法或对有关现象的解释正确的是( )
| A.钠与浓NH4Cl溶液反应,放出的气体中含H2和NH3 |
| B.SO2和NH3分别通入水中,溶液均可以导电,所以SO2和NH3均属于电解质 |
| C.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3 |
| D.SiO2既可与NaOH溶液反应也可与HF溶液反应均生成盐和水,所以SiO2属于两性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】测定0.1mol·L−1Na2SO3溶液先升温再降温过程中的pH,数据如下表。
实验过程中,取①、④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。下列说法不正确 的是
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
A.Na2SO3溶液中存在水解平衡: +H2O⇌ +H2O⇌ +OH− +OH− |
| B.④产生的白色沉淀是BaSO4 |
C.①→③的过程中,c( )在降低 )在降低 |
D.①→③的过程中,温度对水解平衡的影响比c( )的影响更大 )的影响更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下述实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入溴水中 | 验证SO2具有漂白性 |
| B | 在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色褪去 | 验证Na2CO3溶液中存在水解平衡 |
| C | 淀粉溶液和稀H2SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸 | 检验淀粉水解产物有还原性 |
| D | 将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 | 检验气体中含有乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 的化学性质与
的化学性质与 相似。用
相似。用 配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于
配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于 的相关实验叙述正确的是
的相关实验叙述正确的是

 的化学性质与
的化学性质与 相似。用
相似。用 配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于
配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于 的相关实验叙述正确的是
的相关实验叙述正确的是
| A.用A装置稀释浓盐酸 | B.用B装置加快 溶解 溶解 |
C.用C装置保存 溶液 溶液 | D.用D装置制备无水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关说法正确的是
A.少量Ca(OH)2溶液和NaHCO3溶液反应的离子方程式:Ca2++OH-+HCO =CaCO3↓+H2O =CaCO3↓+H2O |
| B.Fe2+与H2O2在酸性溶液中反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O |
C.pH=2的溶液中可能大量存在Na+、NH 、SiO 、SiO |
| D.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作过程中颜色变化所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将NaClO溶液滴入品红溶液中,品红溶液缓慢褪色;若同时加入食醋,红色很快褪去 | ClO-的氧化性随pH的减小而增强 |
| B | 将石油分馏的产品石蜡加热,产生的气体通入酸性高锰酸钾溶液中,溶液紫红色逐渐褪去 | 石油中含有烯烃 |
| C | 向滴有酚酞的氨水中加入CH3COONH4固体,溶液的红色变浅 | CH3COONH4溶液呈酸性 |
| D | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3溶液,产生两种颜色沉淀,但以白色为主 | 溶液中c(Cl-)/c(Br-)减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(
含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下( ,
, )海水中
)海水中 浓度与模拟空气中
浓度与模拟空气中