测定0.1mol·L−1Na2SO3溶液先升温再降温过程中的pH,数据如下表。
实验过程中,取①、④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。下列说法不正确 的是
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
A.Na2SO3溶液中存在水解平衡: +H2O⇌ +H2O⇌ +OH− +OH− |
| B.④产生的白色沉淀是BaSO4 |
C.①→③的过程中,c( )在降低 )在降低 |
D.①→③的过程中,温度对水解平衡的影响比c( )的影响更大 )的影响更大 |
更新时间:2021/01/24 15:25:57
|
相似题推荐
单选题
|
适中
(0.65)
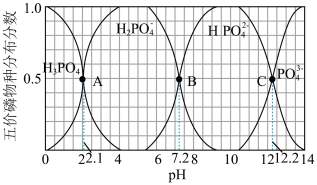
【推荐1】氧化铍( )在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含
)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含 、
、 、
、 和
和 等)为原料提取
等)为原料提取 的流程如图所示。
的流程如图所示。
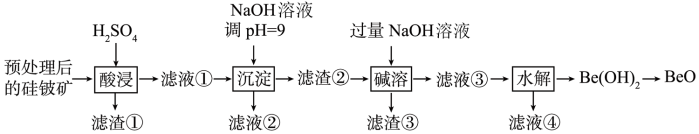
已知: 具有两性,在强碱性溶液中可转化为
具有两性,在强碱性溶液中可转化为 。下列说法错误的是
。下列说法错误的是
 )在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含
)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含 、
、 、
、 和
和 等)为原料提取
等)为原料提取 的流程如图所示。
的流程如图所示。
已知:
 具有两性,在强碱性溶液中可转化为
具有两性,在强碱性溶液中可转化为 。下列说法错误的是
。下列说法错误的是A.“酸浸”步骤所得滤渣①的主要成分为 |
B.滤液②经处理后可获得副产品 |
C.“碱溶”时,主要反应为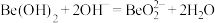 |
D.“水解”时,适当增大溶液 有利于提高 有利于提高 的提取率 的提取率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】25℃时100 mL1 mol/L的三种盐溶液NaX、NaY、NaZ、pH分别为7、8、9下列说法正确的是
| A.HX、HY、HZ的酸性依次增强,电离平衡常数依次减小 |
| B.三种溶液所含阴、阳离子的总数依次增多 |
| C.三种溶液均加水稀释到1000 mL,pH分别变为8、9、10 |
| D.2c(X-)-c(Y- )=c(HY)+c(Z-)+c(HZ) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验中,现象及结论都正确,且二者之间有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeI2溶液中通入少量Cl2 | 溶液变黄 | 则Cl2的氧化性强于Fe3+ |
| B | FeCl3溶液和KSCN溶液混合反应后,再加入少量KCl溶液 | 溶液红色加深 | 增大反应物浓度,平衡正向移动 |
| C | 将铜粉加入到1.0mol·L−1Fe2(SO4)3溶液中 | 铜粉溶解,溶液变蓝 | 金属铁比铜活泼 |
| D | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数:Kh(CH3COO−)<Kh(HCO ) ) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列比较中,正确的是( )
| A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大 |
| B.0.2mol·L-1NH4Cl和0.1mol·L-1NaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| D.同浓度的下列溶液中,(1)NH4Al(SO4)2、(2)NH4Cl、(3)CH3COONH4、(4)NH3·H2O;c(NH4+)由大到小的顺序是:(1)>(2)>(3)>(4) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是
 HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是| A.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B.升高温度,溶液的pH减小 |
| C.稀释溶液,溶液中c(H+)和c(OH-)都减少 |
| D.加入NaOH固体,溶液pH减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,Na2CO3溶液中存在平衡: +H2O
+H2O
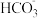 +OH-,下列有关该溶液的说法正确的是
+OH-,下列有关该溶液的说法正确的是
 +H2O
+H2O
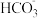 +OH-,下列有关该溶液的说法正确的是
+OH-,下列有关该溶液的说法正确的是| A.Na2CO3在水解过程导致碳酸钠电离平衡被促进 |
| B.升高温度,平衡向右移动 |
| C.滴入CaCl2浓溶液,溶液的pH增大 |
| D.加入NaOH固体,溶液的pH减小 |
您最近半年使用:0次