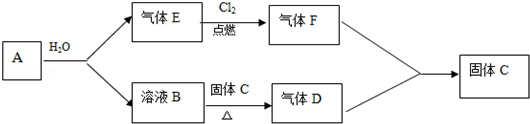
如图为物质转化关系,其中甲是一种金属单质,燃烧时,火焰为黄色。A、C、F常温下为气体;其中C为黄绿色,且A与C点燃时产生苍白色火焰,并且在瓶口有白雾出现。F为温室效应气体,乙为厨房中常用的一种盐,热稳定性强,灼烧时火焰为黄色。
回答下列问题:
(1)写出下列的化学式:A:___ ,B:___ ,D:___ ,F:___ 。
(2)写出甲与水反应的化学方程式:___ 。
(3)写出D与乙反应的化学方程式:___ 。
(4)反应B和F反应的离子方程式:___ 。
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式___ 。

回答下列问题:
(1)写出下列的化学式:A:
(2)写出甲与水反应的化学方程式:
(3)写出D与乙反应的化学方程式:
(4)反应B和F反应的离子方程式:
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式
更新时间:2021-03-02 17:28:58
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】P、Q、W、X、Y、Z是元素周期表前36号元素中的六种常见元素,其原子序数依次增大。W原子最外层电子数与核外电子总数之比是3:4,P可与W形成两种常见的化合物M和N,其分子中原子个数比分别为2:1和1:1,Q、Y的氧化物是导致酸雨的主要物质,X是地壳中含量最高的金属元素,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)N的电子式为:___________ 。W、X、Y的离子半径大到小的顺序为___________ (用离子符号回答)
(2)XQ是一种新型的结构陶瓷材料,具备许多优良的性能,合成的方法之一是高温时用过量的碳在Q单质气体的氛围中还原X的氧化物,试写出该反应的化学反应方程式:___________ 。
(3)已知常温时NaPYW3的溶液呈现较强的酸性,则其溶液中各离子浓度由大到小的排列顺序为:___________ 。
(4)Q的氢化物与Y的最高价氧化物对应的水化物反应生成一种正盐,其水溶液呈___________ 性,原因是___________ (离子方程式解释)
(5)ZCl2溶液中混有FeCl3杂质时,可加入___________ (填试剂化学式)调节pH=___________ ,再过滤。(Fe(OH)3的 ,化学式认为残留在溶液中的离子浓度小于10-5mol/L时沉淀就达完全。)
,化学式认为残留在溶液中的离子浓度小于10-5mol/L时沉淀就达完全。)
(6)工业上可用高温条件下 来冶炼金属Z,生成1molZ时转移的电子总数为
来冶炼金属Z,生成1molZ时转移的电子总数为___________ mol。
(1)N的电子式为:
(2)XQ是一种新型的结构陶瓷材料,具备许多优良的性能,合成的方法之一是高温时用过量的碳在Q单质气体的氛围中还原X的氧化物,试写出该反应的化学反应方程式:
(3)已知常温时NaPYW3的溶液呈现较强的酸性,则其溶液中各离子浓度由大到小的排列顺序为:
(4)Q的氢化物与Y的最高价氧化物对应的水化物反应生成一种正盐,其水溶液呈
(5)ZCl2溶液中混有FeCl3杂质时,可加入
 ,化学式认为残留在溶液中的离子浓度小于10-5mol/L时沉淀就达完全。)
,化学式认为残留在溶液中的离子浓度小于10-5mol/L时沉淀就达完全。)(6)工业上可用高温条件下
 来冶炼金属Z,生成1molZ时转移的电子总数为
来冶炼金属Z,生成1molZ时转移的电子总数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
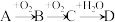
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途____ ;
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式_____ ;
(3)若A为单质,D为弱酸,则A在工业生产中可用于制备同族另一种非金属单质,该反应的化学方程式为____ ;
(4)若A是化合物,C是红棕色气体,则A的化学式为_____ ;C转化为D的过程中,氧化剂与还原剂的质量比为____ 。
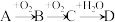
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式
(3)若A为单质,D为弱酸,则A在工业生产中可用于制备同族另一种非金属单质,该反应的化学方程式为
(4)若A是化合物,C是红棕色气体,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有中学化学常见四种金属单质A、B、C、I和三种常见气体甲、乙、丙及物质D、E、F、G、H。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)
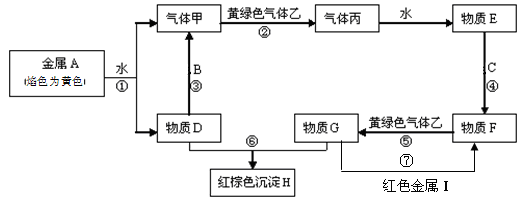
请根据以上信息回答下列问题:
(1)写出物质H的化学式:_______________ ,物质E的名称:_______________ ;
(2)写出反应③的化学方程式___________________ ;写出反应⑦的离子方程式____________ ;
(3)请写出图示中物质C与水蒸气在高温下反应的化学方程式______________ ;
(4)描述一种检验反应④所得产物中阳离子的操作__________________ 。

请根据以上信息回答下列问题:
(1)写出物质H的化学式:
(2)写出反应③的化学方程式
(3)请写出图示中物质C与水蒸气在高温下反应的化学方程式
(4)描述一种检验反应④所得产物中阳离子的操作
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入到适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题:
(1)写出下列各反应的化学方程式
①纯净的A在B中安静地燃烧生成C_______________
②将气体B通入到水中:__________ 。
③将气体B通入到NaOH溶液中:_______________________
④将气体B通入到适量石灰乳中:_______________________
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是________ (用字母表示)。
(3)将白色浑浊物D溶于水得到澄清溶液,分别取适量该澄清液两份。
①向第一份中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为______________ 、________ 。
②向第二份溶液中滴加硝酸酸化的硝酸银溶液,会观察到____________ (填现象)。
③白色浑浊物D因具有漂白性又称为______________ ,该物质在空气中容易变质的原因为_______________ (用化学方程式表示)。
(1)写出下列各反应的化学方程式
①纯净的A在B中安静地燃烧生成C
②将气体B通入到水中:
③将气体B通入到NaOH溶液中:
④将气体B通入到适量石灰乳中:
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是
(3)将白色浑浊物D溶于水得到澄清溶液,分别取适量该澄清液两份。
①向第一份中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为
②向第二份溶液中滴加硝酸酸化的硝酸银溶液,会观察到
③白色浑浊物D因具有漂白性又称为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有A、B、C三种元素:(1)A、B、C的单质在常温下为气体。(2)A的单质可以在C的单质中燃烧生成AC,火焰为苍白色。(3)AC极易溶于水,其水溶液可使蓝色石蕊试纸变红。(4)单质A可以和单质B化合生成A2B(常温下为液体)。(5)C的单质溶于A2B中可得到一种具有漂白性的物质ACB,请推断:
①A、B、C各为何元素(写元素符号)A__________ ;B__________ ;C__________
②AC和ACB各是什么物质(写化学式)AC__________ ;ACB__________
③写出C的单质溶于A2B的化学方程式___________________________________
①A、B、C各为何元素(写元素符号)A
②AC和ACB各是什么物质(写化学式)AC
③写出C的单质溶于A2B的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯碱工厂按下面的流程生产:

(1)电解饱和食盐水的化学方程式是_______ ,氯气在_______ 极产生,检验氯气的方法是_______ 。若产生了71g氯气,则阴极产生气体的物质的量为_______ ,同时生成的氢氧化钠的质量为_______ 。
(2)该流程中合成氯化氢的化学方程式为_______ ,燃烧时火焰呈_______ 色。生成的氯化氢溶于水即得盐酸,写出氯化氢的电离方程式_______ 。
某化学兴趣小组欲用下图装置制备氯水并探究其性质。
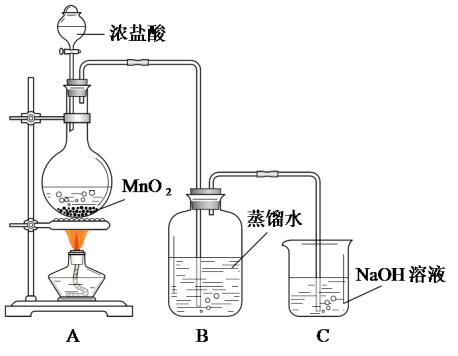
(3)烧瓶内发生的化学反应是_______ (书写化学方程式)。
(4)C装置的作用是_______ ,其中发生的化学反应是_______ (书写化学方程式)。
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:_______ ;化学性质变化:_______ 。
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
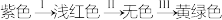
导致变色的微粒I、II、III依次为_______。
(7)某同学从B中取出少量样品,滴在NaHCO3粉末上,有无色气泡产生,由此他认为氯气与水反应产生了酸性强于碳酸的物质。请评价他的观点是否正确并说明理由_______ 。

(1)电解饱和食盐水的化学方程式是
(2)该流程中合成氯化氢的化学方程式为
某化学兴趣小组欲用下图装置制备氯水并探究其性质。

(3)烧瓶内发生的化学反应是
(4)C装置的作用是
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
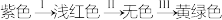
导致变色的微粒I、II、III依次为_______。
| A.H+、HClO、Cl2 | B.H+、ClO-、Cl- | C.HCl、ClO-、Cl- | D.HCl、HClO、Cl2 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
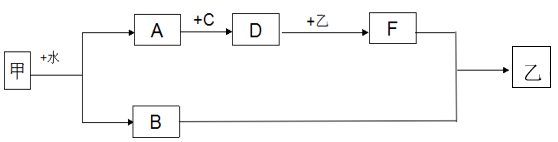
【推荐1】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠: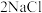 (熔融)
(熔融)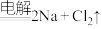 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。 化学方程式:
化学方程式:___________ 。
(2)C电离方程式___________ 。
(3)E和F生成 离子方程式
离子方程式___________ 。
(4)工业生产中常利用B与 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式___________ 。
(5)检验D溶液中含有 的方法是
的方法是___________ 。
(6)若向E溶液中继续通入 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(7)若把A投入盛有D的溶液中,写出总反应的离子方程式___________ 。
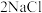 (熔融)
(熔融)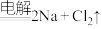 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。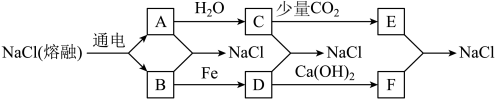
 化学方程式:
化学方程式:(2)C电离方程式
(3)E和F生成
 离子方程式
离子方程式(4)工业生产中常利用B与
 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式(5)检验D溶液中含有
 的方法是
的方法是(6)若向E溶液中继续通入
 ,写出反应的化学方程式
,写出反应的化学方程式(7)若把A投入盛有D的溶液中,写出总反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下面科普短文
世界万物是由什么形成的?这是人类自古以来就不断探索的问题。利用化学方法分析众多的物质,发现组成他们的基本成分一元素其实只有一百多种。下面介绍其中一种重要的元素一钠元素。
钠是一种活泼金属元素,其原子结构示意图为 。单质钠在空气中极易被氧化,用小刀一切,就能观察到其本来面目:银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气。目前,世界上多采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生金属钠和金属钙同时浮在共熔物表面、从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金属钠。
。单质钠在空气中极易被氧化,用小刀一切,就能观察到其本来面目:银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气。目前,世界上多采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生金属钠和金属钙同时浮在共熔物表面、从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金属钠。
金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物。还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生成钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)钠具有的物理性质有___________ 。
(2)金属钠通常保存在石蜡油中,目的是隔绝___________ 。
(3)根据钠的原子结构分析,金属钠具有___________ (填氧化性或还原性)。
(4)钠与水反应的离子方程式是___________ 。
(5)电解熔融氯化钠制取金属钠的化学方程式是___________ 。
(6)用钠制取金属钾的化学方程式是___________ 。
世界万物是由什么形成的?这是人类自古以来就不断探索的问题。利用化学方法分析众多的物质,发现组成他们的基本成分一元素其实只有一百多种。下面介绍其中一种重要的元素一钠元素。
钠是一种活泼金属元素,其原子结构示意图为
 。单质钠在空气中极易被氧化,用小刀一切,就能观察到其本来面目:银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气。目前,世界上多采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生金属钠和金属钙同时浮在共熔物表面、从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金属钠。
。单质钠在空气中极易被氧化,用小刀一切,就能观察到其本来面目:银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气。目前,世界上多采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生金属钠和金属钙同时浮在共熔物表面、从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金属钠。金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物。还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生成钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)钠具有的物理性质有
(2)金属钠通常保存在石蜡油中,目的是隔绝
(3)根据钠的原子结构分析,金属钠具有
(4)钠与水反应的离子方程式是
(5)电解熔融氯化钠制取金属钠的化学方程式是
(6)用钠制取金属钾的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某同学为了探究钠与CO2的反应,利用如图装置进行实验。
已知:①PdCl2能和CO反应生成黑色的Pd;②NaHCO3+HCl=NaCl+H2O+CO2↑

(1)装置①中用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是___________。
(2)装置②的作用是___________ ;装置③的作用是___________ 。
(3)检查完装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到___________ 时再点燃酒精灯。
(4)若反应过程中CO2足量,钠与CO2充分反应后,生成的固体物质可能有多种情况,该同学提出以下猜想;
①生成的固体物质为Na2CO3
②生成的固体物质为Na2CO3和C的混合物
③生成的固体物质为Na2CO3和Na2O的混合物
④生成的固体物质为Na2O和C的混合物
若反应过程中有下列情况:观察到装置⑤PdCl2溶液中有黑色沉淀,装置④中固体成分只有一种,且向该固体中加入稀盐酸可产生能使澄清石灰水变浑浊的气体,写出该情况下钠与CO2反应的化学方程式___________ 。
Ⅱ.比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3 。
(5)试分别写出Na2O2与SO2、SO3反应的化学方程式:___________ 、___________ 。
已知:①PdCl2能和CO反应生成黑色的Pd;②NaHCO3+HCl=NaCl+H2O+CO2↑

(1)装置①中用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是___________。
| A.H2SO4溶液 | B.NaNO3溶液 | C.煤油 | D.稀硝酸 |
(3)检查完装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到
(4)若反应过程中CO2足量,钠与CO2充分反应后,生成的固体物质可能有多种情况,该同学提出以下猜想;
①生成的固体物质为Na2CO3
②生成的固体物质为Na2CO3和C的混合物
③生成的固体物质为Na2CO3和Na2O的混合物
④生成的固体物质为Na2O和C的混合物
若反应过程中有下列情况:观察到装置⑤PdCl2溶液中有黑色沉淀,装置④中固体成分只有一种,且向该固体中加入稀盐酸可产生能使澄清石灰水变浑浊的气体,写出该情况下钠与CO2反应的化学方程式
Ⅱ.比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3 。
(5)试分别写出Na2O2与SO2、SO3反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某固体混合物由KCl、K2CO3、K2SO4和不溶于水的杂质组成。为了提纯KCl,将该混合物进行如图实验,回答相关问题:______ ,判断试剂I已加过量的方法是________ 。
(2)试剂II的化学式为______ ,②中加入试剂II的目的是________ 。
(3)试剂III的名称是______ ,③中发生反应的离子方程式为_______ 。
(4)某同学根据最终所得KCl晶体和原样品的质量求算出氯化钾样品的纯度,你认为其结果是否可靠______ ?并说明理由(不考虑实验误差)______ 。

(2)试剂II的化学式为
(3)试剂III的名称是
(4)某同学根据最终所得KCl晶体和原样品的质量求算出氯化钾样品的纯度,你认为其结果是否可靠
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组同学为验证NaHCO3受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有___ 。
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是___ 。
(3)NaHCO3受热分解的化学方程式为__ 。
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是__ 。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是
(3)NaHCO3受热分解的化学方程式为
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是
您最近一年使用:0次