目前,世界上多采用电解熔融氯化钠的方法来生产金属钠: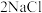 (熔融)
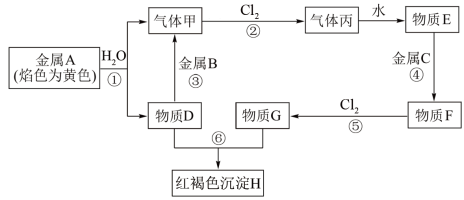
(熔融)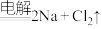 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。 化学方程式:
化学方程式:___________ 。
(2)C电离方程式___________ 。
(3)E和F生成 离子方程式
离子方程式___________ 。
(4)工业生产中常利用B与 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式___________ 。
(5)检验D溶液中含有 的方法是
的方法是___________ 。
(6)若向E溶液中继续通入 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(7)若把A投入盛有D的溶液中,写出总反应的离子方程式___________ 。
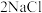 (熔融)
(熔融)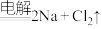 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。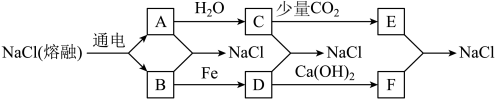
 化学方程式:
化学方程式:(2)C电离方程式
(3)E和F生成
 离子方程式
离子方程式(4)工业生产中常利用B与
 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式(5)检验D溶液中含有
 的方法是
的方法是(6)若向E溶液中继续通入
 ,写出反应的化学方程式
,写出反应的化学方程式(7)若把A投入盛有D的溶液中,写出总反应的离子方程式
更新时间:2023-12-12 19:46:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某无色、澄清溶液中可能含有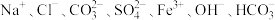 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:
已知: 。
。
(1)原溶液中肯定没有的离子是___________ ,肯定有的离子是___________ 。
(2)写出Ⅲ中发生的反应的离子方程式:___________ 。
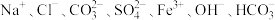 中的几种,依次进行下列实验,观察到的现象如下:
中的几种,依次进行下列实验,观察到的现象如下:| 步骤 | 操作 | 现象 |
| I | 取少量溶液,向其加入适量铝粉 | 有气体生成 |
| Ⅱ | 另取少量溶液,向其滴加足量BaCl2溶液 | 有白色沉淀生成 |
| Ⅲ | 向Ⅱ中滴加足量稀盐酸 | 沉淀部分溶解 |
 。
。(1)原溶液中肯定没有的离子是
(2)写出Ⅲ中发生的反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测的结果如表所示,请回答:
(1)三次检测结果中第_______ 次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在 、
、 和
和 (提示:
(提示: 微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的
微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的_____ (填化学式)溶液,其目的是检验 并将其除去﹔第二步加入过量的
并将其除去﹔第二步加入过量的 溶液,其目的是
溶液,其目的是______ ;第三步过滤,再向滤液中加入___ (填化学式)溶液,发生反应的离子方程式为___ 。
溶液中检测出的物质 | |
第一次 |
|
第二次 |
|
第三次 |
|
(1)三次检测结果中第
(2)在检测时,为了确定溶液中是否存在
 、
、 和
和 (提示:
(提示: 微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的
微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的 并将其除去﹔第二步加入过量的
并将其除去﹔第二步加入过量的 溶液,其目的是
溶液,其目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用单线桥法标明电子转移的方向和数目。___________
(3)次氯酸钠氧化法。

①“反应I”的离子方程式为___________ ,检验 已全部转化为
已全部转化为 的方法为
的方法为___________ 。
②副产品的成分为___________ 。
③生产过程中,理论上每获得1mol的 消耗NaClO的质量为
消耗NaClO的质量为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法。

①“反应I”的离子方程式为
 已全部转化为
已全部转化为 的方法为
的方法为②副产品的成分为
③生产过程中,理论上每获得1mol的
 消耗NaClO的质量为
消耗NaClO的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】化合物X由3种中学化学常见元素组成。某兴趣小组按如下流程进行实验:
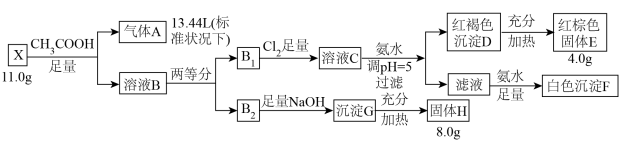
已知:①气体A是室温下密度最小的气体;②室温下,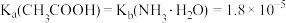 ;③G中的氢氧化物沉淀的
;③G中的氢氧化物沉淀的 分别为
分别为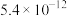 、
、 。请回答:
。请回答:
(1)NaOH的电子式是_______ 。
(2)化合物X中所含金属元素是_______ (填元素符号),其化学式为_______ 。
(3)溶液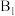 的阳离子与足量
的阳离子与足量 反应的离子方程式是
反应的离子方程式是_______ 。
(4)沉淀F会溶于浓 溶液,请计算F溶于
溶液,请计算F溶于 溶液的平衡常数
溶液的平衡常数
_______ 。关于沉淀F溶解的解释有两种:① 直接与F发生复分解反应;②
直接与F发生复分解反应;② 水解使溶液呈酸性,生成的
水解使溶液呈酸性,生成的 溶解F.请设计实验检验哪种解释是合理的:
溶解F.请设计实验检验哪种解释是合理的:_______ (写出试剂、现象与结论)。

已知:①气体A是室温下密度最小的气体;②室温下,
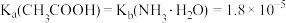 ;③G中的氢氧化物沉淀的
;③G中的氢氧化物沉淀的 分别为
分别为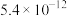 、
、 。请回答:
。请回答:(1)NaOH的电子式是
(2)化合物X中所含金属元素是
(3)溶液
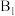 的阳离子与足量
的阳离子与足量 反应的离子方程式是
反应的离子方程式是(4)沉淀F会溶于浓
 溶液,请计算F溶于
溶液,请计算F溶于 溶液的平衡常数
溶液的平衡常数
 直接与F发生复分解反应;②
直接与F发生复分解反应;② 水解使溶液呈酸性,生成的
水解使溶液呈酸性,生成的 溶解F.请设计实验检验哪种解释是合理的:
溶解F.请设计实验检验哪种解释是合理的:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】无机化合物A和金属B是中学化学常见的固体,其中A显淡黄色。相同质量的A、B都能与液体C反应放出气体,两气体又能恰好完全反应生成C。利用B在高温下的挥发性,可通过它的碳酸盐和焦炭在真空环境中来制备B。化合物D可作为有机反应中的脱氢试剂,1molD和1mol NH4Cl反应生成2mol气体E和1molB的氯化物。已知标准状况下气体E的密度为0.76g·L-1。
请回答下列问题:
(1)E的化学式为____________
(2)题中制备B的化学方程式为____________ 下列物质能替代焦炭的是_________ 。
A.Na B.H2 C.KMnO4 D.Cl2
(3)B与E在一定条件下_________ (填“可能”或“不可能”)直接发生反应产生D,判断理由是__________________________ 。
请回答下列问题:
(1)E的化学式为
(2)题中制备B的化学方程式为
A.Na B.H2 C.KMnO4 D.Cl2
(3)B与E在一定条件下
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】(1)某研究性学习小组对“钠在空气中燃烧的产物”进行了探究。其实验过程是:取一小块钠在空气中加热片刻后与一定量的水反应,收集到VmL气体(标准状况),向所得溶液中滴入1.000mol/L的盐酸溶液30.00mL恰好中和完全(如图所示)。试回答:
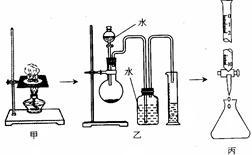
①甲、乙、丙三套装置共有________ 处错误。
②丙的操作中,若以酚酞作指示剂,滴定终点时锥形瓶内溶液颜色变化是______ 。
③若V=168mL(标准状况),在一定条件下将其引燃,恰好完全反应。请将钠块在空气中加热片刻后所得到的固体成分及其质量填表如下:(表格可不填满也可补充)
(2)其实滴定的方法有多种,除上述实验中的酸碱中和滴定外,还有沉淀滴定、络合滴定等。沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂和被滴定物的生成物的溶解度要比滴定剂和指示剂生成物的溶解度_____ (填“大”、“小”、“相同”),否则不能用这种指示剂。如用AgNO3溶液滴定溶液中的Cl-的含量时常以CrO42-为指示剂,这是因为AgCl比Ag2CrO4更____ 溶的缘故。

①甲、乙、丙三套装置共有
②丙的操作中,若以酚酞作指示剂,滴定终点时锥形瓶内溶液颜色变化是
③若V=168mL(标准状况),在一定条件下将其引燃,恰好完全反应。请将钠块在空气中加热片刻后所得到的固体成分及其质量填表如下:(表格可不填满也可补充)
| 成分 | |||
| 质量/g |
(2)其实滴定的方法有多种,除上述实验中的酸碱中和滴定外,还有沉淀滴定、络合滴定等。沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂和被滴定物的生成物的溶解度要比滴定剂和指示剂生成物的溶解度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硼氢化钠(NaBH4)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃)。工业上可用硼镁矿(主要成分为Mg2B2O5·H2O,含少量杂质Fe3O4)制取NaBH4,其工艺流程如下:
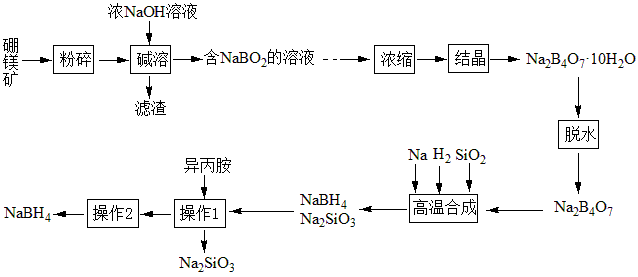
回答下列问题:
(1)碱溶时Mg2B2O5发生反应的化学方程式是___________ ,高温合成的化学方程式___________ 。
(2)滤渣的成分是___________ 。
(3)高温合成中,加料之前需将反应器加热至100℃以上并通入氩气,该操作的目的是___________ ,实验室取用少量金属钠用到的实验用品有___________ 、滤纸、玻璃片和小刀。
(4)操作2的名称为___________ 。流程中可循环利用的物质是___________ 。
(5)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1g NaBH4的还原能力相当于___________ g H2的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同,结果保留两位小数)。

回答下列问题:
(1)碱溶时Mg2B2O5发生反应的化学方程式是
(2)滤渣的成分是
(3)高温合成中,加料之前需将反应器加热至100℃以上并通入氩气,该操作的目的是
(4)操作2的名称为
(5)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1g NaBH4的还原能力相当于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】中国沿海某城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。某实验小组同学模拟工业生产流程,进行如下实验。
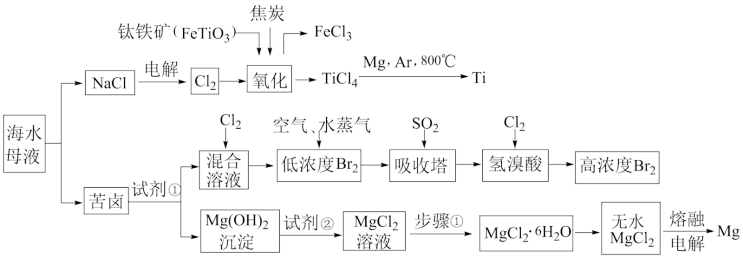
回答下列问题:
(1)海水淡化的方法还有___________ (写出一种)。
(2)吸收塔中反应的化学方程式是___________ 。
(3)步骤①包括___________ 、冷却结晶、过滤。
(4)工业上用电解法制取金属镁,用___________ 方法获得金属汞和银。
(5)若要验证所得无水MgCl2中不含NaCl,最简单的方法是___________ 。
(6)写出钛铁矿在高温下经氧化得到四氯化钛的化学方程式___________ 。
(7)由TiCl4→Ti需要在Ar气中进行的理由是___________ 。

回答下列问题:
(1)海水淡化的方法还有
(2)吸收塔中反应的化学方程式是
(3)步骤①包括
(4)工业上用电解法制取金属镁,用
(5)若要验证所得无水MgCl2中不含NaCl,最简单的方法是
(6)写出钛铁矿在高温下经氧化得到四氯化钛的化学方程式
(7)由TiCl4→Ti需要在Ar气中进行的理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】金属钛具有密度小、强度高、耐腐蚀、无毒等优点,已广泛应用于航空航天工业,并逐步进入了化工、船舶、汽车、体育器材、医疗等民用领域,并显示出了巨大的发展潜力。还原法是工业上冶炼钛常用方法之一,该方法是以金红石(主要含TiO2)为原料来制取,其主要工艺流程如下:

试回答下列问题:
(1)已知反应①通常在800~900 ℃的条件下进行,产物中有一种可燃性无色气体,其中当有1 mol Cl2完全反应时,参加反应的还原剂的物质的量为________ mol。
(2)反应②通常在800 ℃的条件下进行,通入氩气的目的是______________________ ;分离反应②的产物所得到的海绵钛中常混有少量杂质,应如何除去杂质?_______________________ (简述操作过程)。
(3)在上述工艺流程中可以循环使用的物质有________ 。

试回答下列问题:
(1)已知反应①通常在800~900 ℃的条件下进行,产物中有一种可燃性无色气体,其中当有1 mol Cl2完全反应时,参加反应的还原剂的物质的量为
(2)反应②通常在800 ℃的条件下进行,通入氩气的目的是
(3)在上述工艺流程中可以循环使用的物质有
您最近一年使用:0次
【推荐3】海水中含有丰富的Na+、Mg2+、Cl-、Br-等化学资源。将海水淡化与浓缩海水结合是综合利用海水资源的途径之一。以浓缩海水为原料,通过一系列工艺流程可以提取Mg、Br2等产品。
(1)如图是采用膜分离技术的海水淡化示意图。

淡化膜可以让水分子通过,而海水中其他分子和离子均不能通过。加压后,左侧淡水中增加的是__________ (填字母)。
a.溶质质量 b.溶剂质量 c.溶质的质量分数
(2)从海水中提取镁的主要步骤如下:

①操作a的名称是_______________ 。
②写出B冶炼金属镁的化学方程式_______________________________ 。
(3)空气吹出法是用于工业规模海水提溴的常用方法,其中一种工艺是以预先经过酸化的浓缩海水为原料,通过以下步骤提取溴:
步骤一:用氯气置换溴离子使之成为单质溴;
步骤二:通入空气和水蒸气,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用转化成氢溴酸;
步骤三:用氯气将氢溴酸氧化得到产品溴。
①步骤一和步骤二的目的是___________________________________ 。
②步骤二中发生反应的化学方程式为___________________________ 。
(1)如图是采用膜分离技术的海水淡化示意图。

淡化膜可以让水分子通过,而海水中其他分子和离子均不能通过。加压后,左侧淡水中增加的是
a.溶质质量 b.溶剂质量 c.溶质的质量分数
(2)从海水中提取镁的主要步骤如下:

①操作a的名称是
②写出B冶炼金属镁的化学方程式
(3)空气吹出法是用于工业规模海水提溴的常用方法,其中一种工艺是以预先经过酸化的浓缩海水为原料,通过以下步骤提取溴:
步骤一:用氯气置换溴离子使之成为单质溴;
步骤二:通入空气和水蒸气,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用转化成氢溴酸;
步骤三:用氯气将氢溴酸氧化得到产品溴。
①步骤一和步骤二的目的是
②步骤二中发生反应的化学方程式为
您最近一年使用:0次

 、
、 、
、 、
、 、
、 、
、