I.元素在周期表中的位置反映了元素的原子结构和性质。请回答下列有关硼(B)元素的问题:
(1)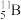 原子核内的中子数为
原子核内的中子数为________ 。
(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为___________ 。
(3)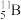 的原子半径比
的原子半径比 的原子半径
的原子半径__________ (填“大”或“小”)。
(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性_______ (填“强”或“弱”)。
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
请回答下列问题:
(1)元素②的原子结构示意图是_______________ 。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为_________ (填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为___________________ 。
(4)⑧与⑩两种元素非金属较强的是_______ (填元素符号)。
(1)
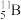 原子核内的中子数为
原子核内的中子数为(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为
(3)
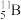 的原子半径比
的原子半径比 的原子半径
的原子半径(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)元素②的原子结构示意图是
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为
(4)⑧与⑩两种元素非金属较强的是
20-21高二·全国·单元测试 查看更多[1]
(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)
更新时间:2021-03-09 10:19:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】表是元素周期表的一部分,试回答下列问题。

我们常用电负性来衡量元素在化合物中吸引电子的能力。电负性越大,吸引电子能力越强。
(1)上述8种元素中,电负性最小的元素是_______ 。(用元素符号回答)
(2)表中元素⑦、⑧的最高价氧化物对应的水化物酸性由强到弱的顺序是:_______ 。(用化学式回答)
(3)表中元素①、③可形成一种摩尔质量为19g·mol-1的离子化合物X,则X的电子式为_______ 。

我们常用电负性来衡量元素在化合物中吸引电子的能力。电负性越大,吸引电子能力越强。
(1)上述8种元素中,电负性最小的元素是
(2)表中元素⑦、⑧的最高价氧化物对应的水化物酸性由强到弱的顺序是:
(3)表中元素①、③可形成一种摩尔质量为19g·mol-1的离子化合物X,则X的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
(1)m的阴离子的结构示意图为___ 。
(2)b的最高价氧化物的化学式为___ ;用化学方程式表示f、d的单质形成f2d2的过程___ 。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___ (用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
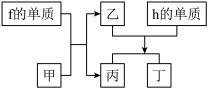
请写出h的单质与乙反应的化学方程式:___ 。
| a | ||||||||
| b | c | d | e | |||||
| f | g | h | m | n | ||||
| …… |
(2)b的最高价氧化物的化学式为
(3)d、g、n形成的简单离子的半径由大到小的顺序为
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。

请写出h的单质与乙反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,用化学用语回答下列问题:
(1)①-⑩号元素中元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ (均用化学式表示)。
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为_______ (用离子符号和“>”表示)。
(3)②与④可以形成一种温室气体,用电子式表示其形成过程_______ 。
(4)由①③⑩三种元素形成的一种离子化合物的电子式_______ 。
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 4 |
(2)④⑤⑥⑦的简单离子半径由大到小的顺序为
(3)②与④可以形成一种温室气体,用电子式表示其形成过程
(4)由①③⑩三种元素形成的一种离子化合物的电子式
(5)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸性
(6)表中③和⑤可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构简式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知X、Y、Z、W、Q是原子序数依次增大的前四周期元素。X原子核外有6种不同运动状态的电子;Y基态原子中s电子总数与p电子总数相等;Z最高价氧化物对应水化物的碱性在同周期元素中最强;W基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反。
(1)基态X原子中电子占据的最高能级的原子轨道形状为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为_______ 。
(2)Y、Z、W的简单离子半径由大到小的顺序为_______ 。(用离子符号表示)
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为_______ 。
②检验溶液中是否含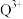 离子的试剂是
离子的试剂是_______ (填化学式),现象为_______ 。
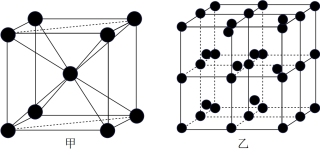
③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是_______ (填字母序号)。
A.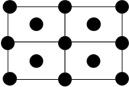 B.
B.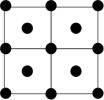 C.
C.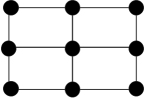 D.
D.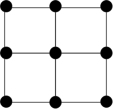
(1)基态X原子中电子占据的最高能级的原子轨道形状为
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为(2)Y、Z、W的简单离子半径由大到小的顺序为
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为
②检验溶液中是否含
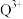 离子的试剂是
离子的试剂是③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是

A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,每个编号代表种元素, 请按要求回答问题:
(1)③和④元素的原子半径较小的是_______ (填元素符号);
(2)⑤和⑥的氢化物更稳定的是_______ (填氢化物的化学式);
(3)①~⑥形成的单质中,既能和盐酸反应又能和NaOH溶液反应的是_______ (填化学式);
(4)常温下,④的气态氢化物的水溶液能使湿润的红色石蕊试纸变_______ 色;
| 族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ③ | ④ | ⑤ | ||||||
| 3 | ① | ② | ⑥ |
(2)⑤和⑥的氢化物更稳定的是
(3)①~⑥形成的单质中,既能和盐酸反应又能和NaOH溶液反应的是
(4)常温下,④的气态氢化物的水溶液能使湿润的红色石蕊试纸变
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】为纪念Dmitri Mendeleev(德米特里·门捷列夫)编制的元素周期表诞生150周年,联合国大会宣布2019年为“国际化学元素周期表年”(TYPT2019)。下图是元素周期表的一部分,根据表中①-⑩元素,请按要求回答下列问题。
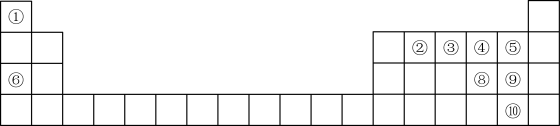
(1)元素③在周期表中的位置___________ 。
(2)原子半径:⑥___________ ⑧(填“>”、“<”或“=”,下同),比较简单氢化物的热稳定性:④___________ ⑧。
(3)①-⑩元素的最高价氧化物的水化物碱性最强的是___________ (填化学式),酸性最强的是___________ (填化学式)。
(4)②的单质与⑧的最高价氧化物的水化物的浓溶液反应的化学方程式___________ 。

(1)元素③在周期表中的位置
(2)原子半径:⑥
(3)①-⑩元素的最高价氧化物的水化物碱性最强的是
(4)②的单质与⑧的最高价氧化物的水化物的浓溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】结合元素周期表回答下列问题:已知表中的实线是元素周期表的部分边界,a位于周期表第一周期第IA族。
(1)b、c、d单质密度由大到小的顺序为___ (填化学式),b、c、d最高价氧化物的水化物(即对应碱)的碱性由强到弱的顺序___ (填化学式),d对应的氧化物有___ 。(填化学式)
(2)h的原子结构示意图为___ ,f在周期表中的位置___ 。
(3)n的单质置换出r的单质的离子方程式___ 。
(4)m的氢化物在t的单质中充分燃烧的化学方程式___ 。
(5)已知砷(As)的氢化物的化学式为AsH3,则As和___ (填字母)在同一主族。
| a | |||||||||||||||||
| b | t | ||||||||||||||||
| c | e | h | i | x | m | n | p | ||||||||||
| d | f | r | |||||||||||||||
(2)h的原子结构示意图为
(3)n的单质置换出r的单质的离子方程式
(4)m的氢化物在t的单质中充分燃烧的化学方程式
(5)已知砷(As)的氢化物的化学式为AsH3,则As和
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是元素周期表的一部分:
Ⅰ.用化学用语 回答下列问题:
(1)①、②、⑥形成的化合物中存在的化学键类型有________ 。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。
(3)写出②的离子结构示意图为__________ 。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______ 。
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途_____ ;
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式_____ ,A和C反应的离子方程式 ___ 。
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是________ ;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式_________ 。
| ① | |||||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ② | ③ | ⑦ | ⑧ | ||||||||||||||
| Fe | |||||||||||||||||
(1)①、②、⑥形成的化合物中存在的化学键类型有
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)写出②的离子结构示意图为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
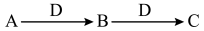
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图,在1~18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
(1)写出A元素的名称 _______ ;写出D元素的符号_______ ;
(2)画出E的原子结构示意图_______ ;
(3)写出C的最高价氧化物的化学式_______ ;
(4)F的最高价氧化物的水化物的化学式是_______ ;
(5)C、E、F三种元素相比较,非金属性最强的是_______ (填元素符号)表中原子半径最大的是_______ (填元素符号);
(6)B单质与A的最高价氧化物的水化物反应的离子方程式:_______ 。
C | D | |||||||
A | B | E | F | |||||
(2)画出E的原子结构示意图
(3)写出C的最高价氧化物的化学式
(4)F的最高价氧化物的水化物的化学式是
(5)C、E、F三种元素相比较,非金属性最强的是
(6)B单质与A的最高价氧化物的水化物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表列出了9种元素在元素周期表(元素周期表中给出部分)中的位置。
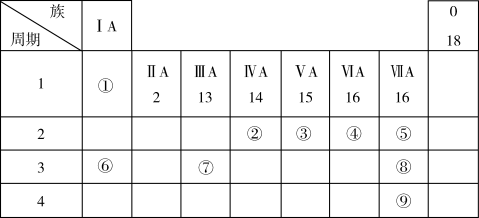
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的符号是_______ 。
(2)画出元素⑧形成的简单离子的结构示意图:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)③、④、⑤二种元素的简单气态氢化物,稳定性顺序是_______ (填化学式,用“>”连接)。
(5)元素③的氢化物与氯化氢形成的盐中的化学键类型为_______ (填“极性共价键”“离子键”或“非极性共价键”)。
(6)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断_______ (填“正确”或者“错误”);根据元素周期律,自然界中最强的碱是_______ (填“化学式”);元素④与元素①形成的原子个数比为1:2的化合物沸点高的原因是_______ 。
(7)通常所说的“芯片”是指集成电路,它是微电子技术的主要产品,制造芯片的核心元素在周期表中的位置是_______ 。

请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤二种元素的简单气态氢化物,稳定性顺序是
(5)元素③的氢化物与氯化氢形成的盐中的化学键类型为
(6)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断
(7)通常所说的“芯片”是指集成电路,它是微电子技术的主要产品,制造芯片的核心元素在周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
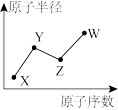
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___ ,说明理由__________________________________ 。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________ ;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________ 。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________ ,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________ 。(写出有关反应的化学方程式)

(1)写出四种元素的元素符号:X
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
请回答下列问题:(用对应的化学用语回答)
(1)B在元素周期表中的位置是___________ ;A和C形成供氧剂的电子式___________ 。
(2) A、C、D、E离子半径由小到大的顺序为___________ 。(用离子符号表示)
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:___________ 。
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:___________ 。
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为___________ 。
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:___________ 。
| 元素 | 原子结构或性质 |
| A | 原子的最外层电子数是电子层数的 ,其含氧化合物可作为供氧剂 ,其含氧化合物可作为供氧剂 |
| B | 其形成的一种同位素原子在考古中可推测化石的年代 |
| C | 地壳中含量最多的元素 |
| D | 其单质位于火山口附近 |
| E | 与D同周期,且最外层电子数等于电子层数 |
| F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
(1)B在元素周期表中的位置是
(2) A、C、D、E离子半径由小到大的顺序为
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:
您最近一年使用:0次



