利用下列装置进行过氧化钠与二氧化碳反应,并收集反应生成的气体。
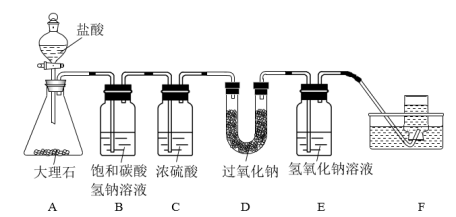
请回答下列问题:
(1)写出D中发生反应的化学方程式____ 。
(2)装置B的作用是___ ,有关反应的离子方程式为___ 。
(3)装置E的作用是___ 。

请回答下列问题:
(1)写出D中发生反应的化学方程式
(2)装置B的作用是
(3)装置E的作用是
更新时间:2021/03/14 22:37:11
|
【知识点】 过氧化钠和二氧化碳反应解读
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】如图所示,“二氧化碳是否在有水存在时,才能与过氧化钠反应?”这个问题可通过以下实验加以证明。
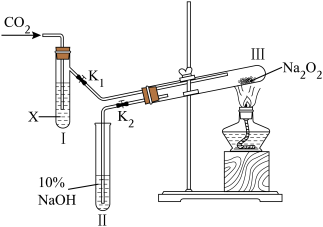
(1)按图装置,在干燥的试管Ⅲ中装入Na2O2后,在通入CO2之前,应事先将活塞(K1、K2)关闭好,目的是____________
(2)试管Ⅰ内的试剂X是________ 时,打开活塞K1、K2,加热试管Ⅲ约5分钟后,将带火星的小木条插入试管Ⅱ的液面上,可观察到带火星的小木条不能剧烈地燃烧起来,且Ⅲ内淡黄色粉末未发生变化。则所得的结论是____________________
(3)试管Ⅰ内试剂为CO2饱和水溶液时,其它操作同(2),通过________ 的现象,可以证明Na2O2与潮湿的CO2能反应且放出O2。
(4)写出 Na2O2与CO2反应的化学方程式___________

(1)按图装置,在干燥的试管Ⅲ中装入Na2O2后,在通入CO2之前,应事先将活塞(K1、K2)关闭好,目的是
(2)试管Ⅰ内的试剂X是
(3)试管Ⅰ内试剂为CO2饱和水溶液时,其它操作同(2),通过
(4)写出 Na2O2与CO2反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】侯德榜是我国近代著名的化工学家,为我国化工事业的发展做出了卓越的贡献,其贡献之一是发明了联合制碱法(即侯氏制碱法),该法先制备出NaHCO3再受热分解生成纯碱,如图是NaHCO3分解及CO2与Na2O2反应的实验。回答下列问题:
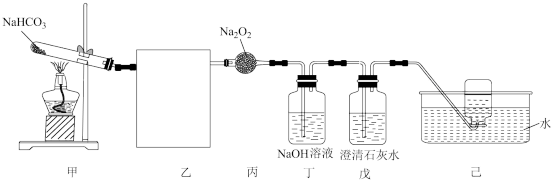
(1)侯氏制碱法的原料是饱和食盐水、CO2、NH3,写出侯氏制碱法中生成NaHCO3的离子方程式:____ 。
(2)装置乙为___ (填标号)。
a.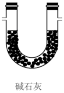 b.
b. 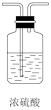 c.
c. 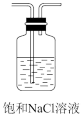 d.
d.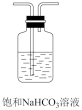
(3)装置丙的名称是___ ,其中反应的化学方程式是___ ,该反应中氧化剂与还原剂的质量比为___ 。
(4)装置丁中NaOH溶液的作用是___ ,装置戊中澄清石灰水的作用是___ 。
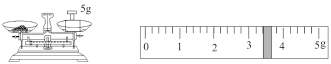
(5)装置甲中用托盘天平称取的NaHCO3的质量如图,则理论上装置乙中收集的气体体积在标准状况下为___ L。

(1)侯氏制碱法的原料是饱和食盐水、CO2、NH3,写出侯氏制碱法中生成NaHCO3的离子方程式:
(2)装置乙为
a.
 b.
b.  c.
c.  d.
d.
(3)装置丙的名称是
(4)装置丁中NaOH溶液的作用是
(5)装置甲中用托盘天平称取的NaHCO3的质量如图,则理论上装置乙中收集的气体体积在标准状况下为

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】完成下列题目。
Ⅰ.实验室欲配制稀盐酸,用到的浓盐酸标签上的数据如下
(1)某学生欲用上述浓盐酸和蒸馏水配制485mL物质的量浓度为0.1mol/L的稀盐酸,需要量取_______ mL上述浓盐酸。(保留到小数点后一位有效数字)
(2)实验过程中用到的玻璃仪器有:烧杯、量筒、试剂瓶、玻璃棒、_______ 、_______ 。
(3)以下操作会使所配溶液浓度偏低的是_______ (填序号)
a.容量瓶使用时瓶内有少量残留的蒸馏水;
b.用量筒量取浓盐酸时视线仰视刻度线;
c.定容时视线仰视刻度线。
Ⅱ.某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
(4)装置②中的试剂是_______ ,
装置⑥中碱石灰的作用是_______ 。
【进行实验】
步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(5)步骤1和步骤2中,a处带火星的木条复燃的是_______ (填步骤1或步骤2)
(6)写出过氧化钠跟二氧化碳反应的化学方程式并用双线桥标出电子转移:_______ 。
Ⅲ.已知:①碳酸钠高温不分解;②碳酸氢钠受热易发生分解反应。充分加热碳酸钠和碳酸氢钠的混合物24.3g,完全反应后固体质量减轻了3.1g,求:
(7)原混合物中碳酸钠的质量是_______ g。
(8)将剩余固体溶于水配成2L溶液,其中 是
是_______ 。
Ⅰ.实验室欲配制稀盐酸,用到的浓盐酸标签上的数据如下
| 盐酸 分子式 HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(1)某学生欲用上述浓盐酸和蒸馏水配制485mL物质的量浓度为0.1mol/L的稀盐酸,需要量取
(2)实验过程中用到的玻璃仪器有:烧杯、量筒、试剂瓶、玻璃棒、
(3)以下操作会使所配溶液浓度偏低的是
a.容量瓶使用时瓶内有少量残留的蒸馏水;
b.用量筒量取浓盐酸时视线仰视刻度线;
c.定容时视线仰视刻度线。
Ⅱ.某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。

(4)装置②中的试剂是
装置⑥中碱石灰的作用是
【进行实验】
步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。(5)步骤1和步骤2中,a处带火星的木条复燃的是
(6)写出过氧化钠跟二氧化碳反应的化学方程式并用双线桥标出电子转移:
Ⅲ.已知:①碳酸钠高温不分解;②碳酸氢钠受热易发生分解反应。充分加热碳酸钠和碳酸氢钠的混合物24.3g,完全反应后固体质量减轻了3.1g,求:
(7)原混合物中碳酸钠的质量是
(8)将剩余固体溶于水配成2L溶液,其中
 是
是
您最近一年使用:0次



