已知NA是阿伏加德罗常数的值,下列说法正确的是
| A.常温下1 L pH=13的氢氧化钠溶液中由水电离出的H+的数目为0.1NA |
| B.4.6g14CO2与N218O的混合物中所含中子数为2.4NA |
| C.标准状况下,NA个SO3分子所占的体积约为22.4 L |
| D.0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2 NA |
更新时间:2021-03-15 21:18:29
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】下列关于0.5mol·L-1Ba(NO3)2溶液叙述中,不正确的是( )
| A.2L该溶液中含NA个Ba2+ |
| B.1L该溶液中所含阴阳离子总数为1.5NA |
| C.1L该溶液中Ba2+的物质的量浓度是0.5mol·L-1 |
D.0.5L该溶液中 的物质的量浓度是0.5mol·L-1 的物质的量浓度是0.5mol·L-1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列叙述中正确的是
| A.常温下,23gNO2含有NA个氧原子 |
| B.1mol Fe溶于过量的浓硝酸,电子转移数为2NA |
C.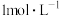 Na2SO4溶液中,阴、阳离子总数为3NA Na2SO4溶液中,阴、阳离子总数为3NA |
| D.10 g质量分数为46%的乙醇溶液中所含氧原子的总数为0.4NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】设阿伏加 德罗常数(NA)的数值为NA,下列说法正确的是
| A.58.5g氯化钠中含有6.02×1023个氯化钠分子 |
| B.1.5 mol NO2与足量H2O反应,转移的电子数为NA |
| C.14g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
| A.标准状况下,22.4LH2S与22.4LH2O中所含的分子数均为NA |
| B.由6.2gNa2O与7.8gNa2O2组成的混合物中阴离子总数为0.2NA |
| C.10g49%的硫酸溶液与10g49%的H3PO4溶液中所含的氧原子数均为0.48NA |
| D.0.1molFe分别与足量的盐酸和氯气反应,转移的电子数均为0.2NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法不正确的是
| A.测得0.1mol·L-1的一元酸HA溶液pH=3,则HA一定为强电解质 |
| B.25℃时将0.1mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11 |
| C.25℃时将0.1mol·L-1的HA溶液加水稀释至pH=4,所得溶液c(OH-)=1×10-10mol·L-1 |
| D.0.1mol·L-1的HA溶液与0.1mol·L-1的NaOH溶液等体积混合,所得溶液pH一定等于7 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.电镀池镀铜,当阴极产生3.2g铜时,理论上转移的电子数为 |
B.常温下,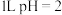 的HF溶液中含有的 的HF溶液中含有的 数目为 数目为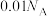 |
C.一定条件下,2mol硫蒸气与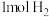 反应生成 反应生成 的分子数为 的分子数为 |
D.常温下,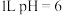 的 的 溶液中水电离出的 溶液中水电离出的 数目为 数目为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】下列判断正确的是


| A.图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线 |
| B.图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线 |
| C.高温下能自发进行的反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔH>0 |
| D.图4可表示反应N2(g)+3H2(g)⇌2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线 |
您最近一年使用:0次

 和
和 中所含原子总数为
中所含原子总数为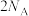
 与足量
与足量 反应转移电子总数为
反应转移电子总数为
 制得的
制得的 胶体粒子数为
胶体粒子数为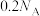
 和
和 混合气体含氧原子数为
混合气体含氧原子数为 中,含有0.6NA个中子
中,含有0.6NA个中子

