室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中 的值减小 的值减小 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10mLpH=11的NaOH溶液,混合液pH=7 |
更新时间:2021-03-17 10:37:57
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
| A.室温下,某溶液由水电离出来的H+的浓度为1.0×10-10 mol·L-1,则该溶液的pH=4 |
| B.100 ℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| C.一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1 |
D.25 ℃时,c(H+)=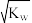 mol·L-1=1.0×10-7 mol·L-1的溶液一定呈中性 mol·L-1=1.0×10-7 mol·L-1的溶液一定呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,等体积的下列各组酸和碱的溶液混和后,溶液pH<7的是
①pH之和为14的硝酸和氢氧化钾溶液; ②pH之和为15的盐酸和氨水溶液;
③pH之和为14的醋酸和苛性钠溶液; ④pH之和为13的硫酸和氢氧化钡溶液。
①pH之和为14的硝酸和氢氧化钾溶液; ②pH之和为15的盐酸和氨水溶液;
③pH之和为14的醋酸和苛性钠溶液; ④pH之和为13的硫酸和氢氧化钡溶液。
| A.② | B.①② | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.常温下,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液的pH>7 |
| B.1 mL浓氨水加水稀释至1000 mL后,溶液中所有离子浓度都减小 |
| C.PH=2的醋酸溶液,加水稀释1000倍后,PH<5 |
| D.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 |
| B.常温下,将pH= 4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.0.1 mol·L-1Na2S溶液:2c(Na+) =c(S2-)+c(HS-) +c(H2S) |
| D.对于Ca(OH)2的沉淀溶解平衡,升高温度,Ca(OH)2的溶解速率增大,Ksp减小 |
您最近一年使用:0次




