按要求填空:
(1)写出钠与水反应的离子方程式:___________ 。
(2)过氧化钠的颜色为:___________ ,其阳离子和阴离子的个数比为___________ ,写出过氧化钠与水反应的化学方程式:___________ 。
(3)写出氯的原子结构示意图:___________ , 写出工业制漂白粉的化学方程式:___________ 。
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:___________ 。
(1)写出钠与水反应的离子方程式:
(2)过氧化钠的颜色为:
(3)写出氯的原子结构示意图:
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:
更新时间:2021-03-22 11:59:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式____ ,将54.8g Na2CO3和NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L,另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=____ ,气体V=____ 。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为____ ,若有2mol氯气参与该反应,则此时转移的电子数为____ NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为____ 。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为____ 。
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为____ g(请保留两位小数)。
(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为
| 9 | 白球比 | 1.6 | |
| 10 | 乳酸脱氢酶 | 161 | U/L |
| 11 | 磷酸肌酸激酶 | 56 | U/L |
| 12 | 甘油三酯 | 0.52 | mmol/L |
| 13 | 总胆固醇 | 4.27 | mmol/L |
| 14 | 高密度脂蛋白胆固醇 | 1.57 | mmol/L |
| 15 | 低密度脂蛋白胆固醇 | 1.40 | mmol/L |
| 16 | 葡萄糖 | 4.94 | mmol/L |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)在新制氯水中加入紫色石蕊试液的现象是_______ 。
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石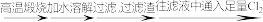 漂白粉溶液
漂白粉溶液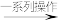 漂白粉
漂白粉
制取漂白粉溶液的过程中,发生反应的化学方程式为_______ 。漂白粉失效的化学方程式为_______ 。
(3)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是_______ 。
(4)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是_______ 。向反应后的集气瓶中加入适量的蒸馏水,振荡,观察到的现象是_______ 。
(1)在新制氯水中加入紫色石蕊试液的现象是
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石
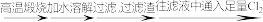 漂白粉溶液
漂白粉溶液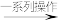 漂白粉
漂白粉制取漂白粉溶液的过程中,发生反应的化学方程式为
(3)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是
(4)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠、氯及其化合物有如图转化关系,请按要求填空:
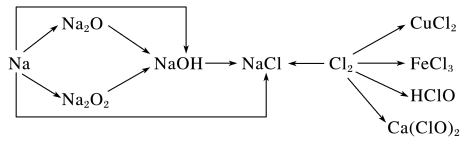
(1)金属钠的密度比水______ ,实验室中金属钠通常保存在______ 中。一小块金属钠投入水中的反应方程式是______ 。
(2)Na2O2是______ 色的固体,Na2O2的重要用途是______ ,有关反应的化学方程式为______ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为_____ 。
(4)新制的氯水滴入AgNO3溶液中,观察到______ 现象,原因是______ 。
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是____ ,漂白粉长时期露至在空气中会失效,用化学方程式表示其失效的原因:____ ,____ 。

(1)金属钠的密度比水
(2)Na2O2是
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为
(4)新制的氯水滴入AgNO3溶液中,观察到
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组设计了一组实验,验证元素周期律。
甲同学在a、b、c、d四只烧杯里分别加入50mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性_______ ;
(2)反应最剧烈的烧杯里金属是_____ (填字母)
(3)写出a烧杯里发生反应的离子方程式_______ 。
(4)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法 。
(5)写出铝和盐酸反应的化学方程式_______ 。
甲同学在a、b、c、d四只烧杯里分别加入50mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性
(2)反应最剧烈的烧杯里金属是_____ (填字母)
| A.钠 | B.镁 | C.铝 | D.钾; |
(4)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法 。
| A.把镁、铝的金属块换成金属粉末 |
| B.把烧杯中的冷水换成热水 |
| C.把烧杯中的冷水换成盐酸 |
| D.把烧杯中的冷水换成氢氧化钠溶液 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,请回答下列问题:
(1)写出下列元素符号:⑤________ ,⑥________ 。
(2)在这些元素中(表中①~⑧),最活泼的金属元素是__________ (填元素符号,下同),最活泼的非金属元素是______ ,最不活泼的元素是________ 。
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是________ (填化学式),碱性最强的是________ (填化学式),原子半径最小的是________ (填元素符号)。
(4)在③与④中,化学性质较活泼的是________ (填元素符号),怎样用化学实验证明?
(简述方法即可)___________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)写出下列元素符号:⑤
(2)在这些元素中(表中①~⑧),最活泼的金属元素是
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是
(4)在③与④中,化学性质较活泼的是
(简述方法即可)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.下列各组化学反应中,盐酸均是反应物。
(1)利用盐酸的氧化性的是(填编号,下同)___________ ;
(2)利用盐酸的还原性的是___________ ;
(3)仅利用盐酸的酸性的是___________ ,既利用还原性又利用酸性的是___________ 。
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②2HCl+2Na=2NaCl+H2↑
③CaCO3+2HCl=CaCl2+H2O+CO2↑
Ⅱ.钠是一种活泼金属,其化合物在生产生活中具有广泛应用。
(4)下列有关钠及其化合物的说法正确的是___________。
(5)Na2O2因能与CO2反应可作潜水艇的供氧剂,涉及的反应方程式为__________ 。
(1)利用盐酸的氧化性的是(填编号,下同)
(2)利用盐酸的还原性的是
(3)仅利用盐酸的酸性的是
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O ②2HCl+2Na=2NaCl+H2↑
③CaCO3+2HCl=CaCl2+H2O+CO2↑
Ⅱ.钠是一种活泼金属,其化合物在生产生活中具有广泛应用。
(4)下列有关钠及其化合物的说法正确的是___________。
| A.少量钠保存在酒精中 | B.Na2O2是白色固体,性质不稳定 |
C.热稳定性: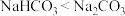 | D. 常用来治疗胃酸过多 常用来治疗胃酸过多 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请写出符合要求的化学方程式。(配平,注意反应条件)
(1)写出一个直接由SO2转化成H2SO4的化学方程式:_________ ;
(2)过氧化钠和二氧化碳气体反应:________ ;
(3)电解饱和食盐水:_______ ;
(4)浓硫酸和碳在加热条件下反应:________ ;
(5)铁粉和硫单质在加热条件下反应:_______ ;
(6)金属镓(元素符号为Ga)与铝元素同主族,两者化学性质非常相似。请写出镓与氢氧化钠溶液反应的化学方程式:_______ ;
(7)CaSO3固体长时间放置在空气中容易变质,请用化学方程式表示其过程:_____ ;
(1)写出一个直接由SO2转化成H2SO4的化学方程式:
(2)过氧化钠和二氧化碳气体反应:
(3)电解饱和食盐水:
(4)浓硫酸和碳在加热条件下反应:
(5)铁粉和硫单质在加热条件下反应:
(6)金属镓(元素符号为Ga)与铝元素同主族,两者化学性质非常相似。请写出镓与氢氧化钠溶液反应的化学方程式:
(7)CaSO3固体长时间放置在空气中容易变质,请用化学方程式表示其过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题:
(1)用氧化物的形式表示硅酸盐的组成,钙沸石Ca(Al2Si3O10)·3H2O表示为___ 。
(2)氢氟酸可刻蚀玻璃,反应的化学方程式为___ 。
(3)工业上使用漂白粉时常向其中加入稀盐酸,化学方程式为___ 。
(4)将钠、镁、铝各0.4mol分别放入100mL1mol/L的盐酸中,同温同压下产生的气体体积比为___ 。
(5)向20mL含有1mol/L的氯化铝和一定量盐酸的溶液中逐滴加入浓度为1mol/L的氢氧化钠溶液,产生沉淀的质量与所加碱的体积如图所示,若由于碱过量 ,最终产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积是___ mL。

(6)将物质的量之比为2:3:4的N2、O2、CO2混合气体通过一定量Na2O2后,气体体积变为原体积的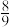 (同温同压),这时混合气体中N2、O2、CO2物质的量之比为
(同温同压),这时混合气体中N2、O2、CO2物质的量之比为___ 。
(1)用氧化物的形式表示硅酸盐的组成,钙沸石Ca(Al2Si3O10)·3H2O表示为
(2)氢氟酸可刻蚀玻璃,反应的化学方程式为
(3)工业上使用漂白粉时常向其中加入稀盐酸,化学方程式为
(4)将钠、镁、铝各0.4mol分别放入100mL1mol/L的盐酸中,同温同压下产生的气体体积比为
(5)向20mL含有1mol/L的氯化铝和一定量盐酸的溶液中逐滴加入浓度为1mol/L的氢氧化钠溶液,产生沉淀的质量与所加碱的体积如图所示,若由于

(6)将物质的量之比为2:3:4的N2、O2、CO2混合气体通过一定量Na2O2后,气体体积变为原体积的
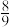 (同温同压),这时混合气体中N2、O2、CO2物质的量之比为
(同温同压),这时混合气体中N2、O2、CO2物质的量之比为
您最近一年使用:0次



