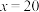葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通常以酒样中SO2的量计),某研究小组设计了如下实验(已知还原性: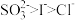 ):下列说法不正确的是
):下列说法不正确的是
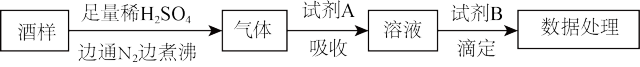
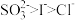 ):下列说法不正确的是
):下列说法不正确的是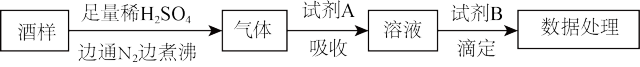
| A.葡萄酒中加亚硫酸盐的主要目的是作抗氧化剂,利用了亚硫酸盐的还原性 |
| B.通入N2和煮沸的目的是为了将产生的气体从溶液中全部驱赶出 |
| C.试剂A选择氯水,试剂B可选择NaOH标准液 |
| D.试剂A选择碱液,调节吸收后溶液至中性,试剂B选择标准I2液 |
16-17高三上·北京海淀·期末 查看更多[21]
北京一零一中学2023-2024学年上学期11月高二统练三化学试题(已下线)题型39 酸碱中和滴定北京市中国人民大学附属中学2019-2020学年高三上学期9月质检化学试题北京市中国人民大学附属中学2020届高三化学质检试题(已下线)第11讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第12练 硫及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)湖南师范大学附属中学2019-2020学年高二下学期期中考试化学试题(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)黑龙江省嫩江市高级中学2021届高三上学期期中考试化学试题黑龙江省大庆市铁人中学2021届高三上学期期中考试化学试题北京市中国人民大学附属中学分校 2021届高三上学期复习质量检测化学试题北京市首都师范大学附属中学2020届高三北京学校联考化学试题山西省太原市第五中学2020届高三10月月考化学试题【全国百强校】山东省青岛二中2019届高三上学期期中考试化学试题江西省抚州市临川区第一中学2018届高三上学期期中考试化学试题2017届北京市第三十一中学高三上学期期中化学试卷2016届北京市海淀区高三上学期期末考试化学试卷
更新时间:2021-03-24 18:04:42
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关实验说法正确的是
| A.易燃物钠、钾、白磷未用完,不能放回原试剂瓶 |
| B.酸碱中和滴定实验中,滴至接近终点时,需改为半滴滴加 |
| C.定容时仰视刻度线导致所配的溶液浓度偏高 |
D.向 溶液中滴加氨水至沉淀溶解得深蓝色溶液,再加入乙醇无明显变化 溶液中滴加氨水至沉淀溶解得深蓝色溶液,再加入乙醇无明显变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定中和滴定的终点。某化学小组同学利用该原理在常温时,分别测定NaOH溶液和氨水的物质的量浓度,并得到如图所示曲线。
①待测溶液:100 mL氨水、100 mL NaOH溶液 ②标准溶液:0.40mol/L的盐酸。
下列说法错误的是( )

①待测溶液:100 mL氨水、100 mL NaOH溶液 ②标准溶液:0.40mol/L的盐酸。
下列说法错误的是( )
| A.滴定NaOH溶液时,所得的曲线是b |
| B.达到滴定终点时,N点溶液的pH<7,M点溶液的pH=7 |
| C.氨水溶液的物质的量浓度为0.10mol/L |
| D.NaOH溶液的pH=13 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】高中课本中有多处“科学探究”,下列说法正确的是
| A.将Fe(OH)3胶体和泥水分别进行过滤,分别得到Fe(OH)3沉淀和泥土 |
| B.将铝箔在酒精灯上加热至熔化,观察熔化的铝并不滴下,这是因为铝表面的氧化膜保护了铝 |
C.铁粉与水蒸气反应的化学方程式:2Fe+3H2O(g) Fe2O3+3H2 Fe2O3+3H2 |
| D.食醋浸泡有水垢的暖壶或水壶,清除其中的水垢的离子方程式:2H++CaCO3=Ca2++H2O+CO2↑ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】过氧化钠可作呼吸面具中的供氧剂,实验室可用下图装置制取少量过氧化钠。下列说法错误的是


| A.装置X 还可以制取H2、CO2等气体 |
| B.②中所盛试剂为饱和小苏打溶液 |
| C.③的作用是防止空气中的水蒸气和二氧化碳进入直通玻璃管 |
| D.实验时需先让 X 装置反应一会儿,再点燃装置Z中的酒精灯 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】实验室中用如图所示装置制取纯净的无水CuCl2(部分仪器和夹持装置已略去)。下列说法正确的是


| A.装置C中试剂可以是饱和食盐水,目的是除去Cl2中的HCl |
| B.实验过程中,硬质玻璃管中产生大量棕黄色的烟 |
| C.装置B中试剂可以是浓硫酸,目的是除去Cl2中的H2O |
| D.实验时,应该先加热装置D,再加热装置A |
您最近一年使用:0次

 浓度的负常用对数)变化关系如图,下列有关说法正确的是
浓度的负常用对数)变化关系如图,下列有关说法正确的是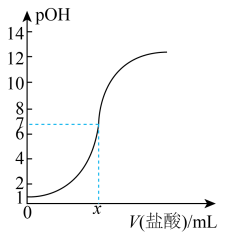
 ,则
,则