实验室用 与浓盐酸共热来制取氯气,并进行相关实验,实验装置如下图所示。请回答下列问题:
与浓盐酸共热来制取氯气,并进行相关实验,实验装置如下图所示。请回答下列问题:
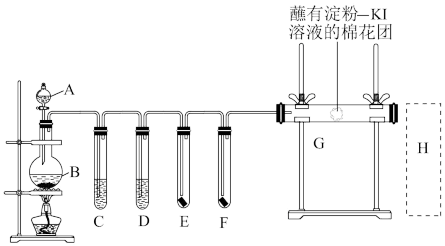
(1)C中盛装饱和 溶液的作用是
溶液的作用是____ ,D中盛装的是试剂是_____ ,写出B中发生反应的离子方程式____ 。
(2)E中为干燥的红色布条,F中为湿润的红色布条,可观察到的现象是___ ,对比E和F中现象的差异可得出的结论是___ 。
(3)G处的现象是____ 。
(4)写出H处尾气吸收装置中的离子反应方程式___ 。
(5)工业生成氯气的方法和实验室不同,请写出工业制氯气的化学反应方程式,并用双线桥分析该反应的电子转移的数目和方向___ 。
 与浓盐酸共热来制取氯气,并进行相关实验,实验装置如下图所示。请回答下列问题:
与浓盐酸共热来制取氯气,并进行相关实验,实验装置如下图所示。请回答下列问题:
(1)C中盛装饱和
 溶液的作用是
溶液的作用是(2)E中为干燥的红色布条,F中为湿润的红色布条,可观察到的现象是
(3)G处的现象是
(4)写出H处尾气吸收装置中的离子反应方程式
(5)工业生成氯气的方法和实验室不同,请写出工业制氯气的化学反应方程式,并用双线桥分析该反应的电子转移的数目和方向
更新时间:2021-03-26 14:22:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和 O2,Cl2O 易溶于水并与水反应生成 HClO。
【制备产品】
将氯气和空气(不参与反应)按体积比 1∶3 混合通入含水 8%的碳酸钠中制备 Cl2O,并 用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。
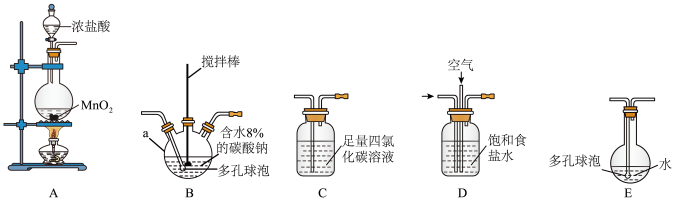
(1)各装置的连接顺序为_____ →_____ →_____ →C→_____ 。
(2)写出 A 中反应的离子方程式______ 。
(3)装置 B 中多孔球泡和搅拌棒的作用是_________ ; 装置 C 的作用是_____ 。
(4)制备 Cl2O 的化学方程式为_____ 。
(5)反应过程中,装置 B 需放在冷水中,其目的是_____ 。
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是_____ 、_____ 。
【测定浓度】
(7)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:
量取 10.00 mL 上述次氯酸溶液,并稀释至 100.00 mL,再从其中取出 10.00 mL 于 锥形瓶中,并加入 10.00 mL 0.8000 mol·L-1的 FeSO4溶液(过量),充分反应后,用0.05000 mol·L-1的酸性 KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液 24.00 mL,则 原次氯酸溶液的浓度为_____ 。判断下列情况对 HClO 含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若 FeSO4标准溶液部分变质,会使测定结果_____ ;若配制酸性 KMnO4溶液 时,定容时俯视刻度线,会使测定结果_________ 。
【制备产品】
将氯气和空气(不参与反应)按体积比 1∶3 混合通入含水 8%的碳酸钠中制备 Cl2O,并 用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。

(1)各装置的连接顺序为
(2)写出 A 中反应的离子方程式
(3)装置 B 中多孔球泡和搅拌棒的作用是
(4)制备 Cl2O 的化学方程式为
(5)反应过程中,装置 B 需放在冷水中,其目的是
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是
【测定浓度】
(7)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:
量取 10.00 mL 上述次氯酸溶液,并稀释至 100.00 mL,再从其中取出 10.00 mL 于 锥形瓶中,并加入 10.00 mL 0.8000 mol·L-1的 FeSO4溶液(过量),充分反应后,用0.05000 mol·L-1的酸性 KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液 24.00 mL,则 原次氯酸溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用如下图所示装置制备Cl2和新制的氯水,回答下列问题。

(1)装置中若无盛饱和食盐水的洗气瓶,将导致_______________ 。
(2)证明同时氯水中存在HCl和HClO的实验操作是____________________ 。
(3)图中制取氯气的化学方程式为________________________ ,
(4)NaOH溶液的作用是_____________________________ ,往反应后的烧杯溶液中加入浓盐酸可观察到有黄绿色气体生成,请写出该反应的化学方程式_____________________ 。

(1)装置中若无盛饱和食盐水的洗气瓶,将导致
(2)证明同时氯水中存在HCl和HClO的实验操作是
(3)图中制取氯气的化学方程式为
(4)NaOH溶液的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有中学化学常见的物质A、B、C、D、E、F、G、H,满足如图所示转化关系,其中A、G为气体单质,A呈黄绿色,H为“84消毒液”的有效成分。B为生活中常见的液体化合物。

回答下列问题:
(1)写出下列物质的化学式:C_______ G_______ 。
(2)写出下列反应的化学方程式:①_______ ,④_______ 。
(3)反应②的反应类型为_______ (填四大基本反应类型)。
(4)向盛有紫色石蕊溶液的试管中持续通入A至过量,溶液颜色可能出现无色、浅黄绿色、红色等变化。

①过程I溶液由紫色变成红色,起作用的物质是_______ (填化学式)。
②过程Ⅱ溶液由红色变成无色,原因是_______ 。
③过程Ⅲ溶液颜色变化是_______ 。

回答下列问题:
(1)写出下列物质的化学式:C
(2)写出下列反应的化学方程式:①
(3)反应②的反应类型为
(4)向盛有紫色石蕊溶液的试管中持续通入A至过量,溶液颜色可能出现无色、浅黄绿色、红色等变化。

①过程I溶液由紫色变成红色,起作用的物质是
②过程Ⅱ溶液由红色变成无色,原因是
③过程Ⅲ溶液颜色变化是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图表示在没有通风橱的条件下制备氯气时设计的装置, 图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)

⑴仪器A的名称是____________________ ;水槽中应盛放的是____________________ ;
烧杯中盛放的是______________________ ;烧瓶中反应的化学方程式________________ ;
⑵在收集氯气时,应打开________ ,关闭_________ 。当氯气收集完毕时打开_________ ,关闭___ 。(填a,b)
⑶ 若要制得标准状况下的Cl2 0.672L,理论上需要MnO2的物质的量是__________ ?

⑴仪器A的名称是
烧杯中盛放的是
⑵在收集氯气时,应打开
⑶ 若要制得标准状况下的Cl2 0.672L,理论上需要MnO2的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】太和一中理化创新社的同学们为了探究在实验室制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有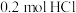 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是_____________________ 。
(2)①装置B的作用是_______________________ ,现象是_____________________ 。
②装置C和D出现的不同现象说明的问题是__________________________ 。
③装置E的作用是_______________________________ 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________ 与_________ 之间(填装置字母序号),装置中应放入___________________________ 。
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(1)若用含有
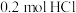 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是(2)①装置B的作用是
②装置C和D出现的不同现象说明的问题是
③装置E的作用是
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中 A、F 为氨气和氯气的发生装置,C 为纯净、干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置 F 中发生反应的离子方程式是______________ 。
(2)装置 A 中的烧瓶内固体可选用_______________ (选填以下选项的代号)。
A 碱石灰 B 浓硫酸 C 生石灰 D 五氧化二磷 E 烧碱
(3)虚线框内应添加必要的除杂装置,请从图的备选装置中选择,并将编号填入下列空格:



Ⅰ Ⅱ Ⅲ
B___ D____ E_____
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:________ ;装置 C 内出现浓厚的白烟,该物质化学式为_________ 。
(5)若从装置 C 中 G 处逸出的尾气中含有 N2 和少量 C12,应如何处理________ 。

请回答下列问题:
(1)装置 F 中发生反应的离子方程式是
(2)装置 A 中的烧瓶内固体可选用
A 碱石灰 B 浓硫酸 C 生石灰 D 五氧化二磷 E 烧碱
(3)虚线框内应添加必要的除杂装置,请从图的备选装置中选择,并将编号填入下列空格:



Ⅰ Ⅱ Ⅲ
B
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:
(5)若从装置 C 中 G 处逸出的尾气中含有 N2 和少量 C12,应如何处理
您最近一年使用:0次



