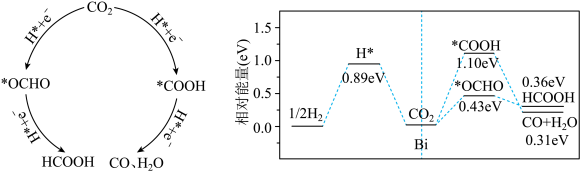
2021年中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法: ,这是迄今最接近人造光合作用的方法,
,这是迄今最接近人造光合作用的方法, 加氢制
加氢制 的一种催化机理如图。下列说法正确的是
的一种催化机理如图。下列说法正确的是

 ,这是迄今最接近人造光合作用的方法,
,这是迄今最接近人造光合作用的方法, 加氢制
加氢制 的一种催化机理如图。下列说法正确的是
的一种催化机理如图。下列说法正确的是
A.反应中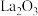 是中间产物 是中间产物 |
B. 转化为 转化为 利用了 利用了 的氧化性 的氧化性 |
C. 经过 经过 活性中心裂解产生带负电荷的H 活性中心裂解产生带负电荷的H |
| D.使用催化剂可以降低反应的焓变,从而提高化学反应速率 |
2021·天津南开·一模 查看更多[6]
吉林省通化市梅河口市第五中学2023-2024学年高三上学期开学考试化学试题内蒙古莫力达瓦旗尼尔基第一中学2021-2022学年高三上学期期末考试化学试题(已下线)专题七 化学反应速率与化学平衡 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第五次月考化学试题黑龙江省大庆中学2021届高三第一次仿真考试化学试题天津市南开区2021届高三下学期一模化学试题
更新时间:2021-04-13 21:44:20
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.对于有气体参加的反应,通过压缩体积来增大压强,单位体积内的活化分子数增多 |
B.中和反应热的测定实验中,把稀HCl换成 溶液,测得中和反应热的数值会偏大 溶液,测得中和反应热的数值会偏大 |
C.用铁片与稀 反应制 反应制 时,若改用98%的浓 时,若改用98%的浓 ,可以增大产生 ,可以增大产生 的速率 的速率 |
D. 的催化氧化是放热反应,所以升高温度,正反应速率增大,逆反应速率减小 的催化氧化是放热反应,所以升高温度,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于有效碰撞理论与影响速率因素之间关系不正确的是
| A.活化分子间所发生的部分碰撞为有效碰撞 |
| B.增大反应物浓度能够增大活化分子数,化学反应速率增大 |
| C.升高温度,活化分子百分数增大,化学反应速率增大 |
| D.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
您最近一年使用:0次