为探究白色固体X(仅含两种元素)的组成和性质,设计并完成如下实验(所加试剂都是过量的):
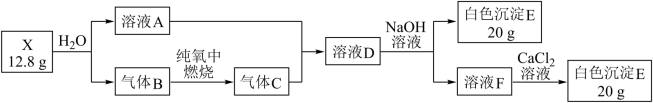
其中气体B在标准状况下的密度为1.16g·L-1 请回答:
(1)气体B的结构式为___________
(2)X的化学式是________
(3)溶液D与NaOH溶液反应的离子反应方程式是______________________

其中气体B在标准状况下的密度为1.16g·L-1 请回答:
(1)气体B的结构式为
(2)X的化学式是
(3)溶液D与NaOH溶液反应的离子反应方程式是
更新时间:2021-04-14 23:19:04
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E为短周期元素,原子序数依次增大,质子数之和为40,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素,问:
(1)B元素在周期表中的位置为_________________ ;
(2)D的单质投入A2C中得到一种无色溶液。E的单质在该无色溶液中反应的离子方程式为_____________________ 。
(3)用电子式表示由A、C两元素组成的四核18电子的共价化合物的形成过程_____________ 。
(4)以往回收电路板中铜的方法是灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,该反应的化学方程式为___________________ 。
(5)乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式__________ ,当转移电子1.2mol时,消耗氧气标况下体积为______________ 。
(1)B元素在周期表中的位置为
(2)D的单质投入A2C中得到一种无色溶液。E的单质在该无色溶液中反应的离子方程式为
(3)用电子式表示由A、C两元素组成的四核18电子的共价化合物的形成过程
(4)以往回收电路板中铜的方法是灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,该反应的化学方程式为
(5)乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2,实验装置如下。

实验步骤如下:①连接好实验装置② 。
③把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。④加热,开始反应,直到不再有气体产生为止。⑤读取量气管读数,换算成标准状况下氧气的体积为278.8 mL。⑥准确称量试管和残留物的质量为15. 55 g。
回答下列问题。
(1)写出氯酸钾分解制O2的化学方程式:__________________________________ 。
(2)实验步骤的第②步是________________________________________________ 。
(3)实验过程中产生氧气的物质的量是_______ mol(保留小数点后四位);实验测得氧气的气体摩尔体积是_________ (保留小数点后两位)。
(4)根据以上实验得出如下结论,其中不正确的是_________________ 。
A.气体摩尔体积与气体的温度相关
B.在该实验条件下,3 mol O2的气体摩尔体积为67.14 L/mol
C.同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D.该实验条件下,O2的密度为1.429 g/L
E. 测量气体体积时,应注意①气体应恢复到室温下;②调整量气管高度,使其液面高度与水准管液面高度相平;③视线与凹液面最低处相平。

实验步骤如下:①连接好实验装置② 。
③把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。④加热,开始反应,直到不再有气体产生为止。⑤读取量气管读数,换算成标准状况下氧气的体积为278.8 mL。⑥准确称量试管和残留物的质量为15. 55 g。
回答下列问题。
(1)写出氯酸钾分解制O2的化学方程式:
(2)实验步骤的第②步是
(3)实验过程中产生氧气的物质的量是
(4)根据以上实验得出如下结论,其中不正确的是
A.气体摩尔体积与气体的温度相关
B.在该实验条件下,3 mol O2的气体摩尔体积为67.14 L/mol
C.同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D.该实验条件下,O2的密度为1.429 g/L
E. 测量气体体积时,应注意①气体应恢复到室温下;②调整量气管高度,使其液面高度与水准管液面高度相平;③视线与凹液面最低处相平。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH 、K+、CO
、K+、CO 、SO
、SO 离子中的几种,为分析其成分,取该溶液分别进行如图四个实验,其操作和有关现象如图所示:
离子中的几种,为分析其成分,取该溶液分别进行如图四个实验,其操作和有关现象如图所示:

回答下列问题:
(1)原溶液中一定存在的离子是____ ,一定不存在的离子是____ 。
(2)实验②中加入稀盐酸的目的是_____ 。
(3)实验③中产生无色无味气体发生反应的化学方程式为_____ 。实验反应过程中转移NA个电子,则产生_____ L气体(标准状况下)。
(4)实验④中最终产生的沉淀是_____ (填化学式)。写出A→B过程中发生反应的离子方程式_____ 。
 、K+、CO
、K+、CO 、SO
、SO 离子中的几种,为分析其成分,取该溶液分别进行如图四个实验,其操作和有关现象如图所示:
离子中的几种,为分析其成分,取该溶液分别进行如图四个实验,其操作和有关现象如图所示:
回答下列问题:
(1)原溶液中一定存在的离子是
(2)实验②中加入稀盐酸的目的是
(3)实验③中产生无色无味气体发生反应的化学方程式为
(4)实验④中最终产生的沉淀是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】在如图所示的物质转化关系中,A是常见气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是一种紫红色金属单质(反应条件和部分生成物未列出)。

请回答下列问题:
(1)A的电子式为_______ 。
(2)实验室长期保存氨水时,需使用_______ 试剂瓶。
(3)实验室检验A的操作为_______ 。
(4)反应①的化学方程式为_______ 。
(5)反应②的离子方程式为_______ 。

请回答下列问题:
(1)A的电子式为
(2)实验室长期保存氨水时,需使用
(3)实验室检验A的操作为
(4)反应①的化学方程式为
(5)反应②的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
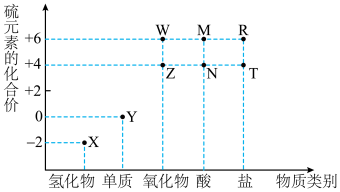
【推荐2】利用元素的化合价物质类别的坐标系,可以对含某元素的各物质性质有整体的认识。如图是硫元素的常见化合价与部分物质类别的对应关系。______ ;检验其阴离子的方法是______ 。
(2)化石燃料的燃烧可产生 ,在上述图表中它是
,在上述图表中它是______ (图中的字母),为避免过多 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为______ 。
②氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH______ (填“升高”“不变”或“降低”)。
③排放海水与原海水相比,减少的 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为______ 。
(3) 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为______ ;每脱除170kg X,消耗标准状况下 的体积为
的体积为______ L。
(2)化石燃料的燃烧可产生
 ,在上述图表中它是
,在上述图表中它是 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。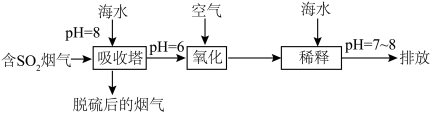
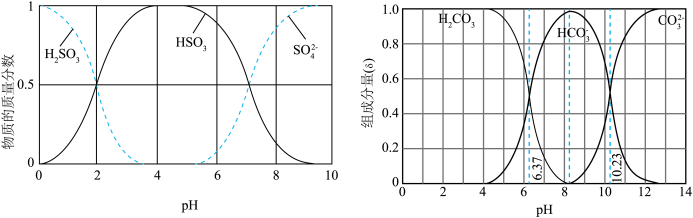
 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为②氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH③排放海水与原海水相比,减少的
 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为(3)
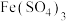 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为 的体积为
的体积为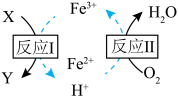
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学欲证明乙炔能与高锰酸钾酸性溶液反应,实验方案如下:将电石与水反应生成的气体通入高锰酸钾酸性溶液,溶液褪色,证明二者发生了反应.请回答:
(1)制备乙炔的反应的化学方程式是_______ ;
(2)该同学的实验方案存在的问题是_______ 。
(3)为了解决上述问题,需重新选择实验装置,实验装置如图所示:
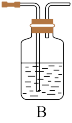
①B装置中所盛放的试剂是_______ ;
②乙炔能与酸性高锰酸钾酸性溶液反应的化学方程式是_______ 。
(1)制备乙炔的反应的化学方程式是
(2)该同学的实验方案存在的问题是
(3)为了解决上述问题,需重新选择实验装置,实验装置如图所示:

①B装置中所盛放的试剂是
②乙炔能与酸性高锰酸钾酸性溶液反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用如图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的乙炔气体中往往含有少量的 气体,请按下列要求填空:
气体,请按下列要求填空:
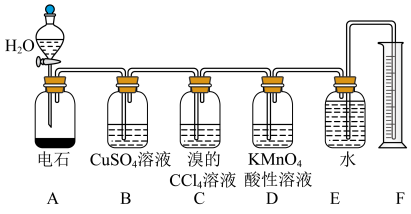
(1)实验室制乙炔的化学方程式是___________ ;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用___________ 来代替水,其目的是___________ 。
(2)装置B中 溶液的作用是
溶液的作用是___________ 。
(3)装置C中观察到的现象是___________ ,反应的化学方程式是___________ 。
(4)装置D中观察到的现象是___________ ,该反应的类型是___________ 。
 气体,请按下列要求填空:
气体,请按下列要求填空:
(1)实验室制乙炔的化学方程式是
(2)装置B中
 溶液的作用是
溶液的作用是(3)装置C中观察到的现象是
(4)装置D中观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组设计如图所示实验装置来制取乙炔,并粗略测定电石(含有N、P、S等元素)中碳化钙的质量分数。回答下列问题:

(1)导管a的作用是_______ 。
(2)仪器b中发生反应的化学方程式为_______ ,实验过程中为了减缓水与电石的反应速率,可采取的措施是_______ (写一条即可)。
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色,_______ (填“能”或“不能”)说明生成的气体全部为乙炔,原因是_______ 。
(4)装置c中盛放的试剂为_______ (填化学式)。
(5)为了安全,点燃乙炔前应_______ , 乙炔燃烧时的现象是_______ 。
(6)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为V mL, 则电石中碳化钙的质量分数为_______ 。(用含 V和m的代数式表示,忽略导管中残留的水和气体中含有的水蒸气,所有气体均已换算成标准状况下)。

(1)导管a的作用是
(2)仪器b中发生反应的化学方程式为
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色,
(4)装置c中盛放的试剂为
(5)为了安全,点燃乙炔前应
(6)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为V mL, 则电石中碳化钙的质量分数为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】丙炔可以发生下列物质转化,结合已知信息,回答下列问题:
(2)写出W的官能团名称:___________ ,写出其中的顺式结构:___________ 。①的反应类型:___________ ,写出反应②的化学方程式:___________ 。
(3)物质 M是丙炔的同系物且同时满足以下三个条件,写出M的系统命名___________ 。
①质谱图中最大质荷比为82;②主链4个碳;③分子中存在三个甲基。
(4)物质Y在光照条件下的一氯代物有___________ 种,物质Y完全氢化后的产物核磁共振氢谱的峰面积比为___________ 。
(5)分子式为C12H18与物质Y互为同系物,且只有一个侧链,写出所有不能被酸性KMnO4溶液氧化成苯甲酸的结构简式:___________ 。(已知:若苯的同系物侧链的烷基中,直接与苯环连接的碳原子上没有C—H,则该物质一般不能被酸性KMnO4溶液氧化成苯甲酸。)

已知:①
②
| A.Li2C2 | B.ZnC2 | C.Al4C3 | D.Mg2C3 |
(2)写出W的官能团名称:
(3)物质 M是丙炔的同系物且同时满足以下三个条件,写出M的系统命名
①质谱图中最大质荷比为82;②主链4个碳;③分子中存在三个甲基。
(4)物质Y在光照条件下的一氯代物有
(5)分子式为C12H18与物质Y互为同系物,且只有一个侧链,写出所有不能被酸性KMnO4溶液氧化成苯甲酸的结构简式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
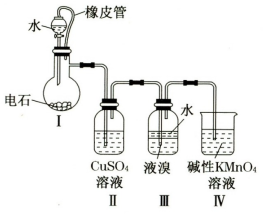
【推荐3】四溴化乙烷(CHBr2-CHBr2)是一种无色液体,常用于合成季铵化合物。某同学在实验室模仿工业生产,以电石(主要成分CaC2,少量CaS、Ca3P2、Ca3As2等)和Br2等为原料制备少量四溴化乙烷,实验装置(夹持装置已省略)如图所示。已知:四溴化乙烷的熔点为1℃,沸点为244℃,密度为2.967g•cm﹣3,难溶于水。回答下列问题:
(1)装置I中CaC2与水反应生成乙炔(C2H2)和氢氧化钙,写出该反应的化学方程式:_______ :该反应剧烈,为了得到平缓的C2H2气流,可采取的措施是 _______ 。
(2)装置II的目的是_______ 。
(3)装置Ⅲ中在液溴液面上加入一层水的目的是_______ 。
(4)装置IV的目的是除去未反应的乙炔。在碱性条件下,KMnO4与C2H2反应生成碳酸盐和MnO2,则该反应中参与反应的氧化剂和还原剂的物质的量之比为_______ 。
(5)实际工业生产中会产生大量的副产物Ca(OH)2,用于制备漂白粉,写出制备漂白粉的化学方程式:_______ 。
(1)装置I中CaC2与水反应生成乙炔(C2H2)和氢氧化钙,写出该反应的化学方程式:
(2)装置II的目的是
(3)装置Ⅲ中在液溴液面上加入一层水的目的是
(4)装置IV的目的是除去未反应的乙炔。在碱性条件下,KMnO4与C2H2反应生成碳酸盐和MnO2,则该反应中参与反应的氧化剂和还原剂的物质的量之比为
(5)实际工业生产中会产生大量的副产物Ca(OH)2,用于制备漂白粉,写出制备漂白粉的化学方程式:

您最近一年使用:0次





