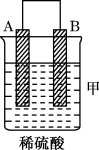
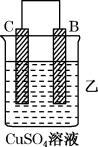
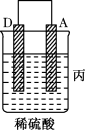
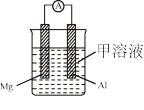
把A、B、C、D四种金属按表中装置进行实验。
根据实验现象回答问题:
(1)装置乙中正极的电极反应式是___ 。
(2)装置丙中溶液的酸性___ (填“变大”“变小”或“不变”)。
(3)四种金属活泼性由强到弱的顺序是___ 。
| 装置 | 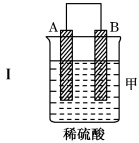 |  | 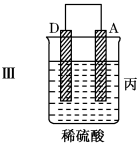 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置乙中正极的电极反应式是
(2)装置丙中溶液的酸性
(3)四种金属活泼性由强到弱的顺序是
更新时间:2021-04-14 16:45:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组研究化学反应中的能量变化,进行了如下实验。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为_______ 。
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。
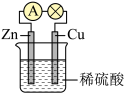
锌片上电极反应式为___________ ;铜片上能够观察到的现象是___________ ;电子流向 ___________ 填“锌片−导线−铜片”或“铜片−导线−锌片”)
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是___________ 。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。

锌片上电极反应式为
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组同学实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:_______ 。
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为_______ 。
综合上述实验,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(2)采用电化学装置进行验证。
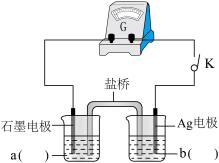
小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为_______ 溶液;b为_______ 溶液;(写a、b化学式)
ii.再向左侧烧杯中滴加较浓的_______ 溶液,产生的现象为_______ 。表明“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为
综合上述实验,证实“Ag++Fe2+
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(2)采用电化学装置进行验证。

小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为
ii.再向左侧烧杯中滴加较浓的
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是__________ (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计的原电池,请在图甲中的横线上完成标注________ 。
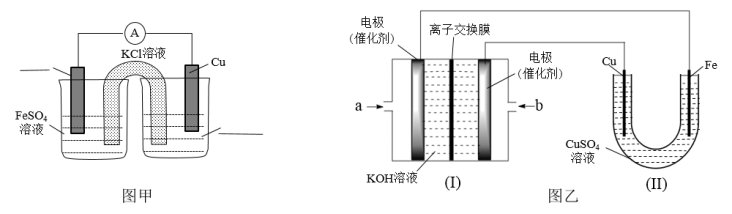
②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入____ (填“CH4”或“O2”),b处电极上发生的电极反应式为_________ ;
若把II中电极均换为惰性电极,电解液换为含有0.1 mol NaCl溶液400 mL,当阳极产生的气体为448 mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,______________ 直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计的原电池,请在图甲中的横线上完成标注

②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入
若把II中电极均换为惰性电极,电解液换为含有0.1 mol NaCl溶液400 mL,当阳极产生的气体为448 mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氯化钒(VCl2)有强还原性和吸湿性,熔点为425℃、沸点为900℃,是制备多种医药、催化剂、含钒化合物的中间体。学习小组在实验室制备VCl2并进行相关探究。回答下列问题:

(1)小组同学通过VCl3分解制备VCl2。
①按气流方向,图中装置合理的连接顺序为_______ (用小写字母填空)。
②A中盛放NaNO2的仪器名称为_______ ,其中发生反应的离子方程式为_______ 。
③实验前需通入N2,其作用为_______ 。
(2)测定产品纯度:实验后产品中混有少量VCl3杂质。称量2.795g样品,溶于水充分水解,调pH后滴加Na2CrO4作指示剂,用0.5000mol/L AgNO3标准溶液滴定Cl-,达到滴定终点时消耗标准液体积为100.00mL(Ag2CrO4为砖红色沉淀,杂质不参加反应)
①滴定终点的现象为_______ 。
②产品中VCl3与VCl2的物质的量之比为_______ 。
(3)小组同学进一步用如图所示装置比较含钒离子的还原性。接通电路后,观察到右侧锥形瓶中溶液蓝色逐渐变深,发生的电极反应式为_______ 。


(1)小组同学通过VCl3分解制备VCl2。
①按气流方向,图中装置合理的连接顺序为
②A中盛放NaNO2的仪器名称为
③实验前需通入N2,其作用为
(2)测定产品纯度:实验后产品中混有少量VCl3杂质。称量2.795g样品,溶于水充分水解,调pH后滴加Na2CrO4作指示剂,用0.5000mol/L AgNO3标准溶液滴定Cl-,达到滴定终点时消耗标准液体积为100.00mL(Ag2CrO4为砖红色沉淀,杂质不参加反应)
①滴定终点的现象为
②产品中VCl3与VCl2的物质的量之比为
(3)小组同学进一步用如图所示装置比较含钒离子的还原性。接通电路后,观察到右侧锥形瓶中溶液蓝色逐渐变深,发生的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示是一个燃料电池的示意图,当此燃料电池工作时:

(1)如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上的电极反应为:______ 。
(2)如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上的电极反应为:______ 。
(3)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:______ 。
(4)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl,当电路中转移1mole-时,交换膜左侧溶液中理论上减少______ mol离子,交换膜右侧溶液中c(HCl)______ 1mol•L-1(填“>”“<”或“=”)(忽略溶液体积变化)。
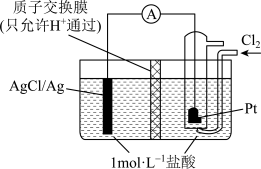

(1)如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上的电极反应为:
(2)如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上的电极反应为:
(3)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:
(4)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl,当电路中转移1mole-时,交换膜左侧溶液中理论上减少

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】电化学知识在物质制备领域的应用前景看好。
(1)利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。
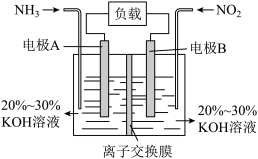
①A电极的电极反应式为____ 。
②下列关于该电池的说法正确的是____ 。
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
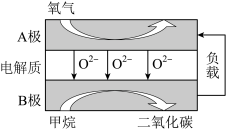
①B极上的电极反应式为____ 。
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到11.2L(标准状况)气体时,消耗甲烷的体积为____ L(标准状况下)。
(3)按如图1所示装置进行电解,A、B、C、D均为铂电极,回答下列问题。
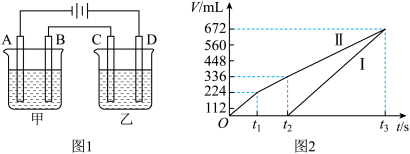
已知一:甲槽电解的是200mL一定浓度的NaCl与CuSO4的混合溶液,理论上两极所得气体体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计)。
①原混合溶液中NaCl的物质的量浓度为____ mol•L-1。
已知二:乙槽为200mLCuSO4溶液:
②当C极析出0.64g物质时,乙槽溶液中生成的H2SO4为____ mol。
③若通电一段时间后,向所得的乙槽溶液中加入0.2mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为____ (用NA表示)。
(1)利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

①A电极的电极反应式为
②下列关于该电池的说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

①B极上的电极反应式为
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到11.2L(标准状况)气体时,消耗甲烷的体积为
(3)按如图1所示装置进行电解,A、B、C、D均为铂电极,回答下列问题。

已知一:甲槽电解的是200mL一定浓度的NaCl与CuSO4的混合溶液,理论上两极所得气体体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计)。
①原混合溶液中NaCl的物质的量浓度为
已知二:乙槽为200mLCuSO4溶液:
②当C极析出0.64g物质时,乙槽溶液中生成的H2SO4为
③若通电一段时间后,向所得的乙槽溶液中加入0.2mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】由A、B、C、D四种金属按下表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是____ 。
(2)装置丙中溶液中的SO 移向
移向____ 极(填D或A)。
(3)四种金属活泼性由强到弱的顺序是____ 。
(4)若C质量增加32g,则当丙中通过和乙等量电量时,丙中将析出标况下的气体体积为___ L。
| 装置 | 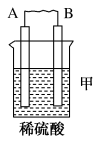 |  | 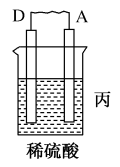 |
| 现象 | 二价金属A 不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置丙中溶液中的SO
 移向
移向(3)四种金属活泼性由强到弱的顺序是
(4)若C质量增加32g,则当丙中通过和乙等量电量时,丙中将析出标况下的气体体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
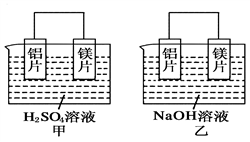
(1)写出甲中正极的电极反应式___________________ 。
(2)乙中负极材料为___________________ ,乙中总反应的离子方程式:___________________ 。
(3)甲与乙同学均认为“如果构成原电池的电极材料都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出___________________ 活动性更强,而乙会判断出___________________ 活动性更强(填写元素符号)。
(4)由此实验得出的下列结论中,正确的有___________________ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析

(1)写出甲中正极的电极反应式
(2)乙中负极材料为
(3)甲与乙同学均认为“如果构成原电池的电极材料都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验得出的下列结论中,正确的有
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
您最近一年使用:0次