计算题。将5.1g 镁铝合金的混合物投入100 mL 某浓度的稀硫酸中,恰好完全反应,放出标准状况下氢气的体积为5.6 L。求:
(1)合金混合物中Mg的质量分数___________
(2)原稀硫酸的物质的量浓度___________ 。
(1)合金混合物中Mg的质量分数
(2)原稀硫酸的物质的量浓度
更新时间:2021-04-19 15:37:48
|
相似题推荐
【推荐1】某兴趣小组为确定Cu(NO3)2·xH2O的结晶水数目,称取样品5.92g,加热使其完全分解,得到1.60g黑色固体产物,同时分解产生的红棕色混合气体经冷凝得到3.2mL无色液体,无气体剩余。请计算:
(1)x=____ 。(写出计算过程,下同)
(2)无色液体的浓度为____ mol·L-1。
(1)x=
(2)无色液体的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铝虽为金属,但可与氢氧化钠溶液发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,现将27g的铝粉投入到足量的NaOH溶液中,充分反应后,计算:
(1)铝粉的物质的量_____ ;
(2)消耗氢氧化钠溶质的质量为多少克?________
(3)得到标准状况下的氢气的体积是多少升?_____________
(1)铝粉的物质的量
(2)消耗氢氧化钠溶质的质量为多少克?
(3)得到标准状况下的氢气的体积是多少升?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】按要求计算
(1) 个
个 含
含_________  氨分子,
氨分子,_________  氢原子,在标准状况下的体积为
氢原子,在标准状况下的体积为________ L。
(2)某金属氯化物 中含有
中含有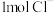 ,则
,则 的物质的量为
的物质的量为_____________ 、摩尔质量为________ ,金属M的相对原子质量为________ ,溶于水配成 溶液,所得溶液中的
溶液,所得溶液中的 的物质的量浓度为
的物质的量浓度为_________
(3)我国海水资源丰富,开发和利用海水资源是当前科学研究的一个重要项目,图是海水综合利用的一个方面:

已知反应⑤的化学方程式为: ,若需生产标况下的氯气
,若需生产标况下的氯气 ,试计算(写出计算过程):
,试计算(写出计算过程):
①消耗食盐的质量________ ;
②生成烧碱的物质的量________ 。
(1)
 个
个 含
含 氨分子,
氨分子, 氢原子,在标准状况下的体积为
氢原子,在标准状况下的体积为(2)某金属氯化物
 中含有
中含有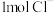 ,则
,则 的物质的量为
的物质的量为 溶液,所得溶液中的
溶液,所得溶液中的 的物质的量浓度为
的物质的量浓度为(3)我国海水资源丰富,开发和利用海水资源是当前科学研究的一个重要项目,图是海水综合利用的一个方面:

已知反应⑤的化学方程式为:
 ,若需生产标况下的氯气
,若需生产标况下的氯气 ,试计算(写出计算过程):
,试计算(写出计算过程):①消耗食盐的质量
②生成烧碱的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】取表面部分氧化的镁条8.00g溶于250mL4.00mol·L-1的稀盐酸中,向所得溶液中滴加未知浓度的NaOH溶液,产生沉淀的质量与NaOH溶液的体积关系如图所示:
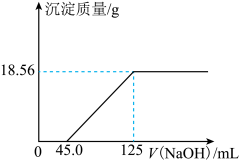
请计算:
(1)NaOH溶液的物质的量浓度___ mol·L-1。
(2)样品中镁元素的质量___ g。

请计算:
(1)NaOH溶液的物质的量浓度
(2)样品中镁元素的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下,进行甲、乙、丙三组实验,三组实验各取30mL同浓度的盐酸,加入同一种镁、铝混合物粉末,产生气体,有关数据列表如下:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 1020 |
| 气体体积/mL | 560 | 672 | 672 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】向500mL氢氧化钠溶液中投入10.8g铝,二者恰好完全反应,计算回答下列问题:
(1)参加反应的铝的物质的量是_______ mol。
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积_____ (请写出计算过程)。
(1)参加反应的铝的物质的量是
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在标准状况下进行甲、乙、丙三组实验:各取30mL同浓度的盐酸溶液,加入不同质量的同一种镁铝合金粉末,产生气体,有关数据记录如下:

试回答:
(1)计算出盐酸的物质的量浓度为__________________ mol/L(保留两位有效数字)。
(2)镁、铝的物质的量之比为__________________ 。

试回答:
(1)计算出盐酸的物质的量浓度为
(2)镁、铝的物质的量之比为
您最近一年使用:0次



