下列关于晶体的说法正确的组合是
①所有分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键
⑤SiO2晶体中每个硅原子与4个氧原子以共价键相结合
⑥晶体中分子间作用力越大,分子越稳定
⑦氯化钠熔化时离子键被破坏
⑧含有共价键的晶体熔沸点都比较高,因为熔化时需要破坏共价键
①所有分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键
⑤SiO2晶体中每个硅原子与4个氧原子以共价键相结合
⑥晶体中分子间作用力越大,分子越稳定
⑦氯化钠熔化时离子键被破坏
⑧含有共价键的晶体熔沸点都比较高,因为熔化时需要破坏共价键
| A.①②⑤ | B.③⑤⑦ | C.⑤⑥⑧ | D.④⑦⑧ |
20-21高二下·辽宁锦州·阶段练习 查看更多[4]
江苏省常州市礼嘉中学2020-2021学年高二下学期第二次阶段质量调研化学试题山东省泰安第十九中学2020-2021学年高二下学期期中考试化学试题(已下线)3.3 金属晶体与离子晶体(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)辽宁省锦州市义县高中2020-2021学年高二下学期4月考试化学试题
更新时间:2021-04-16 11:49:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学键或微粒间作用力叙述正确的是
| A.共价键均有饱和性和方向性 |
| B.离子键的强弱和离子半径及所带电荷有关 |
| C.石英熔化和干冰升华克服的作用力类型相同 |
| D.碳碳双键比碳碳单键键能更大,故碳碳双键更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中正确的是
| A.离子晶体中肯定不含非极性共价键 |
| B.原子晶体的熔点肯定高于其它晶体 |
| C.由分子组成的物质其熔点一定较低 |
| D.原子晶体中除非极性共价键外不存在其它类型的化学键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各项的叙述中都包含两个数值,前一数值大于后一数值的是
| A.单质碘中的分子间作用力和干冰中的分子间作用力 |
| B.NaCl晶体中与一个Cl-紧邻的Na+数和CsCl晶体中与一个Cl-紧邻的Cs+数 |
| C.晶体硅中Si—Si键的键能和金刚石中C—C键的键能 |
| D.原子晶体的沸点和金属晶体的沸点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定条件下,CO2分子晶体可转化为具有类似SiO2结构的原子晶体.从理论上分析,下列说法正确的是( )
| A.该转化过程是物理变化 |
| B.1molCO2原子晶体中含2mol C﹣O键 |
| C.CO2原子晶体的熔点高于SiO2 |
| D.CO2的原子晶体和分子晶体互为同分异构体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】钛铁基储氢合金是由钛、铁两种元素组成的金属间化合物。该合金吸收氢气后的晶胞如图1所示,每个氢被4个钛原子和2个铁原子包围。下列说法不正确 的是


| A.钛铁合金属于金属晶体,主要作用力为金属键 |
| B.未吸收氢气时,钛铁合金的晶胞示意图为图2 |
| C.钛铁合金中每个Ti周围距离最近且等距的Fe有8个 |
| D.图1中形成的金属氢化物的化学式:TiFeH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】碳元素能形成CO、 、
、 、
、 、
、 等多种化合物;其单质也有多种用途,如足量
等多种化合物;其单质也有多种用途,如足量 与
与 反应可用于制备
反应可用于制备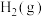 和
和 (俗称水煤气);被称为“黑金”的石墨烯也是一种碳单质,石墨烯是碳原子构成的六边形结构、只有一层原子厚度的二维晶体,又称为“新材料之王”。下列物质结构与性质或物质性质与用途具有对应关系的是
(俗称水煤气);被称为“黑金”的石墨烯也是一种碳单质,石墨烯是碳原子构成的六边形结构、只有一层原子厚度的二维晶体,又称为“新材料之王”。下列物质结构与性质或物质性质与用途具有对应关系的是
 、
、 、
、 、
、 等多种化合物;其单质也有多种用途,如足量
等多种化合物;其单质也有多种用途,如足量 与
与 反应可用于制备
反应可用于制备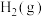 和
和 (俗称水煤气);被称为“黑金”的石墨烯也是一种碳单质,石墨烯是碳原子构成的六边形结构、只有一层原子厚度的二维晶体,又称为“新材料之王”。下列物质结构与性质或物质性质与用途具有对应关系的是
(俗称水煤气);被称为“黑金”的石墨烯也是一种碳单质,石墨烯是碳原子构成的六边形结构、只有一层原子厚度的二维晶体,又称为“新材料之王”。下列物质结构与性质或物质性质与用途具有对应关系的是| A.CO是气体,可用作冶炼铁的原料 | B.甲醛能溶于水,可用于制备酚醛树脂 |
| C.石墨烯是二维晶体,石墨烯具有导电性 | D.金属钙中存在的金属键没有方向性,金属钙具有延展性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于物质熔、沸点高低说法错误的是
A.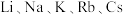 的熔、沸点依次降低 的熔、沸点依次降低 |
B. 比 比 熔点高 熔点高 |
C. 的熔、沸点依次升高 的熔、沸点依次升高 |
| D.分子晶体中共价键的键能越大,分子晶体的熔、沸点越高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下面的排序不正确的是( )
| A.金属Cu中Cu原子堆积方式为面心立方最密堆积,每个Cu原子的配位数均为12 |
| B.晶体的熔点:SiC>CCl4>P4>SO2 |
| C.酸性:HClO4>HClO3>HClO |
| D.晶格能由大到小:NaF>NaCl>NaBr>NaI |
您最近一年使用:0次




