用化学用语表达:
(1)Na2O2的电子式_______ ,N2H4的电子式为:_______ 。
(2)C2H2的结构式为:_______ ,COS的结构式为:_______ 。
(3)用电子式表示下列过程:
①CaCl2的形成过程_______
②H2O2的形成过程_______
(1)Na2O2的电子式
(2)C2H2的结构式为:
(3)用电子式表示下列过程:
①CaCl2的形成过程
②H2O2的形成过程
更新时间:2021-04-22 21:27:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】用化学用语填空:空气中含量最多的气体是___________ ;地壳中含量最多的金属元素与人体中含量最多的非金属元素形成化合物的化学式为___________ 。保持水化学性质的最小粒子是___________ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识回答下列问题
(1)写出NaHSO3在水溶液中的电离方程式______ ;
(2)写出制作印刷电路板常用的反应离子方程式______ ;
(3)写出有机物1,3-丁二烯的结构简式______ ;
(4)写出“84消毒液”有效成分的电子式______ 。
(1)写出NaHSO3在水溶液中的电离方程式
(2)写出制作印刷电路板常用的反应离子方程式
(3)写出有机物1,3-丁二烯的结构简式
(4)写出“84消毒液”有效成分的电子式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭发动机中燃料的喷嘴。氮化硅可由石英、焦炭在高温氮气流中制取。完成下列填空:
SiO2 +______C +_____N2 ______Si3N4 + ________CO
______Si3N4 + ________CO
(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目_____ 。
(2)反应中___________ 被还原,当氧化产物比还原产物多1mol时,反应中电子转移数为___________ 。
(3)在该反应体系中:所涉及物质属于单质的电子式为___________ ;所涉及元素中原子半径最大的原子的结构示意图为___________ 。
SiO2 +______C +_____N2
 ______Si3N4 + ________CO
______Si3N4 + ________CO(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目
(2)反应中
(3)在该反应体系中:所涉及物质属于单质的电子式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)典型物质的电子式
NH4Cl:__________ Na2O2:________ CO2:___________ -OH:__________
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为_______ 。
(3)石油的综合利用方法有四种,其中____ 的目的是提高轻质油的产量,_____ 主要是得到甲烷、乙烯、丙烯等化工原料,_______ 是从石油中获得苯、甲苯等化工原料。
(4)填写有机除杂试剂
C2H6(C2H4)__________
乙酸乙酯(乙酸或乙醇)_____
乙醇(水)____________
苯(溴)________________
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为_______
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为__________
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体__________
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛_____
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:_______
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:___
③苯的硝化反应____________
NH4Cl:
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为
(3)石油的综合利用方法有四种,其中
(4)填写有机除杂试剂
C2H6(C2H4)
乙酸乙酯(乙酸或乙醇)
乙醇(水)
苯(溴)
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:
③苯的硝化反应
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】本题分为选做题(a)、(b)两道平行题,分值一样,可根据高一课程学习情况选择其中一道题完成作答,若二道题均作答,则按(a)题给分。
(a)有H、N、O、Na、Cl五种短周期主族元素。
(1)写出氯离子的原子结构示意图________ ,写出水分子的电子式________ 。
(2)NH4NO3是_______ 化合物(填“离子”或“共价”)。
(3)氯气是有毒气体,写出用饱和氢氧化钠溶液吸收氯气的离子方程式:_____________ 。
(4)金属元素铁是中学化学常见元素,将铁单质浸入氯化铁溶液中,该反应的离子方程式为__________ 。
(5)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出电极反应式。

正极反应式:___________________ ,负极反应式:___________________ 。
(a)有H、N、O、Na、Cl五种短周期主族元素。
(1)写出氯离子的原子结构示意图
(2)NH4NO3是
(3)氯气是有毒气体,写出用饱和氢氧化钠溶液吸收氯气的离子方程式:
(4)金属元素铁是中学化学常见元素,将铁单质浸入氯化铁溶液中,该反应的离子方程式为
(5)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出电极反应式。

正极反应式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学用语、元素周期律等是我们学习元素及其化合物知识的重要工具。请按要求回答下列问题:
(1) 的电子式为
的电子式为___________ ;用电子式表示 的形成过程:
的形成过程:___________ 。
(2)现有XY、Z、W四种元素,其中Z元素的―1价离子和W元素的+1价离子的电子层结构都与氩元素相同,Y原子的M层有3个电子,Y原子的L层电子数恰好是X原子L层电子数的两倍。则X、Y、Z、W的元素符号依次为___________ 、___________ 、___________ 、___________ ;含等质子数的X原子与Z原子的个数之比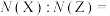
___________ ,写出W的最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物反应的离子方程式:___________ 。
(3)已知:氧族元素(不含Po)的部分知识如表所示。
①碲元素的主要化合价可能有___________ ;氧、硫、硒、碲原子半径逐渐___________ (填“增大”或“减小”)。
②氢硒酸( 的水溶液)有较强的还原性,因此露置在空气中长期保存易变质,其可能发生置换反应生成难溶于水的硒单质,则该置换反应的化学方程式为
的水溶液)有较强的还原性,因此露置在空气中长期保存易变质,其可能发生置换反应生成难溶于水的硒单质,则该置换反应的化学方程式为___________ 。
(1)
 的电子式为
的电子式为 的形成过程:
的形成过程:(2)现有XY、Z、W四种元素,其中Z元素的―1价离子和W元素的+1价离子的电子层结构都与氩元素相同,Y原子的M层有3个电子,Y原子的L层电子数恰好是X原子L层电子数的两倍。则X、Y、Z、W的元素符号依次为
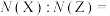
(3)已知:氧族元素(不含Po)的部分知识如表所示。
| 元素 |  (氧) (氧) | 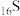 (硫) (硫) |  (硒) (硒) |  (碲) (碲) |
| 元素主要化合价 | ―2 | ―2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐 | |||
②氢硒酸(
 的水溶液)有较强的还原性,因此露置在空气中长期保存易变质,其可能发生置换反应生成难溶于水的硒单质,则该置换反应的化学方程式为
的水溶液)有较强的还原性,因此露置在空气中长期保存易变质,其可能发生置换反应生成难溶于水的硒单质,则该置换反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】科学工作者研发了一种 的系统,借助锂循环可持续合成氨,其原理如图所示:
的系统,借助锂循环可持续合成氨,其原理如图所示:
(1)过程Ⅰ得到Li3N的电子式为___________ 。
(2)过程Ⅱ生成W的化学反应方程式为____________ 。
(3)实验室制取氨气的化学反应方程式为___________ 。
 的系统,借助锂循环可持续合成氨,其原理如图所示:
的系统,借助锂循环可持续合成氨,其原理如图所示: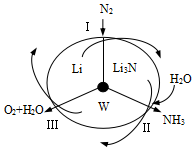
(1)过程Ⅰ得到Li3N的电子式为
(2)过程Ⅱ生成W的化学反应方程式为
(3)实验室制取氨气的化学反应方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】黄河是中华民族的母亲河,主要含有的离子有HCO 、SO
、SO 、Cl-、Ca2+、Mg2+、Na+。
、Cl-、Ca2+、Mg2+、Na+。
完成下列填空:
(1)上述离子所涉及元素:某元素原子的K层与M层电子数之和等于L层上电子数,其简单离子的电子式为_______________ ,与该离子具有相同电子数的四核微粒有______ (写出2种)。
(2)为了确定黄河水中的负离子,某研究小组进行了如下实验,请你参与探究与分析。
(3)某制碱工厂的废液中含有大量OH-,会对黄河原有的哪些离子产生影响:__________ 。
(4)工厂常利用石灰乳做高浓度含氟离子废水的处理剂。已知:氟化钙难溶于水,请写出石灰乳用于处理含氟离子废水的离子方程式。_________________________________
(5)某金属矿场的废液中含Au3+,可以在强碱性条件下,用NaBH4(已知H为-1价)处理,生成单质Au。已知:反应后硼元素以BO 形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。
形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。_____ 。
___Au3++___BH +__ ______=______+__ ______+__H2O
+__ ______=______+__ ______+__H2O
 、SO
、SO 、Cl-、Ca2+、Mg2+、Na+。
、Cl-、Ca2+、Mg2+、Na+。完成下列填空:
(1)上述离子所涉及元素:某元素原子的K层与M层电子数之和等于L层上电子数,其简单离子的电子式为
(2)为了确定黄河水中的负离子,某研究小组进行了如下实验,请你参与探究与分析。
| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 取样,滴加过量的HNO3溶液 | 检验 | |
| 第二步 | 再滴加过量的 | 检验 的存在 的存在 | Ba2++SO =BaSO4↓ =BaSO4↓ |
| 第三步 | 过滤,取滤液少许,滴加 | 检验 | Ag++Cl-=AgCl↓ |
黄河流域沿途工业污水的任意排放是造成黄河水质恶化的最大隐患。
(3)某制碱工厂的废液中含有大量OH-,会对黄河原有的哪些离子产生影响:
(4)工厂常利用石灰乳做高浓度含氟离子废水的处理剂。已知:氟化钙难溶于水,请写出石灰乳用于处理含氟离子废水的离子方程式。
(5)某金属矿场的废液中含Au3+,可以在强碱性条件下,用NaBH4(已知H为-1价)处理,生成单质Au。已知:反应后硼元素以BO
 形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。
形式存在,反应前后硼元素化合价不变,且无气体生成。补全下列方程式并配平。___Au3++___BH
 +__ ______=______+__ ______+__H2O
+__ ______=______+__ ______+__H2O
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】在宏观、微观和符号之间建立联系是化学学科特点。
(1)在水、铜、氯化钠3种物质中,由离子构成的是___________ 。
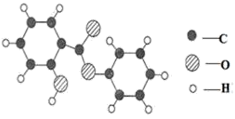
(2)撒罗(salol)是一种消毒剂,其分子模型如图所示,该物质的一个分子中含有___ 个原子,撒罗(salol)中氢元素与氧元素的质量比为_______ 。
(3)A、B、C、D表示4种物质,部分物质的微观示意图如下,A和B在一定条件下反应生成C和D。
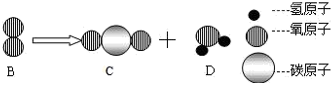
A、B、C、D中属于单质的是_______ (填化学式,下同);属于氧化物的是_____ 。
(4)某粒子的结构示意图为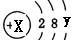 ,当x-y=8时,该粒子为
,当x-y=8时,该粒子为________ 。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是__________ 。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43- 和SO42-
(1)在水、铜、氯化钠3种物质中,由离子构成的是
(2)撒罗(salol)是一种消毒剂,其分子模型如图所示,该物质的一个分子中含有

(3)A、B、C、D表示4种物质,部分物质的微观示意图如下,A和B在一定条件下反应生成C和D。

A、B、C、D中属于单质的是
(4)某粒子的结构示意图为
 ,当x-y=8时,该粒子为
,当x-y=8时,该粒子为(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43- 和SO42-
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】H2O2、KCl、Na2SO4、Na2O2、HCl、O2中只含离子键的是___ ,只含极性键的是___ ,只含非极性键的是___ ,既含离子键又含极性键的是___ ,既含离子键又含非极性键的是___ ,既极性键含又含非极性键的是________ 。
您最近半年使用:0次
【推荐3】填空。
(1)ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。Fe[Zn(OH)Cl2]2的水溶液中不存在的微粒间作用力有_______ (填选项字母)
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
(2)NH3、PH3和AsH3的沸点由高到低的顺序是_______ 。
(3)N(CH3)3和P(CH3)3是重要的化工原料。N(CH3)3中N原子的杂化方式为_______ ;键角C—N—C大于C—P—C的原因是_______ 。
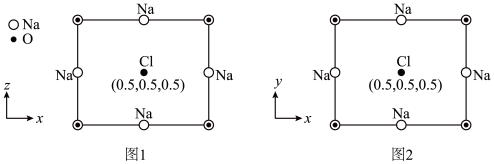
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。Na3OCl属立方晶系(正方体形),晶胞参数为apm。晶胞沿y轴和沿z轴投影的各原子的分布图和原子分数坐标分别如图1、图2所示。据此推断该晶胞中Na原子的数目为_______ 。设NA为阿伏加德罗常数的值,则Na3OC1晶体的密度为_______ g·cm-3(用代数式表示)。
(1)ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。Fe[Zn(OH)Cl2]2的水溶液中不存在的微粒间作用力有
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
(2)NH3、PH3和AsH3的沸点由高到低的顺序是
(3)N(CH3)3和P(CH3)3是重要的化工原料。N(CH3)3中N原子的杂化方式为
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。Na3OCl属立方晶系(正方体形),晶胞参数为apm。晶胞沿y轴和沿z轴投影的各原子的分布图和原子分数坐标分别如图1、图2所示。据此推断该晶胞中Na原子的数目为

您最近半年使用:0次


 B.
B.