H2O2、KCl、Na2SO4、Na2O2、HCl、O2中只含离子键的是___ ,只含极性键的是___ ,只含非极性键的是___ ,既含离子键又含极性键的是___ ,既含离子键又含非极性键的是___ ,既极性键含又含非极性键的是________ 。
更新时间:2016-07-01 11:48:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有短周期A,B,C三种元素,原子序数依次增大,A元素的单质是密度最小的气体,B获得2个电子可达到稳定结构,C与A同主族。
(1)判断A,B,C各为何种元素。A____ ,B____ ,C____ 。
(2)用电子式表示三种元素原子之间可能构成的化合物的形成过程,若含共价键请指出共价键是σ键还是π键,并标明该键的个数。
①A与B:___________________________________________________ 。
②A与C:___________________________________________________ 。
③B与C:___________________________________________________ 。
④A,B,C:___________________________________________________ 。
(1)判断A,B,C各为何种元素。A
(2)用电子式表示三种元素原子之间可能构成的化合物的形成过程,若含共价键请指出共价键是σ键还是π键,并标明该键的个数。
①A与B:
②A与C:
③B与C:
④A,B,C:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)现有以下物质:①NaOH固体②盐酸③CaCO3固体④熔融 KCl⑤蔗糖⑥铜⑦NH3⑧液态的HCl,以上物质中能导电的是___________ ;(填序号,下同);以上物质中属于非电解质的是___________ 。
(2)现有以下物质:
①氩气 ②NaOH③AlCl3④BaCl2 ⑤硫酸 ⑥NH3 ⑦CCl4 ⑧H2O2,
a.以上物质中只含离子键的物质是___________ (填序号,下同);含非极性键的物质是___________ ;含有共价键的离子化合物是___________ ;
b.用电子式表示⑧的形成过程___________ 。
(1)现有以下物质:①NaOH固体②盐酸③CaCO3固体④熔融 KCl⑤蔗糖⑥铜⑦NH3⑧液态的HCl,以上物质中能导电的是
(2)现有以下物质:
①氩气 ②NaOH③AlCl3④BaCl2 ⑤硫酸 ⑥NH3 ⑦CCl4 ⑧H2O2,
a.以上物质中只含离子键的物质是
b.用电子式表示⑧的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(8分)将A.F2、B.CH4、C.MgO、D.SiO2、E.NaOH五种物质按要求填空:
(1)属于离子化合物的是_______________ ,属于共价分子的_____________
属于共价化合物的是_______________ ,只有离子键的物质是_________
(2)由原子直接构成的化合物是____________________ 。
(1)属于离子化合物的是
属于共价化合物的是
(2)由原子直接构成的化合物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Na、Mg、Al、Fe 、Cu是中学阶段常见的几种重要金属元素,请回答以下问题:
(1)Fe在周期表中第____ 周期,第____ 族;它的核外电子排布式:_________ ;
(2)Al的价电子轨道表示式:____________ ;与其同族中第四周期的元素名称,元素符号____ 。
(3)Mg的原子结构示意图:____________ ; Na、Mg、Al第一电离能的由大到小顺序:___________ (用元素符号表示)
(4)Cu2+的未成对电子数:____ ,在硫酸铜溶液中通入氨气直至过量发生的化学反应_____________________________________________ (写离子方程式),小心蒸发,最终得到的[Cu(NH3)4]SO4晶体中含有的化学键除了普通共价键外,还有________ 和________ 。
(1)Fe在周期表中第
(2)Al的价电子轨道表示式:
(3)Mg的原子结构示意图:
(4)Cu2+的未成对电子数:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填空:(填序号,下同)
(1)A NH4Cl B KCl C H2S D F2 E NaOH F H2O2 G Na2O2
①属于共价化合物的是;___________
②只含有离子键的是;___________
③既含有离子键又含有共价键的是_____________
(2)在下列变化中,①I2升华,②烧碱熔化,③NaCl溶于水, ④HCl溶于水,⑤O2溶于水,⑥Na2O2溶于水,未发生化学键破坏的是____ ;仅发生离子键破坏的是___ ;仅发生共价键破坏的是____ ;既发生离子键破坏,又发生共价键破坏的是____ 。
(3)现有A: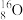 、
、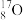 、
、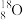 ;B:H2、D2、T2;C:石墨、金刚石;D:
;B:H2、D2、T2;C:石墨、金刚石;D: 、
、 、
、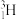
四组微粒或物质,回答下列问题:①互为同位素的是_______ (填字母序号,下同)。 ②互为同素异形体的是________ 。
(1)A NH4Cl B KCl C H2S D F2 E NaOH F H2O2 G Na2O2
①属于共价化合物的是;
②只含有离子键的是;
③既含有离子键又含有共价键的是
(2)在下列变化中,①I2升华,②烧碱熔化,③NaCl溶于水, ④HCl溶于水,⑤O2溶于水,⑥Na2O2溶于水,未发生化学键破坏的是
(3)现有A:
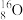 、
、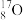 、
、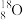 ;B:H2、D2、T2;C:石墨、金刚石;D:
;B:H2、D2、T2;C:石墨、金刚石;D: 、
、 、
、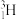
四组微粒或物质,回答下列问题:①互为同位素的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,通常水加热至100℃时变为水蒸气,加热至2000℃会缓慢分解为 和
和 ,从粒子间的相互作用角度进行分析,这两种变化有所不同。
,从粒子间的相互作用角度进行分析,这两种变化有所不同。
(1)水加热至100℃变为水蒸气时,破坏的粒子间的相互作用包含_______ ,加热至2000℃分解为 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是_______ 。
(2)以上三种作用力由大到小的顺序是_______ 。
(3)H、 、
、 半径由大到小的顺序是
半径由大到小的顺序是_______ 。
 和
和 ,从粒子间的相互作用角度进行分析,这两种变化有所不同。
,从粒子间的相互作用角度进行分析,这两种变化有所不同。(1)水加热至100℃变为水蒸气时,破坏的粒子间的相互作用包含
 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是(2)以上三种作用力由大到小的顺序是
(3)H、
 、
、 半径由大到小的顺序是
半径由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质的分类是学习化学的一种重要方法,下列物质:①Cu,②KCl固体,③NaHSO4溶液、④Cu(OH)2溶液、⑤浓盐酸、⑥CO2、⑦熔融的FeCl3、⑧Na2O2粉末。
(1)能导电的物质是_____ (填序号,下同),属于电解质的是_____ ,属于共价化合物的是_____ ,既含离子键又含非极性键的化合物是_____ 。
(2)写出向③中滴加Ba(OH)2溶液至SO 完全沉淀的离子方程式:
完全沉淀的离子方程式:_____ 。
(3)ClO2是一种新型的水处理剂,可通过多种方法制取,如:
①2KClO3+4HCl(浓)=2KCl+2ClO2+Cl2↑+2H2O;
②Cl2+2KClO2=2KCl+2ClO2。
反应①中还原剂是_____ ,反应②的氧化产物与还原产物的物质的量之比是_____ 。
(1)能导电的物质是
(2)写出向③中滴加Ba(OH)2溶液至SO
 完全沉淀的离子方程式:
完全沉淀的离子方程式:(3)ClO2是一种新型的水处理剂,可通过多种方法制取,如:
①2KClO3+4HCl(浓)=2KCl+2ClO2+Cl2↑+2H2O;
②Cl2+2KClO2=2KCl+2ClO2。
反应①中还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答问题
(1)1 mol HCHO分子中含有σ键的数目为_______ NA。
(2)CS2分子中,共价键的类型有_______ 。
(3)下列物质中:①MgCl2;②Na2O2; ③CS2 ;④NaOH; ⑤H2,只存在极性键的是_______ (填序号,下同),只存在非极性键的是_______ ,只存在离子键的是_______ ,既存在离子键又存在极性共价键的是_______ ,既存在离子键又存在非极性共价键的是_______ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:①MgCl2;②Na2O2; ③CS2 ;④NaOH; ⑤H2,只存在极性键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)有以下8种物质:①Ne②HCl③P4④H2O2⑤Na2S⑥NaOH⑦Na2O2⑧NH4Cl请用上述物质的序号填空:
①不存在化学键的是____ 。
②只存在极性共价键的是___ 。
③只存在非极性共价键的是___ 。
④既存在非极性共价键又存在极性共价键的是___ 。
⑤只存在离子键的是___ 。
⑥既存在离子键又存在共价键的是___ 。
(2)在下列变化中:①I2升华②烧碱熔化 ③NaCl溶于水④HCl溶于水⑤O2溶于水⑥Na2O2溶于水。
①未破坏化学键的是___ (填序号,下同);②仅离子键被破坏的是____ ;
③仅共价键破破坏的是___ ;④离子键和共价键同时被破坏的是____ 。
①不存在化学键的是
②只存在极性共价键的是
③只存在非极性共价键的是
④既存在非极性共价键又存在极性共价键的是
⑤只存在离子键的是
⑥既存在离子键又存在共价键的是
(2)在下列变化中:①I2升华②烧碱熔化 ③NaCl溶于水④HCl溶于水⑤O2溶于水⑥Na2O2溶于水。
①未破坏化学键的是
③仅共价键破破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】核外电子排布与化学键。在含有多个电子的原子例,电子的能量不同,根据电子能量的差异,电子应先排布在能量最低的电子层例,然后再依次由里向外排布在能量逐渐升高的电子层例,即分层排布。亨利·莫斯莱和查尔斯·巴克拉的X-射线吸收研究首次与实验中发现电子层。巴克拉把他们称为K、L、M、N(以英文字母排列)等电子层,这些字母后来被n值1、2、3等取代。
(1)结构示意图可以简明地表示微粒的核外电子排布,是一种用于表示原子或离子整体结构的图示。电子式是一类反应原子最外层电子情况,以及微粒之间化学键种类的化学语言。下列表示式正确的是___________
(2)在1916年,G.N。Lewis在讲述他的化学键理论时提出了电子式,故电子式又被称为路易斯式。根据经典的共价键理论,在形成化合物时,原子核外的单电子要尽可能地进行配对,并达到8电子稳定结构(H为2电子稳定结构)。写出 的电子式:
的电子式:___________ 。
(3)在元素周期表中,原子按核电荷数和原子核外电子排布的周期性变化进行排列。一些元素的原子易失去电子或得到电子形成离子,使最外层达到稳定结构。

如表所示是元素周期表的一部分,A、B、C均为短周期元素。已知B、C原子核外电子数之和是A原子核外电子数的4倍,则以下叙述中正确的是___________
(4)化学键(chemical bond)是纯净物分子内或晶体内相邻两个或多个原子(或离子)间强烈的相互作用力的统称。常见的化学键有离子键和共价键。离子键是由正离子和负离子之间相互的静电作用力形成的。共价键是由两个或多个原子共同使用他们的外层电子,在理想的情况下达到电子饱和状态,由此组成比较稳定的化学结构。在下列物质中:
①Ar ②SiC ③NaCl ④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦
其中,存在离子键的物质有___________ (填编号,下同),存在共价键的物质有___________ 。
(5)一般来说,主族元素的性质会随原子序数增加而呈现的变化,称为元素周期律。元素的非金属性表现为元素原子的得电子能力,元素非金属越的强弱会影响非金属单质的氧化性、气态氢化物的稳定性等等。下列物质的性质与解释均正确,且对应关系也正确的是___________
(1)结构示意图可以简明地表示微粒的核外电子排布,是一种用于表示原子或离子整体结构的图示。电子式是一类反应原子最外层电子情况,以及微粒之间化学键种类的化学语言。下列表示式正确的是
A.硫离子的结构示意图: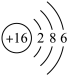 | B.钾原子的结构示意图: |
C.氯离子的电子式: | D.镁离子的电子式: |
 的电子式:
的电子式:(3)在元素周期表中,原子按核电荷数和原子核外电子排布的周期性变化进行排列。一些元素的原子易失去电子或得到电子形成离子,使最外层达到稳定结构。

如表所示是元素周期表的一部分,A、B、C均为短周期元素。已知B、C原子核外电子数之和是A原子核外电子数的4倍,则以下叙述中正确的是
| A.A、B、C都是非金属元素 | B.A、B、C最高价氧化物的水化物均为强酸 |
| C.A、B、C三种核电荷数之和是39 | D.B与A、C均能形成离子化合物 |
①Ar ②SiC ③NaCl ④
 ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦
其中,存在离子键的物质有
(5)一般来说,主族元素的性质会随原子序数增加而呈现的变化,称为元素周期律。元素的非金属性表现为元素原子的得电子能力,元素非金属越的强弱会影响非金属单质的氧化性、气态氢化物的稳定性等等。下列物质的性质与解释均正确,且对应关系也正确的是
| 选项 | 性质 | 解释 |
| A | 还原性: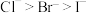 | Cl、Br、I的非金属性依次减弱 |
| B | 沸点: | N的非金属性比P强 |
| C | 分解温度: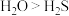 | O的非金属性比S强 |
| D | 酸性: | Cl的非金属比S强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。完成下列填空:
。完成下列填空:
(1)写出 的电子式:
的电子式:_______ 。
(2) 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是_______ 。
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是_______ (填写化学式),所涉及的5种元素中,原子半径最大的是_______ (填写元素符号)。
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: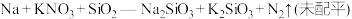 。
。
(4)写出配平后完整的化学方程式_______ 。
(5)结合金属钠的化学性质,说明汽车安全气囊中填充 、
、 的目的
的目的_______ 。
(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的 质量是
质量是_______ (N-14 Na-23)。
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。完成下列填空:
。完成下列填空:(1)写出
 的电子式:
的电子式:(2)
 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是(3)汽车安全气囊填充物的三种物质中属于共价化合物的是
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: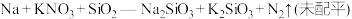 。
。(4)写出配平后完整的化学方程式
(5)结合金属钠的化学性质,说明汽车安全气囊中填充
 、
、 的目的
的目的(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的
 质量是
质量是
您最近一年使用:0次



