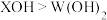下表是部分短周期元素的原子半径及主要化合价,请判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.090 | 0.102 | 0.073 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.A2+与D2-的核外电子数相等 |
| B.B3+是其所在周期中所有常见离子中半径最小的 |
| C.氢化物的稳定性为H2E<H2D |
| D.在相同条件下,单质与同浓度的稀盐酸反应的剧烈程度为B>A |
18-19高一上·山东济南·期末 查看更多[4]
湖南省湘潭市第一中学2022-2023学年高二下学期第一次月考化学试题四川省眉山市彭山区第一中学2020-2021学年高一4月月考化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)山东省济南市山东师范大学附属中学2018-2019学年高一上学期第二次学分认定考试(期末)化学试题
更新时间:2021-04-20 14:56:38
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】主族元素W、X、Y、Z四种位于同一周期,原子序数依次增大,W、X是金属元素,Y、Z是非金属元素。W、X的最高价氧化物对应的水化物可以相互反应,W与Y可形成化合物W2Y,Y的最外层电子数是核外电子层数的2倍。下列说法正确的是
| A.Y的气态氢化物比Z的气态氢化物稳定 |
| B.W的最高价氧化物对应的水化物为中强碱 |
| C.Y的单质和氧气、氢气都能发生化合反应,且产物都具有还原性 |
| D.W、X、Y、Z四种元素的原子半径有小到大的顺序是:W<X<Y<Z |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列性质的比较,不能用元素周期律解释的是
| A.稳定性:HF>HI |
| B.金属性:铁和硫酸铜溶液反应置换出铜 |
| C.碱性:KOH>NaOH |
| D.酸性:HCl>H2S |
您最近一年使用:0次
【推荐1】下列说法正确的是
A. 和 和 所含化学键类型完全相同 所含化学键类型完全相同 |
B. 比 比 稳定是因为 稳定是因为 分子间存在氢键 分子间存在氢键 |
| C.分子的稳定性与分子间作用力无关 |
D.原子序数大于4的短周期元素 和 和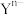 两种离子的电子排布式相同,则X的原子半径比Y小, 两种离子的电子排布式相同,则X的原子半径比Y小, 的离子半径比 的离子半径比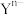 大 大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、W原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示,Z的原子半径在短周期中最大,W基态原子的s能级电子总数是p能级电子总数的2/3。
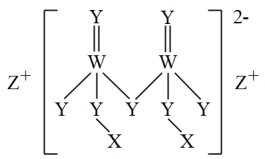
下列说法不正确的是

下列说法不正确的是
| A.Y、Z形成的简单离子半径: Y> Z |
| B.W、Y形成的简单氢化物沸点: Y > W |
| C.Z分别与X、Y形成的化合物中所含化学键类型一定完全相同 |
| D.WX3、X2Y中W原子和Y原子的杂化轨道类型相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】M、X、Y、Z为原子序数依次增大的短周期主族元素,其中M、Z位于同一主族,Z的最高价含氧酸为强酸。M、Z的原子序数之和是X的2倍,Y的最外层电子数等于Z和X的最外层电子数之差。下列叙述正确的是
| A.氢化物沸点:M<Z | B.原子半径:M<X<Y<Z |
| C.工业上用电解法制备单质X | D.华为芯片的主要成分为Y的氧化物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E的原子序数依次增大,A原子是主族元素中原子半径最小的,B原子的最外层电子数等于其次外层电子数3倍,C元素是地壳中含量最高的金属元素,D的最高价氧化物对应水化物的化学式为HnDO2n+2,E有两种常见简单离子,低价离子为绿色。下列说法错误的是
| A.E为过渡元素 |
| B.不能采用电解熔融的CD3的方式制取C的单质 |
| C.简单离子半径:A<B<C<D |
| D.C与D的最高价氧化物的水化物之间可以反应 |
您最近一年使用:0次

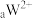 、
、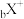 、
、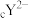 、
、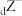 都具有相同的电子层结构,下列推断错误的是
都具有相同的电子层结构,下列推断错误的是