填写下列空格:
(1)写出正丁烷的结构简式_______ 。
(2)金刚石的晶体类型_______ 。
(3)下述属于取代反应的是_______ ;属于加成反应的是_______ 。
A.乙烯使溴水褪色 B.乙烯使酸性高锰酸钾溶液褪色
C.苯与浓硝酸制硝基苯 D.乙醇与金属钠反应
(1)写出正丁烷的结构简式
(2)金刚石的晶体类型
(3)下述属于取代反应的是
A.乙烯使溴水褪色 B.乙烯使酸性高锰酸钾溶液褪色
C.苯与浓硝酸制硝基苯 D.乙醇与金属钠反应
更新时间:2021-04-24 10:33:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷作为溶剂,其中分子结构为正四面体的是____________ ,工业上分离这些多氯代甲烷的方法是__________________ ;
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式:__________________________ (不考虑立体异构);
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
乙烯 1,2-二氯乙烷
1,2-二氯乙烷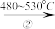 氯乙烯
氯乙烯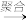 聚氯乙烯
聚氯乙烯
反应①的化学方程式是______________________ ,反应类型为____________ ,反应②的反应类型为________________ 。
(1)多氯代甲烷作为溶剂,其中分子结构为正四面体的是
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式:
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
乙烯
 1,2-二氯乙烷
1,2-二氯乙烷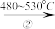 氯乙烯
氯乙烯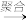 聚氯乙烯
聚氯乙烯反应①的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列反应的化学方程式:
(1)乙烯使溴水褪色的反应__________ ,反应类型__________
(2)苯→硝基苯__________ ,反应类型__________
(3)在碱性条件下乙醛与新制的Cu(OH)2反应__________ ,反应类型__________
(1)乙烯使溴水褪色的反应
(2)苯→硝基苯
(3)在碱性条件下乙醛与新制的Cu(OH)2反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】乙烯是石油化工最重要的化工原料,其产品可用于现代社会各个领域。
(1)乙烯的分子式是___________ ,含有的官能团是___________ 。
(2)乙烯和水反应可制取乙醇,写出乙醇的结构简式___________ 。
(3)实验室用乙醇来制取乙烯,该反应的反应类型是___________ 反应。
(4)乙烯的用途很广泛,请写出它的一种用途___________ 。
(5)酒中含有乙醇,乙醇在人体内通过酶的作用先氧化为A,A再氧化为B,最后转化为CO2和H2O。写出A、B的名称:A___________ 、B___________ 。
(1)乙烯的分子式是
(2)乙烯和水反应可制取乙醇,写出乙醇的结构简式
(3)实验室用乙醇来制取乙烯,该反应的反应类型是
(4)乙烯的用途很广泛,请写出它的一种用途
(5)酒中含有乙醇,乙醇在人体内通过酶的作用先氧化为A,A再氧化为B,最后转化为CO2和H2O。写出A、B的名称:A
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示表示页岩气中某些烃类的结构模型:
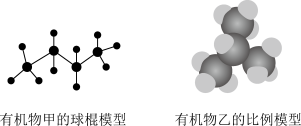
(1)有机物甲的名称为____________ ,有机物甲与有机物乙互为____________ 。
(2)有机物乙的一氯取代物有________ 种,请你根据甲烷分子结构示意图推测,有机物乙中最多有________ 个C原子在同一平面内。

(1)有机物甲的名称为
(2)有机物乙的一氯取代物有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合 制氢为例,反应为
制氢为例,反应为 。
。
①NaH的电子式为___________ ;
②在化学方程式上标出该反应中电子转移的方向与数目___________ 。
(2)甲烷重整制氢。主要反应为: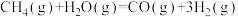 ;
;
① 中氢元素的质量分数为
中氢元素的质量分数为___________ ,是含氢量最高的有机物;甲烷重整制氢是我国目前最主要的制氢来源。
②碳元素在周期表中的位置为___________ ;当1个碳原子与其他4个原子连接时,这个碳原子将采取___________ (填“空间构型”)取向与之成键形成稳定结构,使得烷烃性质稳定。
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为___________ ;该异辛烷的结构简式为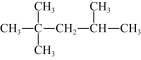 ,用系统命名法命名该有机物
,用系统命名法命名该有机物___________ ;写出同时满足下列条件的正庚烷的一种同分异构体的结构简式:___________ (a.一个支链,b.该物质在光照下与氯气取代的一氯代物有3种)。
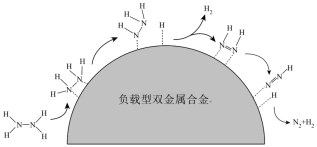
(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼( )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为___________ 。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合
 制氢为例,反应为
制氢为例,反应为 。
。①NaH的电子式为
②在化学方程式上标出该反应中电子转移的方向与数目
(2)甲烷重整制氢。主要反应为:
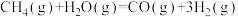 ;
;
①
 中氢元素的质量分数为
中氢元素的质量分数为②碳元素在周期表中的位置为
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为
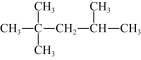 ,用系统命名法命名该有机物
,用系统命名法命名该有机物(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼(
 )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某烃A的相对分子质量为84。回答下列问题:
(1)烃A的分子式为_________ 。
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为__________ 。若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________ 。若烃B的相对分子质量比烃A小6,且B为最简单芳香族化合物,写出B与浓硝酸,浓硫酸混合共热的化学方程式__________
(1)烃A的分子式为
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列3种有机化合物A:CH2=CH2、B: 、C:CH3COOH。
、C:CH3COOH。
(1)写出化合物A、C中官能团的名称:_______ 、_______ 。
(2)3种化合物中能使溴的四氯化碳溶液褪色的是_______ (写名称),该反应的化学方程式为_______ 。该物质在农业上用作水果的_______ 。
(3)B的名称是_______ ,它的分子具有_______ (填分子构型)结构,是否存在单双键交替结构?_______ (填“是”或“否”)。
(4)写出下列有机化学反应的化学方程式。
①苯、浓硫酸与浓硝酸混合在50-60℃的水浴中加热:_______ 。
②乙醇在铜作催化剂、加热的条件下与氧气的反应:_______ 。
 、C:CH3COOH。
、C:CH3COOH。(1)写出化合物A、C中官能团的名称:
(2)3种化合物中能使溴的四氯化碳溶液褪色的是
(3)B的名称是
(4)写出下列有机化学反应的化学方程式。
①苯、浓硫酸与浓硝酸混合在50-60℃的水浴中加热:
②乙醇在铜作催化剂、加热的条件下与氧气的反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某烃A的相对分子质量为84。回答下列问题:
(1)烃A的分子式为_________ 。下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是_____ ;若总质量一定,充分燃烧消耗氧气的量不变的是____ 。
A. C7H8 B.C6H14 C.C7H14 D.C8H8
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为__________ 。若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________ 。若烃B的相对分子质量比烃A小6,且B为最简单芳香族化合物,写出B与浓硝酸,浓硫酸混合共热的化学方程式__________
(3)如图:
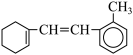
①该物质与足量氢气完全加成后环上一氯代物有________ 种;
②该物质和溴水反应,消耗Br2的物质的量为_______ mol;
③该物质和H2加成需H2________ mol;
(4)如图是辛烷的一种结构M(只画出了碳架,没有画出氢原子)按下列要求,回答问题:
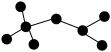
①用系统命名法命名________ 。
②M的一氯代物有________ 种。
③M是由某烯烃加成生成的产物,则该烯烃可能有_______ 种结构。
(1)烃A的分子式为
A. C7H8 B.C6H14 C.C7H14 D.C8H8
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为
(3)如图:
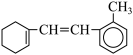
①该物质与足量氢气完全加成后环上一氯代物有
②该物质和溴水反应,消耗Br2的物质的量为
③该物质和H2加成需H2
(4)如图是辛烷的一种结构M(只画出了碳架,没有画出氢原子)按下列要求,回答问题:

①用系统命名法命名
②M的一氯代物有
③M是由某烯烃加成生成的产物,则该烯烃可能有
您最近一年使用:0次
【推荐1】(1)比较给出H+的能力的相对强弱:H2CO3___ C6H5OH(填“>”、“<”或“=”);用一个离子方程式说明CO32‾和C6H5O‾结合H+能力的相对强弱___ 。
(2)Ca(CN)2是离子化合物,各原子均满足8电子稳定结构。写出Ca(CN)2的电子式___ 。
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是___ 。
(2)Ca(CN)2是离子化合物,各原子均满足8电子稳定结构。写出Ca(CN)2的电子式
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是
您最近一年使用:0次
【推荐2】C60、金刚石和石墨的结构模型如图所示(石墨仅表示出其中的一层结构)。
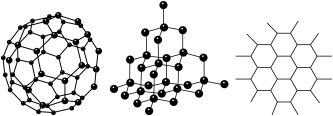
(1)C60、金刚石和石墨三者的关系互为________ 。
A.同分异构体 B.同素异形体
C.同系物 D.同位素
(2)固态时,C60属于________ 晶体(填“离子”、“原子”或“分子”),C60分子中含有双键的数目是________ 个。
(3)硅晶体的结构跟金刚石相似,1 mol硅晶体中含有硅硅单键的数目约是________ NA个。二氧化硅的结构相当于在硅晶体结构中每个硅硅单键之间插入1个氧原子,二氧化硅的空间网状结构中,硅、氧原子形成的最小环上氧原子数目是________ 个。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是________ 个。

(1)C60、金刚石和石墨三者的关系互为
A.同分异构体 B.同素异形体
C.同系物 D.同位素
(2)固态时,C60属于
(3)硅晶体的结构跟金刚石相似,1 mol硅晶体中含有硅硅单键的数目约是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳形成的化合物种类繁多,硅是构成地壳岩石的主要元素。碳在自然界有两种稳定的同位素,有关数据如下表:
请列出碳元素近似相对原子质量的计算式_____________________________________ 。
(1)Si原子的14个电子排布在_______ 个能级上;与硅元素同周期、其原子核外有2个未成对电子的元素的最外层电子排布式为_____________ 。
(2)SiO2用途广泛,以下叙述错误的是______________ 。
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是___________ 。
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式___________ ,写成盐的形式__________ 。
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式____________________________________________ 。
| 同位素 | 相对原子质量 | 丰度(原子分数) |
| 12C | 12(整数,相对原子质量的基准) | 0.9893 |
| 13C | 13.003354826 | 0.0107 |
请列出碳元素近似相对原子质量的计算式
(1)Si原子的14个电子排布在
(2)SiO2用途广泛,以下叙述错误的是
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式
您最近一年使用:0次



