氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合 制氢为例,反应为
制氢为例,反应为 。
。
①NaH的电子式为___________ ;
②在化学方程式上标出该反应中电子转移的方向与数目___________ 。
(2)甲烷重整制氢。主要反应为: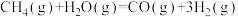 ;
;
① 中氢元素的质量分数为
中氢元素的质量分数为___________ ,是含氢量最高的有机物;甲烷重整制氢是我国目前最主要的制氢来源。
②碳元素在周期表中的位置为___________ ;当1个碳原子与其他4个原子连接时,这个碳原子将采取___________ (填“空间构型”)取向与之成键形成稳定结构,使得烷烃性质稳定。
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为___________ ;该异辛烷的结构简式为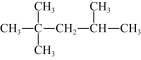 ,用系统命名法命名该有机物
,用系统命名法命名该有机物___________ ;写出同时满足下列条件的正庚烷的一种同分异构体的结构简式:___________ (a.一个支链,b.该物质在光照下与氯气取代的一氯代物有3种)。
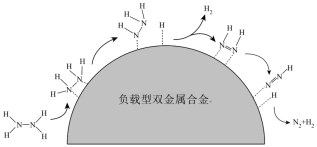
(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼( )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为___________ 。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合
 制氢为例,反应为
制氢为例,反应为 。
。①NaH的电子式为
②在化学方程式上标出该反应中电子转移的方向与数目
(2)甲烷重整制氢。主要反应为:
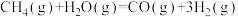 ;
;
①
 中氢元素的质量分数为
中氢元素的质量分数为②碳元素在周期表中的位置为
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为
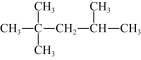 ,用系统命名法命名该有机物
,用系统命名法命名该有机物(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼(
 )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为
更新时间:2023-04-22 11:40:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼 的是___ (填元素符号)。
(2)③的气态氢化物的电子式___ ,②④形成的气态化合物的结构式___ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为___ (填物质的化学式),写出它的电子式:___ ;酸性最强的含氧酸为___ (填物质的化学式),写出它的电离方程式:___ 。
(4)在②和③两种元素中,非金属性较强的是___ (填元素名称),②的单质可以和③的最高价氧化物的水化物反应,请写出有关化学方程式___ 。
(5)②与Si元素分别形成的最高价氧化物,___ 的熔点更高,原因是___ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
(4)在②和③两种元素中,非金属性较强的是
(5)②与Si元素分别形成的最高价氧化物,
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)比较O与N的第一电离能大小为:O____ N(填“>”、“=”或“<”)。
(2)写出Ca(NH2)2电子式____ 。
(3)写出Sc元素原子的电子排布式____ 。
(1)比较O与N的第一电离能大小为:O
(2)写出Ca(NH2)2电子式
(3)写出Sc元素原子的电子排布式
您最近半年使用:0次
【推荐1】按要求填空。
(1)配平下面氧化还原离子方程式:_______ 。
______Cu+___H++___ =____Cu2+____NO↑+____
=____Cu2+____NO↑+____
(2)已知KMnO4与浓盐酸室温下可发生如下反应: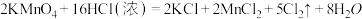
①用“双线桥法”标出上述反应的电子转移情况_______ ;
②此反应体现HCl的_______ 性和_______ 性;
③该反应中,被氧化的氯原子个数与未被氧化的氯原子个数比为_______ 。
④已知:KMnO4溶液酸化采用硫酸而不用盐酸,能结合上述化学方程式,用文字解释酸化KMnO4为什么不用盐酸?_______ 。
(1)配平下面氧化还原离子方程式:
______Cu+___H++___
 =____Cu2+____NO↑+____
=____Cu2+____NO↑+____
(2)已知KMnO4与浓盐酸室温下可发生如下反应:
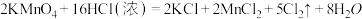
①用“双线桥法”标出上述反应的电子转移情况
②此反应体现HCl的
③该反应中,被氧化的氯原子个数与未被氧化的氯原子个数比为
④已知:KMnO4溶液酸化采用硫酸而不用盐酸,能结合上述化学方程式,用文字解释酸化KMnO4为什么不用盐酸?
您最近半年使用:0次
【推荐2】I.某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr (OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________ 。
(2)该反应中,发生还原反应的过程是________ →________ 。
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:__________ 。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________ 。
II.从定性分析到定量研究是高中生化学学习的重要发展历程。请你根据所学知识对以下化学问题进行定量分析。
(5)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol, 则转移的电子数为__________ , 被氧化的N原子的物质的量为__________ 。
(6)实验室需要为无土栽培配制1 L内含0.24 mol K2SO4、0.5 mol NH4Cl、0.16 mol KCl的某营养液。某小组计划用(NH4)2SO4、KCl、NH4Cl配制,则需这三种固体的物质的量分别为_________ 、_________ 、_________ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
II.从定性分析到定量研究是高中生化学学习的重要发展历程。请你根据所学知识对以下化学问题进行定量分析。
(5)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol, 则转移的电子数为
(6)实验室需要为无土栽培配制1 L内含0.24 mol K2SO4、0.5 mol NH4Cl、0.16 mol KCl的某营养液。某小组计划用(NH4)2SO4、KCl、NH4Cl配制,则需这三种固体的物质的量分别为
您最近半年使用:0次
【推荐3】填空。
(1)请完成并配平如下化学方程式,再用双线桥 标明电子转移的方向和数目: ,
,___________ 。HBr在上述反应中体现的性质有_____ 、____ ,氧化剂与还原剂的物质的量之比为______ 。
(2)NaH可在野外作生氢剂。反应原理为 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)工业废水中的 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为Cr3+,反应的离子方程式
转化为Cr3+,反应的离子方程式___________ 。
(1)请完成并配平如下化学方程式,再用
 ,
,(2)NaH可在野外作生氢剂。反应原理为
 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)工业废水中的
 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为Cr3+,反应的离子方程式
转化为Cr3+,反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
 NaNO2+
NaNO2+ HI―→
HI―→ NO↑+
NO↑+ I2+
I2+ NaI+
NaI+ H2O
H2O
(1)配平上面方程式。_________
(2)上述反应的氧化剂是________ ;若有 1 mol 的还原剂被氧化,则反应中转移电子的数目是________ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,进行实验,下列选项合适的是________ (填字母)。
A.③⑤ B.①②④
C.①②⑤ D.①②③⑤
(4)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为_________________________ 。
 NaNO2+
NaNO2+ HI―→
HI―→ NO↑+
NO↑+ I2+
I2+ NaI+
NaI+ H2O
H2O(1)配平上面方程式。
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,进行实验,下列选项合适的是
A.③⑤ B.①②④
C.①②⑤ D.①②③⑤
(4)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化合价和物质类别是梳理元素及其化合物知识的两个线索,可表示为“价类”二维图。下图是硫元素的“价类”二维图。
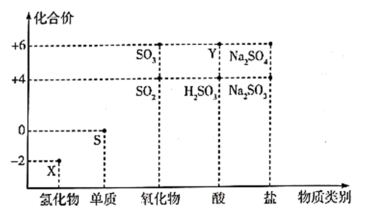
(1)X是___ (填化学式)。
(2)可选取Y的浓溶液和 反应来制备
反应来制备 ,该反应原理是
,该反应原理是___ (填化学方程式);将 排入大气中会引起
排入大气中会引起____ 。
(3) 是一种食品添加剂,其应与图中
是一种食品添加剂,其应与图中___ (填化学式)在同一位置,其具有____ (填“氧化性”或“还原性”)导致 中不可避免地存在
中不可避免地存在 。实验室中检验
。实验室中检验 的常用方法是
的常用方法是____ 。
(4)硫元素还有一种常见的价态-1价,如硫铁矿(主要成分为 )中的硫元素。
)中的硫元素。 可以与
可以与 溶液发生反应:
溶液发生反应: 。
。
①该反应中的氧化剂是____ (填化学式)。
②向反应后的溶液中通入空气就能使 溶液再生,写出再生反应的离子方程式:
溶液再生,写出再生反应的离子方程式:____ 。

(1)X是
(2)可选取Y的浓溶液和
 反应来制备
反应来制备 ,该反应原理是
,该反应原理是 排入大气中会引起
排入大气中会引起(3)
 是一种食品添加剂,其应与图中
是一种食品添加剂,其应与图中 中不可避免地存在
中不可避免地存在 。实验室中检验
。实验室中检验 的常用方法是
的常用方法是(4)硫元素还有一种常见的价态-1价,如硫铁矿(主要成分为
 )中的硫元素。
)中的硫元素。 可以与
可以与 溶液发生反应:
溶液发生反应: 。
。①该反应中的氧化剂是
②向反应后的溶液中通入空气就能使
 溶液再生,写出再生反应的离子方程式:
溶液再生,写出再生反应的离子方程式:
您最近半年使用:0次
【推荐3】NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是__ ,还原性I-__ NO(填“>”或“<”)。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有__ (填序号)。
(3)请配平以下化学方程式:__ Al+__ NaNO3+__ NaOH=__ NaAlO2+__ N2↑+_ H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为__ L。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:
若反应过程中转移5mol电子,则生成标准状况下N2的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】有A、B、C三种烃,它们的结构简式如下图所示:

A的名称是__________________________________________ ;
B的名称是__________________________________________ ;
C的名称是__________________________________________ 。

A的名称是
B的名称是
C的名称是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)大豆黄酮主要存在于大豆及其他豆科植物中。大豆黄酮是一种天然的有效活性成分,具有雌激素和抗雌激素作用、抗氧化作用、提高机体免疫力及影响内分泌系统等多种生物学功能。
①大豆黄酮的结构简式如图所示,它的分子式是_______ ,分子中含有_______ 个苯环,是_______ (填“芳香烃”或“芳香烃的衍生物”)。

②一种化合物根据所含的官能团不同可以将其划归为不同的类别,下列对大豆黄酮的归类正确的是_______ (填编号)。
A.醇类 B.酚类 C.酮类 D.醚类 E.酯类 F.烯烃
(2)某烷烃的相对分子质量为128,其分子式为_______ 。若该烷烃不能由任何一种烯烃与H2加成反应而得到,则该烷烃的结构简式为_______
(1)大豆黄酮主要存在于大豆及其他豆科植物中。大豆黄酮是一种天然的有效活性成分,具有雌激素和抗雌激素作用、抗氧化作用、提高机体免疫力及影响内分泌系统等多种生物学功能。
①大豆黄酮的结构简式如图所示,它的分子式是

②一种化合物根据所含的官能团不同可以将其划归为不同的类别,下列对大豆黄酮的归类正确的是
A.醇类 B.酚类 C.酮类 D.醚类 E.酯类 F.烯烃
(2)某烷烃的相对分子质量为128,其分子式为
您最近半年使用:0次

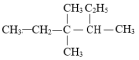 的系统命名为
的系统命名为 N2(g)+O2(g)
N2(g)+O2(g) O2(g)
O2(g)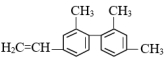 分子中处于同一直线上的碳原子最多有
分子中处于同一直线上的碳原子最多有

