下列装置能达到实验目的的是


| A.图1:氧化碘离子 |
| B.图2:在设定条件下测定镁铝合金中铝的质量分数 |
| C.图3:发生铝热反应 |
D.图4:比较 、 、 、S的氧化性 、S的氧化性 |
更新时间:2021/04/29 20:21:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列气体去除少量杂质的方法中,不能实现目的的是
| 气体(杂质) | 方法 | |
| A | 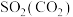 | 通过饱和亚硫酸氢钠溶液 |
| B | 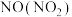 | 通过氢氧化钠溶液 |
| C | 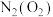 | 通过灼热的铜丝网 |
| D | 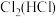 | 通过饱和的食盐水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
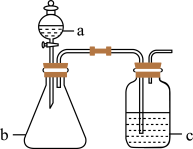
【推荐2】用如图所示装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是

| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有某种含有少量FeCl2杂质的FeCl3样品,现要测定其中铁元素的质量分数,实验采用下列步骤进行:①准确称量m g样品(在2~3g范围内);②向样品中加入10 mL 6mol·L-1的盐酸。再加入蒸馏水,配制成250 mL溶液;③量取25 mL操作②中所配的溶液,加入3 mL氯水,加热使其反应完全;④趁热迅速加入10%的氨水至过量,充分搅拌,使沉淀完全;⑤过滤,将沉淀洗涤后,灼烧、冷却、称重,并重复操作至恒重。若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,则样品中铁元素的质量分数为
A.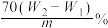 | B.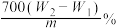 |
C.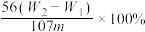 | D.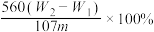 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向Na+、Br-、I-的混合溶液中通入适量氯气,反应完全后将溶液蒸干并小心灼烧至恒重,得固体的成分不可能为
| A.NaCl、NaBr、NaI | B.NaCl、NaBr |
| C.NaCl | D.NaCl、NaI |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验,能正确描述其反应的离子方程式是
A.Na2SO3溶液与少量C12反应:3SO +Cl2+H2O═2HSO +Cl2+H2O═2HSO +2Cl-+ +2Cl-+ |
| B.H2O2溶液中与少量FeCl3反应:2Fe3++ H2O2=O2+2H+ +2Fe2+ |
C.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:Ba2++ =BaSO4↓ =BaSO4↓ |
D.Ba(OH)2溶液与少量NaHCO3溶液反应:2 +Ba2++2OH-=BaCO3↓+ +Ba2++2OH-=BaCO3↓+ +H2O +H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.2.4g镁在足量O2中燃烧,转移的电子数为0.1NA |
| B.1L 0.1mol/L FeCl3溶液中加入过量铁粉,反应中转移的电子数为0.1NA |
| C.23g Na与足量H2O反应完全后可生成NA个H2分子 |
| D.标准状况下,8.1g Al与足量NaOH溶液反应生成气体22.4L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子检验或除杂方法错误的是
| A.除去Fe粉中混有的少量铝粉:加入过量NaOH溶液,过滤 |
| B.除去Na2CO3溶液中混有的少量NaHCO3:加入适量NaOH溶液 |
C.向某溶液中加入过量稀盐酸无明显现象,再加入BaCl2溶液,有白色沉淀生成,该溶液中一定含有SO |
| D.向某溶液中加入AgNO3溶液,有白色沉淀生成,该溶液中一定含有Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列解释有关事实的方程式不正确的是
A.铝热法炼铁:Fe2O3+ 2Al Al2O3+ 2Fe Al2O3+ 2Fe |
B.工业上用NH3制备NO:4NH3+ 5O2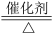 4NO十6H2O 4NO十6H2O |
C.向受酸雨影响的湖泊中喷洒CaCO3粉末:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
D.淀粉酿酒:(C6H10O5)n+nH2O  n C6H12O6,C6H12O6 n C6H12O6,C6H12O6 2C2H5OH+2CO2 2C2H5OH+2CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】铝热反应的实验装置如图。下列有关铝热反应的说法中,不正确的是


| A.铝热反应是放热反应 |
| B.铝热反应可用于冶炼某些高熔点金属 |
| C.实验中镁条的主要作用是还原氧化铁 |
| D.实验现象为产生耀眼白光,漏斗下方有红热熔融物流出 |
您最近一年使用:0次


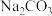
 溶液
溶液
 中的
中的
 溶液
溶液 ):加入足量NaOH溶液,过滤
):加入足量NaOH溶液,过滤 溶液(
溶液( );加入过量铁粉,过滤
);加入过量铁粉,过滤 溶液(
溶液( ):加入适量烧碱溶液
):加入适量烧碱溶液 气体(HCl):依次通过饱和
气体(HCl):依次通过饱和

