现有下列八种物质:①铝;②蔗糖;③SiO2;④H2SO4;⑤NaOH;⑥FeSO4溶液;⑦Ba(OH)2;⑧氢氧化铁胶体
(1)上述物质属于电解质的有____ (填序号)。
(2)向⑤的水溶液中加入①的粉末,反应的离子方程式为____ 。
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为____ 。
(4)实验室制备⑧的离子方程式为___ ;若在⑧中缓慢加入④的溶液,产生的现象是___ 。
(5)③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为___ ;工艺师常用___ (填物质名称)来雕刻玻璃。
(1)上述物质属于电解质的有
(2)向⑤的水溶液中加入①的粉末,反应的离子方程式为
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(4)实验室制备⑧的离子方程式为
(5)③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为
更新时间:2021-05-01 13:02:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩冰水混合物
(1)以上物质中属于混合物的是________ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出制备物质⑤的化学方程式________ ,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。鉴别胶体成功制备最简单的方法是_________ 。
(3)在含40g溶质的①溶液中缓缓通入标准状况下66gCO2,则反应后溶液的溶质有______ (填化学式),该过程的离子反应方程式为___________ 。
(1)以上物质中属于混合物的是
(2)写出制备物质⑤的化学方程式
(3)在含40g溶质的①溶液中缓缓通入标准状况下66gCO2,则反应后溶液的溶质有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)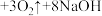 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠(Na2FeO4)属于___________ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为___________ 价;与O2互为同素异形体的物质的化学式为___________ 。
(2)将上述反应的化学方程式改写成离子方程式:___________ ,该反应中的O2为___________ (填标号)。
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
(3)实验室制备 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴___________ (填化学式)饱和溶液,继续煮沸至液体呈___________ 色,停止加热。
(4)当生成48g O2时,至少有___________ g水参与反应,生成的NaOH的质量为___________ g。
 (胶体)
(胶体)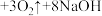 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:(1)高铁酸钠(Na2FeO4)属于
(2)将上述反应的化学方程式改写成离子方程式:
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
(3)实验室制备
 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴(4)当生成48g O2时,至少有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】人类学会了烧制陶瓷,冶炼金属,创造了光辉灿烂的古代文明,我国是世界上发明陶瓷、火药、冶金等较早的国家。赤铁矿是炼铁的主要原料,主要成分为 ,
, 又称铁红,请根据要求完成下列问题。
又称铁红,请根据要求完成下列问题。
(1) 固体(红棕色)属于
固体(红棕色)属于___________ (填“纯净物”或“混合物”)。炼铁的主要原理: ,该反应中被氧化和被还原的原子个数比为
,该反应中被氧化和被还原的原子个数比为___________ ,将 加入到适量的盐酸中,反应的化学方程式:
加入到适量的盐酸中,反应的化学方程式:___________ 。
(2)用上述所得溶液进行下列实验:取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式:___________ 。
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴 饱和溶液,继续煮沸至溶液呈
饱和溶液,继续煮沸至溶液呈___________ 色,即可制得 胶体,化学方程式为
胶体,化学方程式为___________ 。
 ,
, 又称铁红,请根据要求完成下列问题。
又称铁红,请根据要求完成下列问题。(1)
 固体(红棕色)属于
固体(红棕色)属于 ,该反应中被氧化和被还原的原子个数比为
,该反应中被氧化和被还原的原子个数比为 加入到适量的盐酸中,反应的化学方程式:
加入到适量的盐酸中,反应的化学方程式:(2)用上述所得溶液进行下列实验:取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式:
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴
 饱和溶液,继续煮沸至溶液呈
饱和溶液,继续煮沸至溶液呈 胶体,化学方程式为
胶体,化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)现有以下物质①熔融状态的NaCl ②NH3·H2O ③Na2O固体 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦液态HCl ⑧KNO3溶液,其中属于电解质的是:___________ ;该状态下能导电的是_____________ ;属于非电解质的是_________________ 。(请用序号作答)
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内____ ;该反应的还原剂是_________________ ;
②H2O2既体现氧化性,又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是__________ 。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:___________ 。
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内
②H2O2既体现氧化性,又体现还原性的反应是
③请用双线桥法表示B反应中电子转移的方向和数目:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请将下列物质前的编号按要求填入相应的空格中。
①空气 ②氧气 ③食盐水 ④H2SO4 ⑤铜 ⑥氢氧化钾 ⑦酒精 ⑧水 ⑨蔗糖 ⑩碳酸氢钠
(1)混合物:______ ;
(2)单质:______ ;
(3)酸:______ ;
(4)碱:______ ;
(5)盐:_______ ;
(6)氧化物:______ ;
(7)电解质:______ ;
(8)非电解质:______ 。
①空气 ②氧气 ③食盐水 ④H2SO4 ⑤铜 ⑥氢氧化钾 ⑦酒精 ⑧水 ⑨蔗糖 ⑩碳酸氢钠
(1)混合物:
(2)单质:
(3)酸:
(4)碱:
(5)盐:
(6)氧化物:
(7)电解质:
(8)非电解质:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】分类思想在化学中有重要的应用,通常会对物质及反应进行分类研究。
(1)①空气②氧气③食盐水④氢氧化钾⑤铜⑥碳酸氢钠⑦蔗糖⑧酒精。以上物质中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:___________ 。
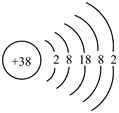
(3)锶( )原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:___________ 。
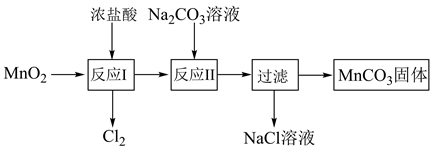
(4)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。
①写出“反应Ⅱ”的离子方程式:___________ 。
②过滤操作需要的玻璃仪器有烧杯、___________ 、___________ 。
③过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为___________ 。
(1)①空气②氧气③食盐水④氢氧化钾⑤铜⑥碳酸氢钠⑦蔗糖⑧酒精。以上物质中,属于电解质的是
(2)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
(3)锶(
 )原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
(4)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅱ”的离子方程式:
②过滤操作需要的玻璃仪器有烧杯、
③过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料是___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)Na2SiO3溶液俗称___________ 。工业上常用2C+SiO2 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___________ (填化学式),氧化剂是___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)Na2SiO3溶液俗称
 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属及非金属在高中化学中占有重要地位。
(1)为了验证某溶液中含有 而不含有
而不含有 ,正确的方法是
,正确的方法是 ______ (填字母)。
A.直接滴加 溶液
溶液
B.先通入足量氯气,再滴入 溶液
溶液
C.先滴入 溶液,再通入氯气
溶液,再通入氯气
D.先加入足量铁粉,充分振荡后再滴加 溶液
溶液
(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是______ (用化学方程式表示)。
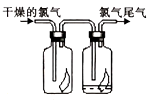
(3)如图所示,将氯气依次通过盛有干燥有色布条、潮湿有色布条的广口瓶可观察到的现象是_____ ,说明起漂白性的物质是 _____ (填化学式)。
(4)无水 易升华,可用作有机合成的催化剂等。工业上由铝土矿(
易升华,可用作有机合成的催化剂等。工业上由铝土矿( 、
、 )为原料制备无水
)为原料制备无水 的工艺流程如图。
的工艺流程如图。
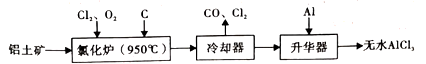
①氯化炉中, 、
、 和C反应中的氧化产物是
和C反应中的氧化产物是 ______ (填化学式)。
②用 溶液可除去冷却器排出尾气中的
溶液可除去冷却器排出尾气中的 ,此反应的离子方程式为
,此反应的离子方程式为_________ 。
③流程中需要向升华器内加入少量Al,其作用是________ 。
(1)为了验证某溶液中含有
 而不含有
而不含有 ,正确的方法是
,正确的方法是 A.直接滴加
 溶液
溶液B.先通入足量氯气,再滴入
 溶液
溶液C.先滴入
 溶液,再通入氯气
溶液,再通入氯气D.先加入足量铁粉,充分振荡后再滴加
 溶液
溶液(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是
(3)如图所示,将氯气依次通过盛有干燥有色布条、潮湿有色布条的广口瓶可观察到的现象是

(4)无水
 易升华,可用作有机合成的催化剂等。工业上由铝土矿(
易升华,可用作有机合成的催化剂等。工业上由铝土矿( 、
、 )为原料制备无水
)为原料制备无水 的工艺流程如图。
的工艺流程如图。
①氯化炉中,
 、
、 和C反应中的氧化产物是
和C反应中的氧化产物是 ②用
 溶液可除去冷却器排出尾气中的
溶液可除去冷却器排出尾气中的 ,此反应的离子方程式为
,此反应的离子方程式为③流程中需要向升华器内加入少量Al,其作用是
您最近半年使用:0次

 制备硅单质,该反应能否说明
制备硅单质,该反应能否说明 的氧化性强于
的氧化性强于 ?
? 的混合固体,欲从中分离出
的混合固体,欲从中分离出

