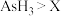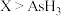(1)现有以下物质①熔融状态的NaCl ②NH3·H2O ③Na2O固体 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦液态HCl ⑧KNO3溶液,其中属于电解质的是:___________ ;该状态下能导电的是_____________ ;属于非电解质的是_________________ 。(请用序号作答)
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内____ ;该反应的还原剂是_________________ ;
②H2O2既体现氧化性,又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是__________ 。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:___________ 。
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内
②H2O2既体现氧化性,又体现还原性的反应是
③请用双线桥法表示B反应中电子转移的方向和数目:
更新时间:2018-03-09 23:22:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学使我们的生活丰富多彩,在过去的100多年中,科学家合成和分离了近2300万种物质,满足了人类生存和社会进步的物质需求。现有下列物质:
①NaOH溶液 ②浓硫酸 ③氨水 ④冰醋酸 ⑤ ⑥冰 ⑦蔗糖 ⑧石墨
⑥冰 ⑦蔗糖 ⑧石墨
回答下列问题:
(1)以上物质中属于弱电解质的有________ (填序号,下同),属于非电解质的有________ 。
(2)室温下,用 ①滴定
①滴定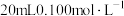 ④的溶液,溶液pH随①体积的变化如图所示。
④的溶液,溶液pH随①体积的变化如图所示。

①根据上图计算醋酸的电离常数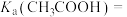
________ 。
②a、b、c三点溶液中,水的电离程度由大到小的顺序为________ 。
③c点溶液中离子浓度由大到小的顺序为________ 。
(3)某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断下列说法错误的是________ 。

a.a值一定大于9
b.Ⅱ为氨水稀释时溶液的pH变化曲线
c.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
d.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积 (氨水)
(氨水)
①NaOH溶液 ②浓硫酸 ③氨水 ④冰醋酸 ⑤
 ⑥冰 ⑦蔗糖 ⑧石墨
⑥冰 ⑦蔗糖 ⑧石墨回答下列问题:
(1)以上物质中属于弱电解质的有
(2)室温下,用
 ①滴定
①滴定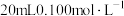 ④的溶液,溶液pH随①体积的变化如图所示。
④的溶液,溶液pH随①体积的变化如图所示。
①根据上图计算醋酸的电离常数
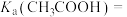
②a、b、c三点溶液中,水的电离程度由大到小的顺序为
③c点溶液中离子浓度由大到小的顺序为
(3)某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断下列说法错误的是

a.a值一定大于9
b.Ⅱ为氨水稀释时溶液的pH变化曲线
c.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
d.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积
 (氨水)
(氨水)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下7种生活中常见的物质:① ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:
(1)以上物质中属于电解质的是_______ (填序号,下同);属于碱的是_______ ;属于盐的是_______ 。
(2)①在水中电离的方程为_______ 。
(3)②与稀盐酸反应的离子方程式为_______ 。
(4)写出④转化成①的化学方程式_______ 。
(5)现设计实验由大理石( )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液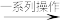 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:_______ 。
 ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:(1)以上物质中属于电解质的是
(2)①在水中电离的方程为
(3)②与稀盐酸反应的离子方程式为
(4)写出④转化成①的化学方程式
(5)现设计实验由大理石(
 )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液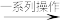 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)按要求写出方程式:
①HNO3(电离方程式)___________
②硫酸钠和氯化钡溶液反应(离子方程式)___________
③钠与水反应(离子方程式)___________
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥蔗糖⑦澄清石灰水,其中属于电解质的有___________ ,属于非电解质的有___________ (填编号)。
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是___________ (用化学式表示,后同),___________ 元素被氧化,还原产物为___________
②用单线桥在方程式中标出电子转移的情况:___________ 。
2Fe(OH)3+4NaOH+3NaC1O=2Na2FeO4+3NaCl+5H2O
(1)按要求写出方程式:
①HNO3(电离方程式)
②硫酸钠和氯化钡溶液反应(离子方程式)
③钠与水反应(离子方程式)
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥蔗糖⑦澄清石灰水,其中属于电解质的有
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是
②用单线桥在方程式中标出电子转移的情况:
2Fe(OH)3+4NaOH+3NaC1O=2Na2FeO4+3NaCl+5H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列化学反应,按要求回答问题:
A.(NH4)2SO3 2NH3↑+H2O+SO2↑ B.2CO+O2
2NH3↑+H2O+SO2↑ B.2CO+O2 2CO2
2CO2
C.2C+SiO2 Si+2CO↑ D.NH4NO3
Si+2CO↑ D.NH4NO3 N2O+ 2H2O
N2O+ 2H2O
E.CaCO3 + CO2+ H2O=Ca(HCO3)2 F.MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(1)以上反应中,属于氧化还原反应的是________________ (填上述反应的编号);
(2)在反应MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O中:
MnCl2 + Cl2↑+ 2H2O中:
①氧化剂是___________ ,氧化产物是________ 。
②在该反应方程式中用双线桥法表示出电子转移的方向和数目_______________ 。
③若产生了标准状况下3.36L的氯气,则被氧化的HCl的物质的量为________ 摩尔。
A.(NH4)2SO3
 2NH3↑+H2O+SO2↑ B.2CO+O2
2NH3↑+H2O+SO2↑ B.2CO+O2 2CO2
2CO2C.2C+SiO2
 Si+2CO↑ D.NH4NO3
Si+2CO↑ D.NH4NO3 N2O+ 2H2O
N2O+ 2H2OE.CaCO3 + CO2+ H2O=Ca(HCO3)2 F.MnO2 + 4HCl(浓)
 MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O(1)以上反应中,属于氧化还原反应的是
(2)在反应MnO2 + 4HCl(浓)
 MnCl2 + Cl2↑+ 2H2O中:
MnCl2 + Cl2↑+ 2H2O中:①氧化剂是
②在该反应方程式中用双线桥法表示出电子转移的方向和数目
③若产生了标准状况下3.36L的氯气,则被氧化的HCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体 ②水 ③蔗糖溶液 ④Ca(OH)2悬浊液
(4)用单线桥 标出下列反应中电子转移的情况:_______ 。
8NH3+6NO2 7N2+12H2O
7N2+12H2O
(5)请写出最恰当的试剂除去括号中的杂质:Cl2(HCl)_______ 。
(6)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的原因是为了防止Fe(OH)2被氧化,写出其被氧化的化学反应方程式_______ 。
(1)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)当光束通过下列物质时,会出现丁达尔效应的是
①Fe(OH)3胶体 ②水 ③蔗糖溶液 ④Ca(OH)2悬浊液
(4)用
8NH3+6NO2
 7N2+12H2O
7N2+12H2O(5)请写出最恰当的试剂除去括号中的杂质:Cl2(HCl)
(6)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的原因是为了防止Fe(OH)2被氧化,写出其被氧化的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列反应是在溶液中进行的反应,按下列要求作答:MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用双线桥表示反应中电子的转移情况___ ;MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(2)该反应的氧化剂是___ ,发生了___ 反应。
(3)将其改写成离子方程式___ 。
(4)当有2molHCl消耗时,转移的电子的物质的量为___ mol。
(5)浓盐酸在该反应中表现的性质是___ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑(1)用双线桥表示反应中电子的转移情况
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑(2)该反应的氧化剂是
(3)将其改写成离子方程式
(4)当有2molHCl消耗时,转移的电子的物质的量为
(5)浓盐酸在该反应中表现的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】烟道气中含有 ,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。

(1)写出 的电子式
的电子式___________ ;
(2)下列叙述正确的是___________ ;
A.烟道气中的 含量可用一定体积、浓度的酸性高锰酸钾溶液测定
含量可用一定体积、浓度的酸性高锰酸钾溶液测定
B. 是橡胶硫化剂,橡胶硫化程度越高,弹性越好
是橡胶硫化剂,橡胶硫化程度越高,弹性越好
C. 可与
可与 发生反应,能作为
发生反应,能作为 的脱水剂
的脱水剂
D. 固体中含阳离子
固体中含阳离子 和阴离子
和阴离子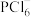 ,
, 空间构型为正四面体
空间构型为正四面体
E. 易溶于
易溶于 ,则
,则 为非极性分子
为非极性分子
(3) 与过量
与过量 反应的化学方程式
反应的化学方程式___________ ;
(4) 与
与 反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为
反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为___________ ;
(5)设计实验检验 与足量NaOH溶液反应生成的阴离子
与足量NaOH溶液反应生成的阴离子___________ 。
 ,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
(1)写出
 的电子式
的电子式(2)下列叙述正确的是
A.烟道气中的
 含量可用一定体积、浓度的酸性高锰酸钾溶液测定
含量可用一定体积、浓度的酸性高锰酸钾溶液测定B.
 是橡胶硫化剂,橡胶硫化程度越高,弹性越好
是橡胶硫化剂,橡胶硫化程度越高,弹性越好C.
 可与
可与 发生反应,能作为
发生反应,能作为 的脱水剂
的脱水剂D.
 固体中含阳离子
固体中含阳离子 和阴离子
和阴离子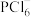 ,
, 空间构型为正四面体
空间构型为正四面体E.
 易溶于
易溶于 ,则
,则 为非极性分子
为非极性分子(3)
 与过量
与过量 反应的化学方程式
反应的化学方程式(4)
 与
与 反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为
反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为(5)设计实验检验
 与足量NaOH溶液反应生成的阴离子
与足量NaOH溶液反应生成的阴离子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
(1)实验室制备氯气的离子方程式是_____ ;若多余的氯气用氢氧化钠溶液吸收,其离子方程式为_____ 。
II.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有NaCl与Cl2生成。
(2)写出并配平该反应的化学方程式_____ 。
(3)如果反应中生成标准状况下11.2L氯气,则转移电子数为_____ 。
(4)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为-1价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式_____ 。
(1)实验室制备氯气的离子方程式是
II.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有NaCl与Cl2生成。
(2)写出并配平该反应的化学方程式
(3)如果反应中生成标准状况下11.2L氯气,则转移电子数为
(4)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为-1价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式
您最近一年使用:0次

 、
、 、
、 、
、 、
、 、
、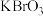 在反应中得到电子,则该反应的还原剂是
在反应中得到电子,则该反应的还原剂是 在反应中得到10个电子生成X,则X的化学式为
在反应中得到10个电子生成X,则X的化学式为