硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)埋在地下的光导纤维如果裸露在碱性土壤中,会导致断路,用离子方程式说明原因___________ ;工艺师常用___________ (填物质名称)来雕刻玻璃。
(2)工业上常利用反应 制备硅单质,该反应能否说明
制备硅单质,该反应能否说明 的氧化性强于
的氧化性强于 ?
?___________ (说明理由)。
(3)有一 、
、 的混合固体,欲从中分离出
的混合固体,欲从中分离出 ,应如何操作?
,应如何操作?___________
(1)埋在地下的光导纤维如果裸露在碱性土壤中,会导致断路,用离子方程式说明原因
(2)工业上常利用反应
 制备硅单质,该反应能否说明
制备硅单质,该反应能否说明 的氧化性强于
的氧化性强于 ?
?(3)有一
 、
、 的混合固体,欲从中分离出
的混合固体,欲从中分离出 ,应如何操作?
,应如何操作?
更新时间:2021-09-20 06:47:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列反应的化学方程式。
(1)电解饱和食盐水:____________ 。
(2)氢氧化钠溶液腐蚀磨砂玻璃塞:____________ 。
(3)实验室用亚硫酸钠与浓硫酸反应制备二氧化硫:____________ 。
(4)氢氧化铝溶于氢氧化钠溶液:____________ 。
(5)氨在催化剂的作用下与氧气发生反应,生成一氧化氮____________ 。
(1)电解饱和食盐水:
(2)氢氧化钠溶液腐蚀磨砂玻璃塞:
(3)实验室用亚硫酸钠与浓硫酸反应制备二氧化硫:
(4)氢氧化铝溶于氢氧化钠溶液:
(5)氨在催化剂的作用下与氧气发生反应,生成一氧化氮
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氢氟酸是HF的水溶液,可与 发生反应生成
发生反应生成 和
和 。请写出该反应的化学方程式
。请写出该反应的化学方程式______ 。想一想为什么可以用氢氟酸溶蚀玻璃生产磨砂玻璃_________ 。
 发生反应生成
发生反应生成 和
和 。请写出该反应的化学方程式
。请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。请写下列空白:
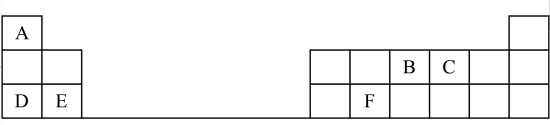
(1)A与B形成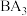 的化学式为
的化学式为___________ ;C的原子结构示意图为___________ 。
(2)B的最高价氧化物对应的水化物的化学式为___________ ;D、E的最高价氧化物对应的水化物中碱性较弱的是___________ (用化学式表示),元素C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)。
(3)E位于周期表的第三周期第___________ 族;F的氧化物与氢氧化钠溶液反应的离子方程式为___________ 。

(1)A与B形成
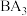 的化学式为
的化学式为(2)B的最高价氧化物对应的水化物的化学式为
(3)E位于周期表的第三周期第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硅是带来人类文明的重要元素之一,工业上可用石英砂制备硅单质。
(1)硅和锗(Ge)属于同主族元素。下列推测不合理的是___________ (填字母)。
a.Ge与Si的最外层电子数均为4 b.常温下 是气体
是气体
c.酸性: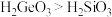 d.Si和Ge都可做半导体材料
d.Si和Ge都可做半导体材料
(2)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是___________ 。
②在以上流程中,能否将盐酸改为NaOH溶液,请说明理由:___________ 。
(3)氮化硅( )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为 。
。
①该反应中的氧化剂为___________ (填化学式)。
②若生成标准状况下16.8L CO,则生成氮化硅的质量是___________ (保留1位小数)。
(4)我国成功发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石(主要成分为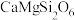 )、斜长石(主要成分为
)、斜长石(主要成分为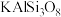 )和橄榄石(主要成分为
)和橄榄石(主要成分为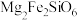 )等,橄榄石的主要成分中铁元素为
)等,橄榄石的主要成分中铁元素为___________ 价,橄榄石的主要成分的氧化物形式可表示为___________ 。辉石、斜长石及橄榄石的主要成分均属于___________ (填“氧化物”“混合物”或“硅酸盐”)。
(1)硅和锗(Ge)属于同主族元素。下列推测不合理的是
a.Ge与Si的最外层电子数均为4 b.常温下
 是气体
是气体c.酸性:
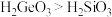 d.Si和Ge都可做半导体材料
d.Si和Ge都可做半导体材料(2)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是
②在以上流程中,能否将盐酸改为NaOH溶液,请说明理由:
(3)氮化硅(
 )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为 。
。①该反应中的氧化剂为
②若生成标准状况下16.8L CO,则生成氮化硅的质量是
(4)我国成功发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石(主要成分为
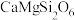 )、斜长石(主要成分为
)、斜长石(主要成分为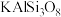 )和橄榄石(主要成分为
)和橄榄石(主要成分为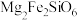 )等,橄榄石的主要成分中铁元素为
)等,橄榄石的主要成分中铁元素为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列各题。
(1)硅元素在自然界以___________ (选填“游离态”或“化合态”)形式存在,硅的氧化物属于___________ (选填“酸性”“两性”或“碱性”)氧化物。
(2) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是___________ (用化学方程式表示)。
(3)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。 可通过
可通过 与纯碱混合后高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
与纯碱混合后高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)制备硅半导体材料必须先得到高纯硅,三氯硅烷( )还原法是当前制备高纯硅的主要方法,生产过程示意图如下图所示:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如下图所示:

①写出由纯 制备高纯硅反应的化学方程式:
制备高纯硅反应的化学方程式:___________ 。
②整个制备过程必须严格控制无水无氧,因为 遇水剧烈反应生成
遇水剧烈反应生成 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:___________ 。
(1)硅元素在自然界以
(2)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(3)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作 可通过
可通过 与纯碱混合后高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
与纯碱混合后高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)制备硅半导体材料必须先得到高纯硅,三氯硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程示意图如下图所示:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如下图所示:
①写出由纯
 制备高纯硅反应的化学方程式:
制备高纯硅反应的化学方程式:②整个制备过程必须严格控制无水无氧,因为
 遇水剧烈反应生成
遇水剧烈反应生成 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ ,Na在氧气中完全燃烧所得产物的电子式为_______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________ (填“高”或“低”)
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为______ ;SiO2的晶体类型为________ 。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为______ (写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵___ kg。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池板的是_________ (填化学式)。
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为_________ 。
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(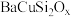 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
(4)工业上提纯硅有多种路线,其中一种工艺流程如图:

①电弧炉中发生反应的化学方程式为_________ 。
②在流化床反应的产物中, 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和_________ 。
③整个制作过程必须严格控制无水、无氧, 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为_________ 。
(1)可用于制作计算机芯片和太阳能电池板的是
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(
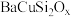 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。A.可用氧化物形式表示为 | B.性质稳定,不易脱色 |
| C.x等于6 | D.易溶解于强酸和强碱 |

①电弧炉中发生反应的化学方程式为
②在流化床反应的产物中,
 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和| 物质 |  |  |  | 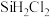 | 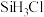 |  |  |
沸点/ | 2355 | 57.6 | 31.8 | 8.2 |  |  |  |
③整个制作过程必须严格控制无水、无氧,
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢氧化镁是已知用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面。镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4,含氧化铝、氧化铁、氧化亚铁等杂质]可用于生产氢氧化镁,简要工艺流程如下:
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
(1)对矿石焙烧的目的是_______________________ 。
(2)加入H2O2溶液反应的离子方程式是___________________ 。
(3)向溶液Ⅰ中加入的X可以是______________ ,作用是______________ 。
(4)加入氨水时,Mg2+转化率随温度t的变化如图所示:
①溶液Ⅱ中发生反应的离子方程式是__________________ 。
②t1前Mg2+转化率增大的原因是__________________ ;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________ 。

已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是
(2)加入H2O2溶液反应的离子方程式是
(3)向溶液Ⅰ中加入的X可以是
(4)加入氨水时,Mg2+转化率随温度t的变化如图所示:

①溶液Ⅱ中发生反应的离子方程式是
②t1前Mg2+转化率增大的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲苯和溴乙烷混合物可通过如图流程进行分离。
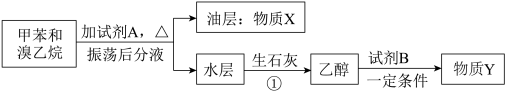
请填写下列空白:
(1)试剂A的名称为___ ,X的结构简式为___ 。
(2)操作①是___ 。
(3)写出甲苯和溴乙烷的混合物中加入试剂A时发生反应的方程式___ 。

请填写下列空白:
(1)试剂A的名称为
(2)操作①是
(3)写出甲苯和溴乙烷的混合物中加入试剂A时发生反应的方程式
您最近一年使用:0次

 固体;④铜;⑤熔融KCl
固体;④铜;⑤熔融KCl

