工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
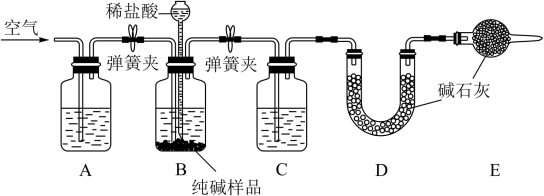
(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若___ ,说明装置不漏气。
(2)实验结束后通入空气的目的为___ 。
(3)装置A的试剂为___ ,装置C中的试剂为___ 。
(4)装置E作用为___ 。
(5)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为__ 。
(6)有同学认为该实验设计有较大缺陷,你认为要如何改进__ 。

(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(2)实验结束后通入空气的目的为
(3)装置A的试剂为
(4)装置E作用为
(5)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为
(6)有同学认为该实验设计有较大缺陷,你认为要如何改进
18-19高一上·河北石家庄·期末 查看更多[4]
湖北省公安县第三中学2023-2024学年高一上学期11月考试化学试题宁夏银川唐徕回民中学2021-2022学年高一上学期期末考试化学试题(已下线)周末培优2 有关钠和氯的实验题-2021-2022学年高一化学课后培优练(人教版2019必修第一册)河北省石家庄外国语学校2018-2019学年高一上学期期末化学试题
更新时间:2021-05-01 13:02:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在化学课上老师向NaOH溶液通入CO2后无明显现象。
(提出问题)如何通过实验证明CO2与NaOH发生了反应?
[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(Na2CO3+HCl=NaCl+NaHCO3)
②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之--CO2消失的角度,某同学设计了如图所示的实验,打开活塞,向充满CO2的瓶中滴入NaOH溶液,一会儿后观察到的现象是______________ 。据此现象判断NaOH与CO2发生了化学反应。

但上述实验不足证明反应.其理由是______________________ ,完善的方案是_______________ 。
(2)从生成物Na2CO3角度,经过讨论,分别设计了以下两个实验方案:
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH变化,如图所示。请用化学方程式回答下列问题:

(3) BC段pH降低的原因可能是_____________________ ;
(4)CD段pH低于7的原因可能是_____________________ 。
(提出问题)如何通过实验证明CO2与NaOH发生了反应?
[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(Na2CO3+HCl=NaCl+NaHCO3)
②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之--CO2消失的角度,某同学设计了如图所示的实验,打开活塞,向充满CO2的瓶中滴入NaOH溶液,一会儿后观察到的现象是

但上述实验不足证明反应.其理由是
(2)从生成物Na2CO3角度,经过讨论,分别设计了以下两个实验方案:
| 实验操作 | 实验现象 | 结论 |
| 方案一:向实验(1)所得的溶液中加入 | 有白色沉淀产生 | 有新物质Na2CO3生成,发生反应。 |
| 方案二:向实验(1)所得溶液中滴加过量稀盐酸 |

(3) BC段pH降低的原因可能是
(4)CD段pH低于7的原因可能是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、 、
、 的逐步分离。相应的实验过程可用下列流程图表示:
的逐步分离。相应的实验过程可用下列流程图表示:

(1)写出上述实验过程中所用试剂的化学式:
试剂1_______ 、试剂2_______ 、试剂3_______ 、试剂4_______
(2)溶液②中含有_______ 种阳离子。
(3)加入过量试剂3的目的是_______
(4)恰当地控制试剂4的加入量的方法是_______
(5)在加入试剂4后,获得固体D的实验操作④是_______ (填操作名称)
 、
、 的逐步分离。相应的实验过程可用下列流程图表示:
的逐步分离。相应的实验过程可用下列流程图表示:
(1)写出上述实验过程中所用试剂的化学式:
试剂1
(2)溶液②中含有
(3)加入过量试剂3的目的是
(4)恰当地控制试剂4的加入量的方法是
(5)在加入试剂4后,获得固体D的实验操作④是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】粤盐集团晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下:
等。粗盐提纯的工艺流程如下:
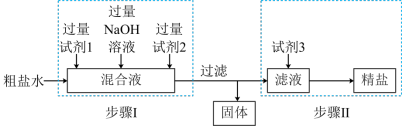
(1)“步骤I”中所加试剂的顺序依次为:试剂1为______________ 溶液,检验试剂1加入已足量的操作方法是:__________________ 。
(2)试剂2为_______________ 溶液;涉及的离子反应有: __________________ ;__________ 。
(3)所加试剂3 的目的是:_______________________ 。
(4)“步骤II”从滤液中获得精盐的实验操作中用到的主要硅酸盐仪器是(填两件):_________________________ 。
 、
、 、
、 等。粗盐提纯的工艺流程如下:
等。粗盐提纯的工艺流程如下:
(1)“步骤I”中所加试剂的顺序依次为:试剂1为
(2)试剂2为
(3)所加试剂3 的目的是:
(4)“步骤II”从滤液中获得精盐的实验操作中用到的主要硅酸盐仪器是(填两件):
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有一固体混合物A,已知其中可能含有MgCl2、CuSO4、CaCO3、FeCl3四种物质中的两种或多种。按如图所示进行实验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全进行)。
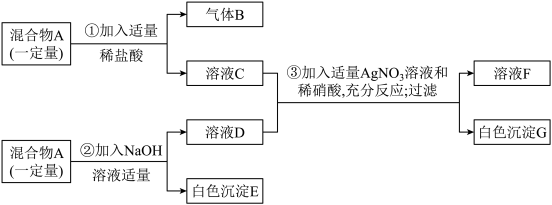
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的化学式为______ 。
(2)在混合物A里,上述四物质中肯定不存在的物质是_____ (写化学式)。
(3)在溶液F中,主要含有___ 种溶质,其中大量含有的酸根离子符号是____ 。
(4)写出1个生成白色沉淀G的化学方程式:_____ 。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的化学式为
(2)在混合物A里,上述四物质中肯定不存在的物质是
(3)在溶液F中,主要含有
(4)写出1个生成白色沉淀G的化学方程式:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室用废铁屑制备硫酸铁铵[NH4Fe(SO4)2·xH2O],具体流程如下:
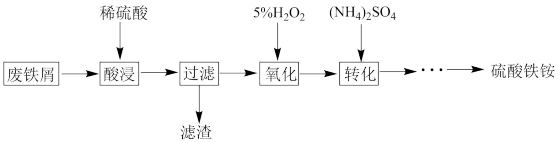
(1)废铁屑需用热的纯碱溶液洗涤,其目的是___________ 。
(2)“酸浸”是温度需保持为80~95℃,采用的合适加热方式是___________ 。实验室过滤操作必须用到的玻璃仪器有烧杯、 ___________ 。
(3)5%H2O2的作用是氧化Fe2+(“酸浸”过程稀硫酸过量),写出该反应的离子方程式是___________ 。
(4)“转化”后制取硫酸铁铵晶体的操作主要包括___________ 、过滤、洗涤、干燥。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为___________ 。

(1)废铁屑需用热的纯碱溶液洗涤,其目的是
(2)“酸浸”是温度需保持为80~95℃,采用的合适加热方式是
(3)5%H2O2的作用是氧化Fe2+(“酸浸”过程稀硫酸过量),写出该反应的离子方程式是
(4)“转化”后制取硫酸铁铵晶体的操作主要包括
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐3】某同学进行实验研究时,欲配制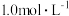 Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。
Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。
(1)烧杯中未溶物仅为BaCO3,理由是_______
(2)假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计实验方案,进行成分检验。在答题卡上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
(3)将试剂初步提纯后,准确测定其中Ba(OH)2·8H2O的含量。实验如下:
①配制250ml 约 Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,
Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,_______ ,将溶液转入_______ ,洗涤,定容,摇匀。
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将_______ (填“0.020”、“0.05”、“0.1980”或“1.5”) 盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
③ 计算Ba(OH)2·8H2O的质量分数=_______ (只列出算式,不做运算)
(4)室温下,_______ (填“能”或“不能”) 配制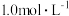 Ba(OH)2溶液。
Ba(OH)2溶液。
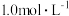 Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。
Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究原因,该同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。(1)烧杯中未溶物仅为BaCO3,理由是
(2)假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计实验方案,进行成分检验。在答题卡上写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀 | |
| 步骤2:取适量的滤液于试管中,滴加稀硫酸 | |
| 步骤3:取适量步骤1中的沉淀于试管中 | |
| 步骤4: |
①配制250ml 约
 Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,
Ba(OH)2·8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将
 盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
盐酸装入50ml酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。③ 计算Ba(OH)2·8H2O的质量分数=
(4)室温下,
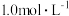 Ba(OH)2溶液。
Ba(OH)2溶液。
您最近半年使用:0次



