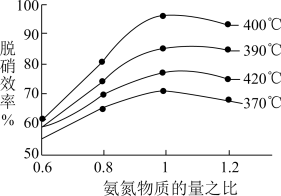
汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝: 4NO(g)+4NH3(g)+O2(g)  4N2(g)+6H2O(g) ΔH<0 根据下图判断提高脱硝效率的最佳条件是
4N2(g)+6H2O(g) ΔH<0 根据下图判断提高脱硝效率的最佳条件是___________ ;氨氮比一定时,在400 ℃时,脱硝效率最大,其可能的原因是___________ 。
 4N2(g)+6H2O(g) ΔH<0 根据下图判断提高脱硝效率的最佳条件是
4N2(g)+6H2O(g) ΔH<0 根据下图判断提高脱硝效率的最佳条件是
2021高三·全国·专题练习 查看更多[4]
上海戏剧学院附属高级中学2023-2024学年高二上学期(第2次)质量监测(等级)化学试卷 (已下线)05 常考题空5 平衡图像原因解释之选择反应最佳条件 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)第七章 化学反应速率与化学平衡 第45讲 实际工业生产中图像问题分类突破(已下线)小题31 化学平衡新情景图像——备战2021年高考化学经典小题考前必刷(全国通用)
更新时间:2021-05-05 19:09:47
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)在一定条件下,xA+yB zC的反应达到平衡。
zC的反应达到平衡。
①已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是________ ;
②已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向______ (填“正反应方向”或“逆反应方向”)移动;
③若加热后C的质量分数减少,则正反应是_______ (填“放热”或“吸热”)反应。
(2)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。硫酸生产中,SO2催化氧化生成SO3的原理为:2SO2(g)+O2(g)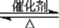 2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
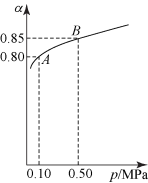
根据图示回答下列问题:平衡状态由A变到B时,平衡常数K(A)_______ K(B)(填“>”、“<”或“=”)。
 zC的反应达到平衡。
zC的反应达到平衡。①已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是
②已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向
③若加热后C的质量分数减少,则正反应是
(2)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。硫酸生产中,SO2催化氧化生成SO3的原理为:2SO2(g)+O2(g)
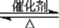 2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
2SO3(g)。某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。
根据图示回答下列问题:平衡状态由A变到B时,平衡常数K(A)
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)密闭容器中mA(g)+nB(g) pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
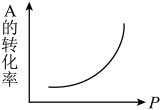
①增大压强,A的转化率___ 平衡向___ 移动,达到平衡后,混合物中C的浓度___ 。
②上述化学方程式中的系数m、n、p的正确关系是____ 。
③当降低温度时,C的浓度减小,正反应是___ 热反应。
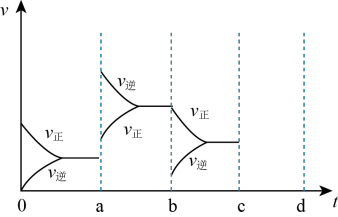
(2)如图表示在密闭容器中反应:2SO2(g)+O2(g) 2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是
2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___ ;b-c过程中改变的条件可能是____ ;若增大压强时,反应速度变化情况画在c-d处。___
 pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
①增大压强,A的转化率
②上述化学方程式中的系数m、n、p的正确关系是
③当降低温度时,C的浓度减小,正反应是
(2)如图表示在密闭容器中反应:2SO2(g)+O2(g)
 2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是
2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)对于下列反应:2SO2(g) + O2(g) 2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为
2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 __________________ 。
(2)下图表示在密闭容器中反应:2SO2+O2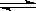 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是___________________ ; 请将增大压强时的反应速率变化情况画在c~d处:___________
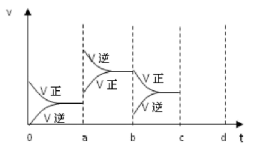
(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内混合气体的平均相对分子质量比原平衡时___________ (填“增大”、“减小”或“相等”)。
 2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为
2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 (2)下图表示在密闭容器中反应:2SO2+O2
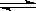 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内混合气体的平均相对分子质量比原平衡时
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】乙醇是一种优良燃料,在推动能源变革方面具有重要的作用。某地煤制乙醇的过程表示如图。
煤→⋯→乙酸甲酯 乙醇
乙醇
(1)Cu(NO3)2是制备“催化剂X”的重要试剂。

①气体A的名称是_______ 。
②实验室用Cu(NO3)2固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3的作用_______
(2)过程a包括以下3个主要反应:
Ⅰ.CH3COOCH3(g) +2H2(g)⇌C2H5OH(g)+CH3OH(g) ΔH1
Ⅱ. CH3COOCH3(g)+C2H5OH(g)⇌CH3COOC2H5(g)+CH3OH(g) ΔH2
Ⅲ.CH3COOCH3(g)+H2(g)⇌CH3CHO(g)+CH3OH(g) ΔH3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性(如乙醇选择性=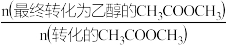 )如图所示。
)如图所示。
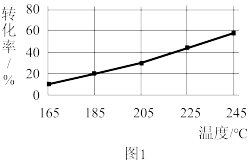
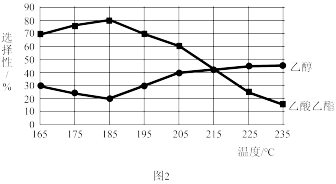
① 已知:ΔH1 <0。随温度降低,反应Ⅰ化学平衡常数的变化趋势是_______ 。
②下列说法不合理 的是_______ 。
a.温度可影响反应的选择性
b.225℃~235℃,反应Ⅰ处于平衡状态
c.增大H2的浓度,可以提高CH3COOCH3的转化率
③为防止“反应Ⅲ”发生,反应温度应控制的范围是_______ 。
④ 在185℃下,CH3COOCH3起始物质的量为5 mol,生成乙醇的物质的量是_______ 。
煤→⋯→乙酸甲酯
 乙醇
乙醇(1)Cu(NO3)2是制备“催化剂X”的重要试剂。

①气体A的名称是
②实验室用Cu(NO3)2固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3的作用
(2)过程a包括以下3个主要反应:
Ⅰ.CH3COOCH3(g) +2H2(g)⇌C2H5OH(g)+CH3OH(g) ΔH1
Ⅱ. CH3COOCH3(g)+C2H5OH(g)⇌CH3COOC2H5(g)+CH3OH(g) ΔH2
Ⅲ.CH3COOCH3(g)+H2(g)⇌CH3CHO(g)+CH3OH(g) ΔH3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性(如乙醇选择性=
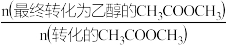 )如图所示。
)如图所示。 

① 已知:ΔH1 <0。随温度降低,反应Ⅰ化学平衡常数的变化趋势是
②下列说法
a.温度可影响反应的选择性
b.225℃~235℃,反应Ⅰ处于平衡状态
c.增大H2的浓度,可以提高CH3COOCH3的转化率
③为防止“反应Ⅲ”发生,反应温度应控制的范围是
④ 在185℃下,CH3COOCH3起始物质的量为5 mol,生成乙醇的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+ 11O2 2Fe2O3+ 8SO2
2Fe2O3+ 8SO2
该反应中氧化剂和氧化产物之比为______________ ;标准状态下得到4.48升SO2 时,一共转移了________ mol e-。
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的最佳反应条件是_________ 。
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 kJ,写出该反应的热化学方程式:____________________________________ 。若在该条件下将2 mol SO2放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 kJ,则此时SO2的转化率为____________ (用含Q1、Q2代数式表示)。
(4)市售浓硫酸的密度是1.84 g/cm3、质量分数为98 % ,若用H2SO4·XH2O来表示这种浓硫酸,则X为_________ 。
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+ 11O2
 2Fe2O3+ 8SO2
2Fe2O3+ 8SO2该反应中氧化剂和氧化产物之比为
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的最佳反应条件是
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A.400-500℃ 0.1 MPa | B.400℃ 10 MPa |
| C.500℃ 10 MPa | D.400-500℃ 1 MPa |
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 kJ,写出该反应的热化学方程式:
(4)市售浓硫酸的密度是1.84 g/cm3、质量分数为98 % ,若用H2SO4·XH2O来表示这种浓硫酸,则X为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表表示合成氨反应(N2+3H2 2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
分析上表数据,回答下列问题:
(1)200℃、100MPa时,平衡混合物中氨的含量已达0.988,如果继续增大压强______
(填“能”或“不能”)使平衡混合物中氨的含量等于1,理由是:___________________________________________________________________________________________ 。
(2)欲使平衡混合物中氨的含量增大,则可采取的措施有:____________________ 。
(3)欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:____________ 。
 2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。 压强(MPa) 压强(MPa) 氨的含量 氨的含量温度(℃) | 0.1 | 10 | 30 | 60 | 100 |
| 200 | 0.153 | 0.815 | 0.899 | 0.954 | 0.988 |
| 300 | 0.022 | 0.520 | 0.710 | 0.842 | 0.926 |
| 400 | 0.004 | 0.251 | 0.470 | 0.652 | 0.798 |
分析上表数据,回答下列问题:
(1)200℃、100MPa时,平衡混合物中氨的含量已达0.988,如果继续增大压强
(填“能”或“不能”)使平衡混合物中氨的含量等于1,理由是:
(2)欲使平衡混合物中氨的含量增大,则可采取的措施有:
(3)欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:
您最近半年使用:0次



