为确定某碱式碳酸镁 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸(
的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 为
为 ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
(1)98%的硫酸溶液物质的量浓度是___________ ;
(2)根据实验测定的数据,求出碱式碳酸镁化学式中X、Y、Z的比值(要求写出计算过程)___________ 。
 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸(
的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 为
为 ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:(1)98%的硫酸溶液物质的量浓度是
(2)根据实验测定的数据,求出碱式碳酸镁化学式中X、Y、Z的比值(要求写出计算过程)
2021·浙江台州·二模 查看更多[4]
浙江省台州市2021届高三4月选考科目教学质量评估试题(二模)化学试题(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)浙江省杭州市富阳区场口中学、桐庐富春中学2021-2022学年高二下学期(3月)检测化学试题
更新时间:2021-05-04 10:29:58
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】常温下,将20.0g质量分数为14.0%的KNO3溶液与30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.01 g/cm3的混合溶液。计算:
(1)混合后溶液的质量分数。_____
(2)混合后溶液的物质的量浓度。______
(3)在1000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?____
(1)混合后溶液的质量分数。
(2)混合后溶液的物质的量浓度。
(3)在1000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后回答下列问题:
(1)阿司匹林的相对分子质量为______ 。蔗糖的物质的量为______ mol。
(2)1 L“鲜花保鲜剂”中K+的物质的量浓度为(蔗糖、阿司匹林中不含K+)______ mol·L-1。
(3)使用时应将“鲜花保鲜剂”稀释至20倍后使用,稀释后c(AgNO3)=______ mol·L-1(用科学记数法表示)。
(4)配制1 L上述“鲜花保鲜剂”过程中,下列操作使配制浓度偏低的是______ 。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视
C.用蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液倒入废液缸中,防止污染环境
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)高锰酸钾的作用除了做钾肥外,还有消毒杀菌的作用,说明高锰酸钾具有______ 性。已知氯气也是常用消毒剂,“鲜花保鲜剂”中高锰酸钾的消毒效率(消毒效率是指单位质量的消毒剂得电子数的多少,KMnO4被还原为Mn2+)相当于氯气的______ 倍。(保留1位小数)
| 成分 | 质量/g | 摩尔质量/(g·mol-1) |
| 蔗糖 | 85.50 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 1.58 | 158 |
| 硝酸银 | 0.034 | 170 |
(2)1 L“鲜花保鲜剂”中K+的物质的量浓度为(蔗糖、阿司匹林中不含K+)
(3)使用时应将“鲜花保鲜剂”稀释至20倍后使用,稀释后c(AgNO3)=
(4)配制1 L上述“鲜花保鲜剂”过程中,下列操作使配制浓度偏低的是
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视
C.用蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液倒入废液缸中,防止污染环境
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)高锰酸钾的作用除了做钾肥外,还有消毒杀菌的作用,说明高锰酸钾具有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】物质的量在计算中有着举足轻重的地位。请根据物质的量的相关概念和公式,完成下列各题。
(1)等质量的 和
和 的物质的量之比为
的物质的量之比为__________ ,所含氢原子数之比为__________ 。
(2)标准状况下,在一体积可变的密闭容器中充有 由CO和
由CO和 组成的混合气体,该混合气体的体积为
组成的混合气体,该混合气体的体积为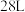 ,则该混合气体的平均摩尔质量为
,则该混合气体的平均摩尔质量为__________  ,CO、
,CO、 的体积比为
的体积比为__________ 。若将该混合气体在点燃条件下充分反应后,恢复到标准状况下,此时容器内的物质为__________ (填“纯净物”或“混合物”),体积为__________ L。
(3)把标准状况下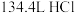 气体溶于
气体溶于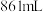 水中,所得溶液的密度为
水中,所得溶液的密度为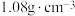 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为__________  。
。
(1)等质量的
 和
和 的物质的量之比为
的物质的量之比为(2)标准状况下,在一体积可变的密闭容器中充有
 由CO和
由CO和 组成的混合气体,该混合气体的体积为
组成的混合气体,该混合气体的体积为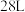 ,则该混合气体的平均摩尔质量为
,则该混合气体的平均摩尔质量为 ,CO、
,CO、 的体积比为
的体积比为(3)把标准状况下
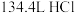 气体溶于
气体溶于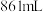 水中,所得溶液的密度为
水中,所得溶液的密度为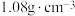 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现将芒硝(化学式为Na2SO4·10H2O)48.3 g配成2 L溶液,求该溶液中Na2SO4的物质的量浓度____________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】若胆矾中含有少量Cu(NO3)2·3H2O,测定其中CuSO4·5H2O的含量,实验步骤如下:称量胆矾样品的质量为m1,加水溶解,滴加足量BaCl2溶液,充分反应后过滤,将滤渣烘干、冷却,称得其质量为m2.样品中CuSO4·5H2O的质量分数为_______ (列出算式可能用到的化学式量:CuSO4 160、CuSO4·5H2O 250、Cu(NO3)2·3H2O 242、BaSO4 233)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)如图为物质B(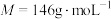 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。

①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为_______ g,物质的量为_______ mol;
②80℃时,物质饱和溶液的物质的量浓度为_______ mol∙L-1。
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。

计算:
①反应后溶液中c(H+)=_______ mol∙L-1 (忽略反应前后溶液体积变化);
②计算常温常压下的气体摩尔体积_______ L∙mol-1。
(1)如图为物质B(
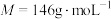 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为
②80℃时,物质饱和溶液的物质的量浓度为
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL
 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
计算:
①反应后溶液中c(H+)=
②计算常温常压下的气体摩尔体积
您最近一年使用:0次

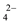 的物质的量为
的物质的量为

