下列叙述中正确的是
| A.乙硫醇(CH3CH2SH)沸点大于乙醇(CH3CH2OH),因为前者相对分子质量大 |
| B.[Cu(NH3)4]SO4·H2O中含离子键、极性共价键、配位键、分子间作用力 |
| C.原子的电子云轮廓图中小黑点表示核外电子运动过一次 |
| D.电负性越大的元素,第一电离能也越大 |
更新时间:2021-04-29 22:58:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】磷原子核外3p亚层中的电子,不相同的是
| A.电子云伸展方向 | B.电子云形状 |
| C.能量 | D.自旋方向 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确 的是
A. 、 、 、 、 分子中的键能依次减小 分子中的键能依次减小 |
| B.基态Cu中的电子从3d轨道跃迁到4s轨道要吸收能量 |
| C.核外电子运动的概率密度分布图(电子云图)就是原子轨道 |
| D.电子的运动状态可从能层、能级、原子轨道、自旋状态4个方面进行描述 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A. 分子形状呈三角锥形,是非极性分子 分子形状呈三角锥形,是非极性分子 |
| B.凡有规则外形的固体一定是晶体 |
| C.电负性越大的元素,第一电离能也越大 |
D. 分子中σ键与π键的数目之比是1:1 分子中σ键与π键的数目之比是1:1 |
您最近一年使用:0次
【推荐2】现有3种元素的基态原子的电子排布式如下:①1s22s22p63s23p3;②1s22s22p3;③1s22s22p5。则下列比较中,正确的是
| A.第一电离能:③>②>① | B.原子半径:①>③>② |
| C.电负性:③>①>② | D.最高化合价:③>②=① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】M、W、X、Y、Z是原子序数依次增大的同周期主族元素,基态X原子2p能级上仅有2个电子,Y元素原子的价层电子数是W的两倍,由五种元素组成的某电极材料的结构如图所示。下列说法正确的是
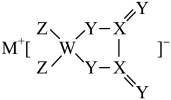
| A.氢化物沸点:X<Y |
| B.该化合物中必然存在配位键 |
| C.由M单质和Y单质反应生成的化合物中存在共价键 |
| D.基态原子未成对电子数:W<X<Y<Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温常压下,22.4L乙烯气体中σ键总数为5NA |
| B.1mol[Cu(NH3)4]SO4中含有的σ键总数16NA |
| C.常温常压下,2gD2O含有的质子数、电子数、中子数均为NA |
| D.1mol的CH3CH(NH2)COOH中,为sp3杂化的原子总数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不正确 的是
| A.向硫酸铜溶液中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解后得到深蓝色的透明溶液,形成该溶液是因为产生了配合离子[Cu(NH3)4] 2+ |
| B.NH4+的空间构型是正四面体形 |
| C.氨气极易溶于水的重要原因之一:氨分子与水分子之间能形成氢键 |
| D.由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于氢键,下列说法中不正确的是( )
| A.冰中的氢键有方向性和饱和性是导致冰的密度比水小的原因 |
| B.在水蒸气、水和冰中都含有氢键 |
| C.分子间若形成氢键,则物质的熔点和沸点较高 |
| D.HF是弱酸与氢键有关 |
您最近一年使用:0次

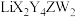 能有效减缓锂离子电池容量衰减,其结构式如图所示。其中Z原子满足8电子稳定结构,Z、Y、W、X是原子序数依次增大的短周期元素,X、Y原子核外均有2个未成对电子。下列说法正确的是
能有效减缓锂离子电池容量衰减,其结构式如图所示。其中Z原子满足8电子稳定结构,Z、Y、W、X是原子序数依次增大的短周期元素,X、Y原子核外均有2个未成对电子。下列说法正确的是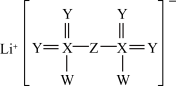
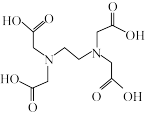 ,简写为H4Y)。在强酸性溶液中有六级离解平衡,相当于六元酸。下列说法不正确的是
,简写为H4Y)。在强酸性溶液中有六级离解平衡,相当于六元酸。下列说法不正确的是