写出下列物质的电子式
①Cl2_______ ; ②Na2O2_______ ; ③NaOH________ ;④HCl________ ; ⑤H2O2________ ; ⑥MgF2_______
①Cl2
更新时间:2021-05-22 09:18:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1) 的名称是
的名称是_______ ; 的电子式为
的电子式为_______ 。
(2)硫酸钾在水溶液中的电离方程式为_______ 。
(3)在加热条件下木炭与浓硫酸反应的化学方程式为_______ 。
(1)
 的名称是
的名称是 的电子式为
的电子式为(2)硫酸钾在水溶液中的电离方程式为
(3)在加热条件下木炭与浓硫酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中学化学教材中涉及许多金属和非金属元素,掌握它们的单质及其化合物的性质是学好化学的基础。回答下列问题:
(1) 的结构式为
的结构式为___________ ,过氧化钠的电子式为___________ 。
(2)黄磷(P4)与过量浓NaOH溶液反应,产生PH3和次磷酸钠( ),该反应的化学方程式为
),该反应的化学方程式为___________ ,其中还原剂和氧化剂的质量比为___________ ;根据题意可判断 是
是___________ 元酸(填“一”“二”或“三”)。
(3)向含有1mol 和1mol
和1mol 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①写出生成a的离子方程式:___________ 。
②n1=___________ 。
③向P点溶液中加入铜粉,反应的离子方程式为___________ ,最多可溶解铜粉___________ g。
(1)
 的结构式为
的结构式为(2)黄磷(P4)与过量浓NaOH溶液反应,产生PH3和次磷酸钠(
 ),该反应的化学方程式为
),该反应的化学方程式为 是
是(3)向含有1mol
 和1mol
和1mol 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
①写出生成a的离子方程式:
②n1=
③向P点溶液中加入铜粉,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求完成下列问题:
(1)请写出NaCl的电子式___________ ,甲烷的结构式___________ 。
(2)用反应方程式表示制备漂白粉的原理为:___________ 。
(3)漂白粉的有效成分是___________ ,小苏打的化学式为___________ 。
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示___________ 。
(1)请写出NaCl的电子式
(2)用反应方程式表示制备漂白粉的原理为:
(3)漂白粉的有效成分是
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答问题:
(1)①铁红的化学式是___________ ;②氨气的电子式___________ 。
(2)NaHCO3在水中的电离方程式:___________ 。
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目___________ 。
(4)关于固体NaHSO4的组成和性质的表述正确的是:___________ (填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
(1)①铁红的化学式是
(2)NaHCO3在水中的电离方程式:
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目
(4)关于固体NaHSO4的组成和性质的表述正确的是:
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
图1 图2
图2
①在图示的转化中,被还原的元素是_______ ,X的化学式为_______ 。
②钡元素在周期表中的位置是_______ 。
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:_______ 。
(3)利用ClO2氧化氮氧化物反应过程如下:NO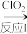 NO2
NO2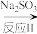 N2
N2
反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应Ⅱ的离子方程式是_______ 。
(4)加入过量次氯酸钠可使废水中NH 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。
①写出次氯酸钠的电子式_______ 。
②检验废水中是否存在NH 的方法是
的方法是_______ 。
③若处理废水产生了0.448L N2(标准状况),则需消耗浓度为2mol·L-1的次氯酸钠的体积为_______ mL。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
图1
 图2
图2
①在图示的转化中,被还原的元素是
②钡元素在周期表中的位置是
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:
(3)利用ClO2氧化氮氧化物反应过程如下:NO
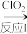 NO2
NO2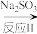 N2
N2反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应Ⅱ的离子方程式是
(4)加入过量次氯酸钠可使废水中NH
 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。①写出次氯酸钠的电子式
②检验废水中是否存在NH
 的方法是
的方法是③若处理废水产生了0.448L N2(标准状况),则需消耗浓度为2mol·L-1的次氯酸钠的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请写出下列反应的离子方程式:
①氯气与氯化亚铁溶液的反应_________________________________________________
②二氧化锰与浓盐酸反应_______________________________________________________
③氢氧化铝与足量氢氧化钠反应__________________________________________________
④ 偏铝酸钠与过量二氧化碳的反应________________________________________________
①氯气与氯化亚铁溶液的反应
②二氧化锰与浓盐酸反应
③氢氧化铝与足量氢氧化钠反应
④ 偏铝酸钠与过量二氧化碳的反应
您最近一年使用:0次
【推荐2】对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代的。某化学兴趣小组对下列三组物质进行研究:
A组:CaO、 、
、 、CuO
、CuO
B组: 、
、 、
、 、Cu
、Cu
C组: 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
(1)上表中应该分别填入:①_______ ,②_______ ,③_______ 。
(2)写出实验室制备 的化学反应方程式
的化学反应方程式_______ 。
(3)工业上用 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是_______ 。84消毒液与氯气相比具有贮运方便等优点,工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产100kg该溶液需消耗氯气的质量为_______ kg(保留整数)。
(4)采用“空气吹出法”可从浓海水吹出 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是_______ ,吸收 时,转移的电子数为
时,转移的电子数为_______ mol。
A组:CaO、
 、
、 、CuO
、CuOB组:
 、
、 、
、 、Cu
、CuC组:
 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
| 组别 | A组 | B组 | C组 |
| 分类标准 | 碱性氧化物 | ② | ③ |
| 不属于该类别的物质 | ① | Cu |  |
(1)上表中应该分别填入:①
(2)写出实验室制备
 的化学反应方程式
的化学反应方程式(3)工业上用
 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是(4)采用“空气吹出法”可从浓海水吹出
 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是 时,转移的电子数为
时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题:
(1) 个
个 分子的质量为
分子的质量为_______ g。
(2)常温下可用铁槽车运输浓硫酸,原因是_______ 。
(3)氯气可用于制备“战略金属”钛,有关反应为: ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目_______ 。
(4)氯气发生泄漏时,人员应_______ (填字母);同时喷 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为_______ 。
a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用_______ (填“玻璃”或“橡胶”)塞。
(1)
 个
个 分子的质量为
分子的质量为(2)常温下可用铁槽车运输浓硫酸,原因是
(3)氯气可用于制备“战略金属”钛,有关反应为:
 ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目(4)氯气发生泄漏时,人员应
 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放
 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据如图所示的转化关系以及现象回答下列问题。

(1)固体 X的化学式是:________________
(2)写出反应1 的化学方程式:____________________________
(3)写出反应2 的离子方程式:________________________________
(4)若15.6gX 和足量的气体 A反应,转移__________ mol 电子。

(1)固体 X的化学式是:
(2)写出反应1 的化学方程式:
(3)写出反应2 的离子方程式:
(4)若15.6gX 和足量的气体 A反应,转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列物质:①稀盐酸②小苏打③氨水④二氧化碳⑤ 固体⑥NaOH稀溶液⑦硝酸亚铁溶液⑧铁⑨石墨⑩过氧化钠。按要求填空:
固体⑥NaOH稀溶液⑦硝酸亚铁溶液⑧铁⑨石墨⑩过氧化钠。按要求填空:
(1)上述物质中属于电解质的为_______ (填标号,下同);可以导电的为_______ 。
(2)⑦中溶质的电离方程式为_______ ;①和⑧反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,小苏打与胃酸反应的离子方程式为_______ 。
(4)⑩中氧元素的化合价为_______ 价,⑩与④发生反应的化学方程式为_______ 。
 固体⑥NaOH稀溶液⑦硝酸亚铁溶液⑧铁⑨石墨⑩过氧化钠。按要求填空:
固体⑥NaOH稀溶液⑦硝酸亚铁溶液⑧铁⑨石墨⑩过氧化钠。按要求填空:(1)上述物质中属于电解质的为
(2)⑦中溶质的电离方程式为
(3)小苏打可用于治疗胃酸过多,小苏打与胃酸反应的离子方程式为
(4)⑩中氧元素的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:

(1)若A为水,B为过氧化钠,C中盛有酸化过的FeCl2溶液,旋开活塞E后,烧瓶中发生反应的化学方程式为_________ ,C中的现象为___________________ ;
(2)利用上述装置可以验证物质的性质,如设计证明氧化性:KMnO4>Cl2并制取漂白液(有效成分为NaClO),则A为浓盐酸,B为高锰酸钾C中发生反应的离子方程式为________ D装置的作用是:___________ 也可设计证明酸性的强弱:H2SO4>H2CO3>H2SiO3则A为硫酸、B为纯碱、C中盛有水玻璃,则小试管中的现象是_____________ ;
(3)利用上述装置可以验证SO2的性质,若A为浓硫酸,B为亚硫酸钠固体,那么C中盛有__________ 溶液时可验证其具有漂白性;而C中盛有_________ 溶液时可验证其具有还原性。

(1)若A为水,B为过氧化钠,C中盛有酸化过的FeCl2溶液,旋开活塞E后,烧瓶中发生反应的化学方程式为
(2)利用上述装置可以验证物质的性质,如设计证明氧化性:KMnO4>Cl2并制取漂白液(有效成分为NaClO),则A为浓盐酸,B为高锰酸钾C中发生反应的离子方程式为
(3)利用上述装置可以验证SO2的性质,若A为浓硫酸,B为亚硫酸钠固体,那么C中盛有
您最近一年使用:0次



