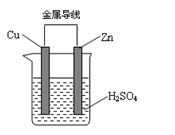
如图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:
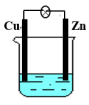
(1)Zn电极是___________ (填“正”或“负”)极,其电极反应为___________ ,该反应是___________ (填“氧化”或“还原”,下同)反应;
(2)Cu电极是___________ 极,其电极反应为___________ ,该反应是___________ 反应。
(3)装置中锌的作用是___________ ,稀硫酸的作用是___________
A.电极材料 B.电极反应物
C.电子导体 D.离子导体

(1)Zn电极是
(2)Cu电极是
(3)装置中锌的作用是
A.电极材料 B.电极反应物
C.电子导体 D.离子导体
更新时间:2021-06-01 09:17:11
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)将锌片、铜片按照如图所示装置连接,铜片做____ 极(填“正”或“负”),外电路电子的流向为_____ (填“Cu→Zn”或“Zn→Cu”)。
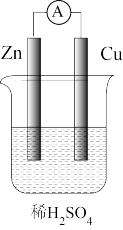
若将装置中的稀H2SO4用CuSO4溶液替代,当转移2mol电子时,溶液质量_____ (填变大,变小,不变)如果有变化则变化____ g。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:____ 。正极电极反应式_____ 。当线路中转移0.2mol电子时,则被腐蚀铜的质量为:____ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)下列关于能源说法不正确的是____ (填序号)。
(1)将锌片、铜片按照如图所示装置连接,铜片做

若将装置中的稀H2SO4用CuSO4溶液替代,当转移2mol电子时,溶液质量
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)下列关于能源说法不正确的是
| A.煤、石油、天然气是现代社会主要能源,由此获取热能的主要途径是通过物质的燃烧 |
| B.化石燃料燃烧排放的粉尘、SO2、NOx、CO2等是大气污染物的主要来源 |
| C.新能源有太阳能、风能、地热能、海洋能和氢能等 |
| D.在能量利用阶段,可采取合理的措施促进能源循环利用,提高能源利用率 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
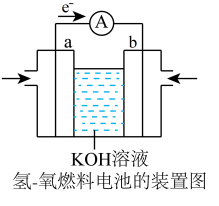
【推荐2】航天技术上使用的一种氢—氧燃料电池原理可以简单看作下图,则:工作时,氢燃料通入该电池的___________ (填电极名称),OH-向___________ (a或b)极移动。

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是________ ,再用导线把锌片和铜片连接起来,在导线中间接入灵敏电流计,灵敏电流计上观察到的现象是________ ;该原电池中电子流动的方向是________ ,总反应的化学方程式是________ ,其中________ 元素被氧化,________ 极上发生还原反应;在上述化学方程式上方用单线桥标出电子转移的方向和数目。___________


您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应: ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
(1)B的转化率___________ 。
(2)恒温达平衡时容器内的压强与开始时压强比___________ 。
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
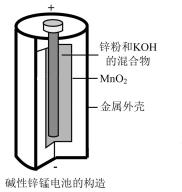
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是___________ (填名称),负极上发生的电极反应为___________ 。若反应消耗13g负极材料,则电池中转移电子的物质的量为___________ mol。
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为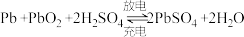 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。
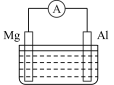
(5)镁铝电池的构造如图所示,当电解质溶液为NaOH溶液时,可知电池的负极材料为_______ (填“Mg”或“Al”),正极上的电极反应式为___________ 。
 ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:(1)B的转化率
(2)恒温达平衡时容器内的压强与开始时压强比
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为
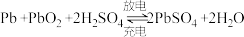 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。| A.电解液中H2SO4的浓度始终保持不变 |
B.放电时正极上的电极反应式为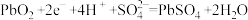 |
| C.放电时,当外电路通过1mol电子时,理论上负极质量增加48g |
D.放电时,溶液中的 向正极移动 向正极移动 |

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
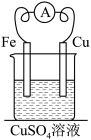
【推荐3】(1)由铜、铁和硫酸铜溶液组成的原电池中,作正极的是________ (填化学式),正极的电极反应式为____________________________ ;电子由______ (填“正”或“负”,下同)极经导线移向______ 极,总反应的离子方程式为_________________________ 。
(2)若以反应 来设计原电池,则电池的负极材料是
来设计原电池,则电池的负极材料是______________ (填化学式,下同),电解质溶液为________________ 溶液。
(2)若以反应
 来设计原电池,则电池的负极材料是
来设计原电池,则电池的负极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】相对分子质量为44的烷烃和O2气在KOH溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为O2 +2e-+2 H2O= 4OH-
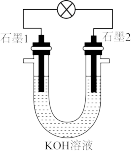
(1)石墨1极为_______ (填“负”或“正”)极。在石墨2极上发生的电极反应为_______
(2)放电时,电子流向是_______ (填字母)。
a.由石墨1极流出,经外电路流向石墨2极
b.由石墨2极流出,经电解质溶液流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极
d.由石墨2极流出,经外电路流向石墨1极

(1)石墨1极为
(2)放电时,电子流向是
a.由石墨1极流出,经外电路流向石墨2极
b.由石墨2极流出,经电解质溶液流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极
d.由石墨2极流出,经外电路流向石墨1极
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图。

(1)Pt电极(a)为_______ 极(填“正”或“负”);Pt电极(b)上的电极反应式为_______ 。
(2)该过程总反应的化学反应方程式为_______ ,反应一段时间后,KOH溶液的浓度将_______ (填“增大”“减小”或“不变”)。当消耗0.1 mol O2时,理论上转移电子个数为_______ ;
(3)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是_______ (填名称),发生的电极反应式为_______ 。

(1)Pt电极(a)为
(2)该过程总反应的化学反应方程式为
(3)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
您最近一年使用:0次