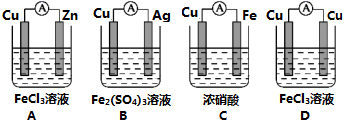
I.原电池可将化学能转化为电能。由A、B、C、D四种金属按下表中装置进行实验:
(1)装置甲中 向
向___________ 极移动(填“A”或“B”);
(2)四种金属活动性由强到弱的顺序是___________ ;
(3)若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g.则导线中通过电子的物质的量为___________ mol。
II.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下图为甲烷燃料电池的构造示意图,由此判断

Y极为电池的___________ 极,X极的电极反应方程式为___________ ,电路中每转移0.2mol电子,标准状况下正极上消耗气体的体积是___________ L。
(2)为了验证Fe3+与Cu2+氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是___________ 。
(3)铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
Pb +PbO2+2H2SO4.铅蓄电池放电时正极是___________ (填物质化学式),该电极质量___________ (填“增加”或“减少)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到___________ mol/L。
| 装置 | 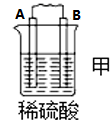 | 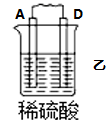 | 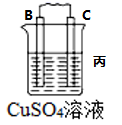 |
| 现象 | B上有气体产生 | D不断溶解 | C质量增加 |
(1)装置甲中
 向
向(2)四种金属活动性由强到弱的顺序是
(3)若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g.则导线中通过电子的物质的量为
II.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下图为甲烷燃料电池的构造示意图,由此判断

Y极为电池的
(2)为了验证Fe3+与Cu2+氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是

(3)铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O
 Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
更新时间:2021-05-21 11:17:45
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】甲醇是一种重要的化工原料,在化工领域有广泛应用。
(1)甲醇燃料电池由于结构简单、能量转化率高、对环境天污染,可作为常规能源的替代品而越来越受到关注。其工作原理如如图所示:
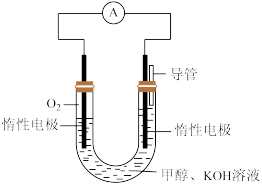
①该电池正极的电极反应为___ ,放电过程中负极区域溶液的pH值___ (填“变大”或“变小”或“不变”)。
②该电池总反应的化学方程式为___ 。
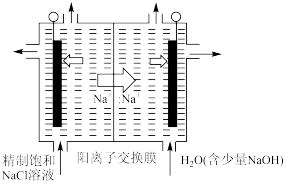
(2)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高校、光谱、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
①如图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为____ 。
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为___ mol。
(3)英国《自然》杂志近期报道了一种新型铝离子电池,以金属铝和石墨为电极,用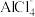 和有机阳离子构成电解质溶液,其放电工作原理如图所示。
和有机阳离子构成电解质溶液,其放电工作原理如图所示。

①电池放电时负极的电极反应式为___ 。
②充电时有机阳离子向___ 电极移动(填“铝”或“石墨”)。
③电池充电时,电路中每转移0.15mol电子,理论上生成___ g铝。
(1)甲醇燃料电池由于结构简单、能量转化率高、对环境天污染,可作为常规能源的替代品而越来越受到关注。其工作原理如如图所示:

①该电池正极的电极反应为
②该电池总反应的化学方程式为
(2)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高校、光谱、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
①如图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为

(3)英国《自然》杂志近期报道了一种新型铝离子电池,以金属铝和石墨为电极,用
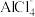 和有机阳离子构成电解质溶液,其放电工作原理如图所示。
和有机阳离子构成电解质溶液,其放电工作原理如图所示。
①电池放电时负极的电极反应式为
②充电时有机阳离子向
③电池充电时,电路中每转移0.15mol电子,理论上生成
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,甲、乙是电化学实验装置,请回答下列问题:

(1)若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是____________ 。
②将湿润的淀粉KI试纸放在乙烧杯的上方,发现试纸先变蓝后褪色,这是因为电解生成的某种气体A氧化了I-生成了I2。若A气体和I2按物质的量之比为5∶1反应,且生成两种酸,该反应的化学方程式为_________ 。
③如果不考虑气体产物与烧杯中溶液之间的反应,当乙反应有0.01 mol电子转移后停止实验,烧杯中溶液的体积为100 mL,则溶液混匀后的c(OH-)=_____ 。
(2)若甲、乙两烧杯中均盛放CuSO4溶液。
①甲中铁棒上的电极反应式为_______________ 。
②乙中总反应的离子方程式为_________________ 。
③如果起始时乙中盛放100 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的c(H+)=0.1mol/L,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入_____ (填写物质的化学式)______ g。

(1)若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是
②将湿润的淀粉KI试纸放在乙烧杯的上方,发现试纸先变蓝后褪色,这是因为电解生成的某种气体A氧化了I-生成了I2。若A气体和I2按物质的量之比为5∶1反应,且生成两种酸,该反应的化学方程式为
③如果不考虑气体产物与烧杯中溶液之间的反应,当乙反应有0.01 mol电子转移后停止实验,烧杯中溶液的体积为100 mL,则溶液混匀后的c(OH-)=
(2)若甲、乙两烧杯中均盛放CuSO4溶液。
①甲中铁棒上的电极反应式为
②乙中总反应的离子方程式为
③如果起始时乙中盛放100 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的c(H+)=0.1mol/L,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有如下两个反应:
①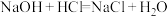
②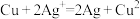
(1)根据上述两个反应的本质,判断它们能否设计成原电池:_________________________________ 。
(2)如果不能,说明原因:_________________________________________ 。
(3)如果能,则写出正、负极材料及其电极反应式。
①负极:_______________ ,_________________________________________ 。
②正极:_______________ ,_________________________________________ 。
①
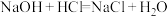
②
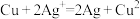
(1)根据上述两个反应的本质,判断它们能否设计成原电池:
(2)如果不能,说明原因:
(3)如果能,则写出正、负极材料及其电极反应式。
①负极:
②正极:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某小组学生研究常见的金属腐蚀现象,分析其原理.按要求回答下列问题.
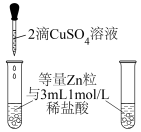
(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的________ 。其原因是________________ 。
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
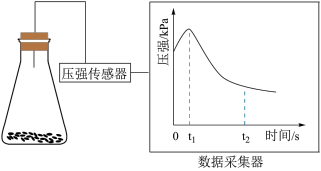
① 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为________ 。
② 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为________________ 。
③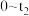 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________ (填“氧化反应”或“还原反应”)。
②写出使用暖贴时的注意事项:________________ 。
③暖贴发热时,正极材料为________ ;食盐的作用为________ 。
④当暖贴放热结束时,铁粉转化成的物质中可能含有________ 。

(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③
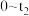 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度 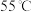 ,最高温度 ,最高温度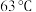 ,发热时间12小时以上 ,发热时间12小时以上 |
②写出使用暖贴时的注意事项:
③暖贴发热时,正极材料为
④当暖贴放热结束时,铁粉转化成的物质中可能含有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)某兴趣小组为研究原电池原理,设计如图装置。
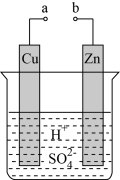
①a和b不连接时,烧杯中发生反应的离子方程式是_____ 。
②a和b用导线连接,Cu极为原电池____ 极(填“正”或“负”),Zn极发生____ 反应,外电路中,电子流向____ 极(填“正”或“负”,下同),内电路溶液中,SO 移向
移向____ 极。
(2)有同学想把CuO与稀H2SO4的反应设计成原电池,你认为是否可行____ (填“是”或“否”),理由是____ 。
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是
②a和b用导线连接,Cu极为原电池
 移向
移向(2)有同学想把CuO与稀H2SO4的反应设计成原电池,你认为是否可行
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请根据反应Fe+CuSO4==Cu+FeSO4设计一个原电池,画出装置图
_____________________

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示,组成原电池,回答下列问题。
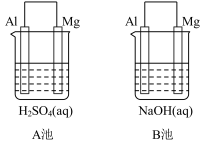
(1)该装置是把___________ 能转化为_________ 能的装置。
(2)A池中Mg电极是__________ (填“正”或“负”)极,其在反应中_____ (填“得到”或“失去”)电子,该极发生的反应是__________ (填“氧化”或“还原”)反应,其电极反应为________________________ ,该装置中电流的方向是由_____ 到 ______ 。
(3)B池中负极材料是_________ ,该装置中电子的移动方向是由_____ 到 ______ 。

(1)该装置是把
(2)A池中Mg电极是
(3)B池中负极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.铅蓄电池是典型的可充型电池,电池总反应为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O。
2PbSO4+2H2O。
请回答下列问题:
(1)放电时,负极材料是___ ;电解液中H2SO4的浓度将变___ (选“变大”“变小”或“不变”);
(2)充电时,阳极的电极反应式是___ 。
II.如图是一个化学过程的示意图。
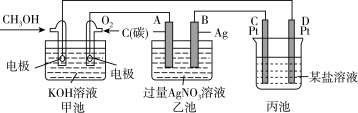
(1)图中甲池是___ 装置(填“电解池”或“原电池”),其中K+移向___ 极(选“正”或“负”)
(2)乙池中石墨电极A上发生的电极反应式:___ 。
(3)若丙内为足量NaCl溶液,当甲池内通入11.2LO2(标准状况下),则丙池中产生的气体的体积为____ L(标准状况下)。
 2PbSO4+2H2O。
2PbSO4+2H2O。请回答下列问题:
(1)放电时,负极材料是
(2)充电时,阳极的电极反应式是
II.如图是一个化学过程的示意图。

(1)图中甲池是
(2)乙池中石墨电极A上发生的电极反应式:
(3)若丙内为足量NaCl溶液,当甲池内通入11.2LO2(标准状况下),则丙池中产生的气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常见铅蓄电池是二次电池,其电极材料分别为Pb和PbO2,电解液为稀H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O。请依据上述情况判断:
2PbSO4+2H2O。请依据上述情况判断:
(1)铅蓄电池的负极材料是_______ 。
(2)请依据两极材料总反应,写出放电时正极反应是_______ 。
(3)请依据总反应式和正极反应式,写出放电时负极反应是_______ 。
 2PbSO4+2H2O。请依据上述情况判断:
2PbSO4+2H2O。请依据上述情况判断:(1)铅蓄电池的负极材料是
(2)请依据两极材料总反应,写出放电时正极反应是
(3)请依据总反应式和正极反应式,写出放电时负极反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】原电池装置如图所示。回答下列问题
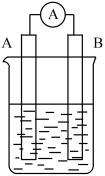
(1)若A、B均为铂片,分别从A、B两极通入 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为_______ (填正极或负极)写出B电极的电极反应式:_______ ,溶液中的 向
向_______ (填“A”或“B”)极移动;当烧杯内的液体为氢氧化钾溶液,此时A电极的电极反应式:_______ ,当消耗0.2mol氧气时,电路中通过电子数为_______ 。
(2)若A为Pb,B为 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: 。写出B电极的电极反应式:
。写出B电极的电极反应式:_______ 。

(1)若A、B均为铂片,分别从A、B两极通入
 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为 向
向(2)若A为Pb,B为
 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: 。写出B电极的电极反应式:
。写出B电极的电极反应式:
您最近一年使用:0次




