次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)在印染、医药以及原子能工业中应用广泛.以Na2SO3、SO2,HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
步骤1:如图1所示,在烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,制得NaHSO3溶液。
步骤2:将装置A中导气管换成橡皮塞,向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在95~100℃下,反应约3h,冷却至室温抽滤。
步骤3:将滤液经系列操作得到次硫酸氢钠甲醛晶体。
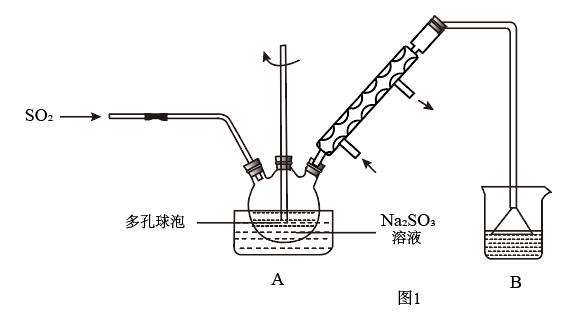
(1)A中多孔球泡的作用是___ 。
(2)①步骤2中,反应生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的实验操作是___ 。
②写出步骤2中制备NaHSO2•HCHO•2H2O反应的化学方程式:___ 。
(3)B中的试剂为___ 溶液。
(4)ZnSO4的溶解度随温度的变化如图2所示,请补充完整由副产品Zn(OH)2获得ZnSO4•7H2O的实验方案:将副产品Zn(OH)2置于烧杯中,___ (实验中可选用的试剂:稀硫酸、无水乙醇)。

(5)通过下列方法测定产品纯度:准确称取2.000gNaHSO2•HCHO•2H2O样品,完全溶于水配成100.00mL溶液,取20.00mL于碘量瓶中,加入50.00mL0.09000mol·L-1I2标准溶液,振荡,于暗处充分反应。以淀粉溶液为指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液10.00mL。测定过程中发生下列反应:NaHSO2•HCHO•2H2O+2I2=NaHSO4+4HI+HCHO,2S2O +I2=S4O
+I2=S4O +2I-,则NaHSO2•HCHO•2H2O样品的纯度为
+2I-,则NaHSO2•HCHO•2H2O样品的纯度为___ 。
步骤1:如图1所示,在烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,制得NaHSO3溶液。
步骤2:将装置A中导气管换成橡皮塞,向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在95~100℃下,反应约3h,冷却至室温抽滤。
步骤3:将滤液经系列操作得到次硫酸氢钠甲醛晶体。

(1)A中多孔球泡的作用是
(2)①步骤2中,反应生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的实验操作是
②写出步骤2中制备NaHSO2•HCHO•2H2O反应的化学方程式:
(3)B中的试剂为
(4)ZnSO4的溶解度随温度的变化如图2所示,请补充完整由副产品Zn(OH)2获得ZnSO4•7H2O的实验方案:将副产品Zn(OH)2置于烧杯中,

(5)通过下列方法测定产品纯度:准确称取2.000gNaHSO2•HCHO•2H2O样品,完全溶于水配成100.00mL溶液,取20.00mL于碘量瓶中,加入50.00mL0.09000mol·L-1I2标准溶液,振荡,于暗处充分反应。以淀粉溶液为指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液10.00mL。测定过程中发生下列反应:NaHSO2•HCHO•2H2O+2I2=NaHSO4+4HI+HCHO,2S2O
 +I2=S4O
+I2=S4O +2I-,则NaHSO2•HCHO•2H2O样品的纯度为
+2I-,则NaHSO2•HCHO•2H2O样品的纯度为
更新时间:2021/06/04 13:23:00
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】张明同学对硫酸及其盐的某些性质中进行了如下实验探究。
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如右图所示的实验装置后,加热装置甲。(夹持和加热装置省略)

(1)该装置设计上存在明显缺陷,其缺陷是 _________________________________ ___。
(2)装置甲中反应的化学方程式是___________ ___。
(3)装置乙中的试剂是_____________________________________________________。
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
[实验三]用KHSO4制取H2O2并测其质量分数
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:
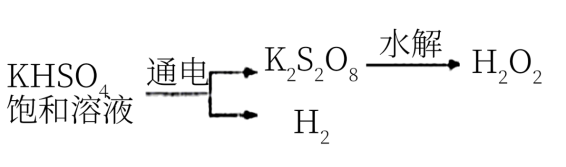
张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4―+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00 mL H2O2溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000 mol/L KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00 mL、19.98 mL、20.02 mL。
请回答:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为____________________________。
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快。Mn2+的作用是_____________ ___。
(7)原H2O2溶液中溶质的质量分数是__________ _____ ____。
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如右图所示的实验装置后,加热装置甲。(夹持和加热装置省略)

(1)该装置设计上存在明显缺陷,其缺陷是 _________________________________ ___。
(2)装置甲中反应的化学方程式是___________ ___。
(3)装置乙中的试剂是_____________________________________________________。
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
| 实验操作 | 预期现象和结论 |
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:

张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4―+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00 mL H2O2溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000 mol/L KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00 mL、19.98 mL、20.02 mL。
请回答:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为____________________________。
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快。Mn2+的作用是_____________ ___。
(7)原H2O2溶液中溶质的质量分数是__________ _____ ____。
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】实验室中以活性炭为催化剂制备 并测定钴元素的含量。
并测定钴元素的含量。
已知: 是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生
是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生 、
、 ;
; 不易被氧化,
不易被氧化, 有较强还原性。
有较强还原性。
Ⅰ.制备晶体(装置如图1,55℃水浴加热)
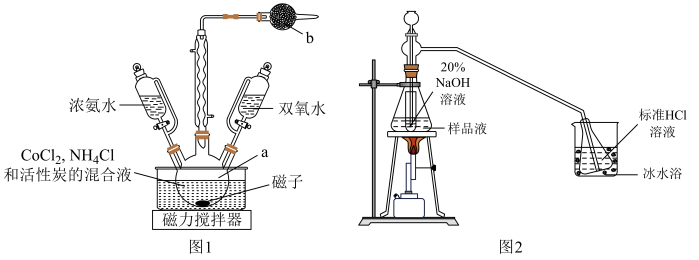
Ⅱ.测定产品 中钴元素的含量(装置如图2)
中钴元素的含量(装置如图2)
称取 样品于锥形瓶中,加水溶解。在另一锥形瓶中加入
样品于锥形瓶中,加水溶解。在另一锥形瓶中加入 标准
标准 溶液并置于冰水浴中,向漏斗中加入足量
溶液并置于冰水浴中,向漏斗中加入足量 的
的 溶液,加热,保持微沸状态一段时间后,取出插入标准
溶液,加热,保持微沸状态一段时间后,取出插入标准 溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准
溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准 溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
溶液的锥形瓶中。取出锥形瓶,加入指示剂,用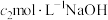 标准溶液滴定剩余的
标准溶液滴定剩余的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 。
。
回答下列问题:
(1) 制备
制备 的化学方程式为
的化学方程式为___________ 。
(2)仪器a的名称是___________ ;b中的试剂是___________ 。
(3)向 、
、 和活性炭混合液中先加浓氨水目的是
和活性炭混合液中先加浓氨水目的是___________ 。
(4)样品中钴元素的质量分数为___________ (用含 、
、 、
、 、
、 、
、 的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果
的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
(5)① 的空间结构为正八面体,若
的空间结构为正八面体,若 中2个
中2个 被2个
被2个 取代,能得到
取代,能得到___________ 种产物。
②钴(Ⅱ)与氯化钴和氨水以及 反应中若不加活性炭催化剂,可能有
反应中若不加活性炭催化剂,可能有 、
、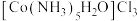 生成。现有
生成。现有 浓度为
浓度为 的
的 或
或 溶液,用
溶液,用 的
的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 ,则该溶液中的溶质为
,则该溶液中的溶质为___________ (填化学式)。
 并测定钴元素的含量。
并测定钴元素的含量。已知:
 是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生
是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生 、
、 ;
; 不易被氧化,
不易被氧化, 有较强还原性。
有较强还原性。Ⅰ.制备晶体(装置如图1,55℃水浴加热)

Ⅱ.测定产品
 中钴元素的含量(装置如图2)
中钴元素的含量(装置如图2)称取
 样品于锥形瓶中,加水溶解。在另一锥形瓶中加入
样品于锥形瓶中,加水溶解。在另一锥形瓶中加入 标准
标准 溶液并置于冰水浴中,向漏斗中加入足量
溶液并置于冰水浴中,向漏斗中加入足量 的
的 溶液,加热,保持微沸状态一段时间后,取出插入标准
溶液,加热,保持微沸状态一段时间后,取出插入标准 溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准
溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准 溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
溶液的锥形瓶中。取出锥形瓶,加入指示剂,用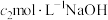 标准溶液滴定剩余的
标准溶液滴定剩余的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 。
。回答下列问题:
(1)
 制备
制备 的化学方程式为
的化学方程式为(2)仪器a的名称是
(3)向
 、
、 和活性炭混合液中先加浓氨水目的是
和活性炭混合液中先加浓氨水目的是(4)样品中钴元素的质量分数为
 、
、 、
、 、
、 、
、 的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果
的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果(5)①
 的空间结构为正八面体,若
的空间结构为正八面体,若 中2个
中2个 被2个
被2个 取代,能得到
取代,能得到②钴(Ⅱ)与氯化钴和氨水以及
 反应中若不加活性炭催化剂,可能有
反应中若不加活性炭催化剂,可能有 、
、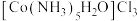 生成。现有
生成。现有 浓度为
浓度为 的
的 或
或 溶液,用
溶液,用 的
的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 ,则该溶液中的溶质为
,则该溶液中的溶质为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
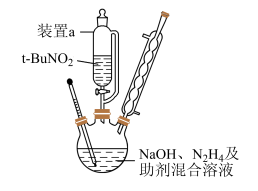
【推荐3】叠氮化钠(NaN3)是一种白色剧毒晶体,是汽车安全气囊的主要成分;易溶于水,微溶于乙醇,水溶液呈弱碱性,能与酸发生反应产生具有爆炸性的有毒气体叠氮化氢。实验室可利用亚硝酸叔丁酯(t-BuNO2,以t-Bu表示叔丁基)与N2H4、氢氧化钠溶液混合反应制备NaN3。
(1)用化学语言解释NaN3溶液呈弱碱性的原因:__________ 。
(2)制备NaN3
按图示组装仪器(加热装置略)进行反应,反应的化学方程式为: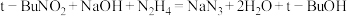 。
。
①装置a的名称是____________ ;
②反应后溶液在 下冷却至有大量晶体析出后过滤。所得晶体使用
下冷却至有大量晶体析出后过滤。所得晶体使用_______ 洗涤;
③试解释低温下过滤的原因是__________ 。
(3)产率计算
①称取2.0g NaN3试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol/L(NH4)2Ce(NO3)6溶液40.00mL (假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol/L(NH4)2Fe(SO4)2标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。
i.配平(NH4)2Ce(NO3)6与叠氮化钠反应方程式:
____ (NH4)2Ce(NO3)6+____ NaN3=____ NH4NO3+____ Ce(NO3)3____ NaNO3+____ N2↑;
ii.计算NaN3的质量分数为____ (保留2位有效数字);
iii.下列操作会导致所测定样品中NaN3质量分数偏大的是_________ 。
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加(NH4)2Ce(NO3)6溶液时,滴加前俯视读数,滴加后仰视读数
C.滴定过程中,将挂在锥形瓶壁上的(NH4)2Ce(NO3)6标准液滴用蒸馏水冲进瓶内
(4)分析不直接用酸性高锰酸钾滴定NaN3可能的原因是_________ 。
(5) NaN3有毒,可以使用NaClO溶液对含有NaN3的溶液进行销毁,反应产生无色无味的无毒气体,试写出反应的离子方程式_________ 。

(1)用化学语言解释NaN3溶液呈弱碱性的原因:
(2)制备NaN3
按图示组装仪器(加热装置略)进行反应,反应的化学方程式为:
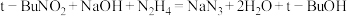 。
。①装置a的名称是
②反应后溶液在
 下冷却至有大量晶体析出后过滤。所得晶体使用
下冷却至有大量晶体析出后过滤。所得晶体使用③试解释低温下过滤的原因是
(3)产率计算
①称取2.0g NaN3试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol/L(NH4)2Ce(NO3)6溶液40.00mL (假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol/L(NH4)2Fe(SO4)2标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。
i.配平(NH4)2Ce(NO3)6与叠氮化钠反应方程式:
ii.计算NaN3的质量分数为
iii.下列操作会导致所测定样品中NaN3质量分数偏大的是
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加(NH4)2Ce(NO3)6溶液时,滴加前俯视读数,滴加后仰视读数
C.滴定过程中,将挂在锥形瓶壁上的(NH4)2Ce(NO3)6标准液滴用蒸馏水冲进瓶内
(4)分析不直接用酸性高锰酸钾滴定NaN3可能的原因是
(5) NaN3有毒,可以使用NaClO溶液对含有NaN3的溶液进行销毁,反应产生无色无味的无毒气体,试写出反应的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】砂质土壤分析中常用 Karl Fischer法是测定其中微量水含量,该方法是利用I2和SO2反应定量消耗水作为原理(假设土壤中其他成分不参加反应),据此回答下列问题:
(1)写出该反应的化学反应方程式:_______________________ 。
步骤I:反应样品中的水
下图是某同学在实验室模拟Karl Fischer法的实验装置图:

(2)装置连接的顺序为a→____________ (填接口字母顺序);M仪器的名称为________________ ,其在实验过程中的作用是:____________ ;
(3)操作步骤为:①连接装置并检查装置气密性,②装入药品,____________________ ;③关闭弹簧夹,打开分液漏斗活塞;④反应结束后,关闭分液漏斗活塞,继续通入N2 ,⑤取下D装置,···
步骤④中继续通入N2的目的是________________________________
步骤 II:测定剩余的碘
向反应后的D装置加入蒸馏水,过滤,充分洗涤,并合并洗涤液和滤液,将其配成250.00mL溶液,取 25.00mL 用0.20 mol·L-1 Na2S2O3标准液滴定剩余的I2单质,已知反应如下:2S2O32-+I2=S4O62-+2I-。
(4)Na2S2O3标准液应装在_____________ (填“酸式”、“碱式”)滴定管中;上述操作中,合并洗涤液和滤液的目的是__________________________ ;
(5)滴定实验重复四次得到数据如下:
①若实验开始时,向D 装置中加入10.00 g土壤样品和10.16克I2(已知I2过量),则样品土壤中水的含量为_________ %。
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将____________ (填“偏高”、“ 偏低”或“不变”)。
(1)写出该反应的化学反应方程式:
步骤I:反应样品中的水
下图是某同学在实验室模拟Karl Fischer法的实验装置图:

(2)装置连接的顺序为a→
(3)操作步骤为:①连接装置并检查装置气密性,②装入药品,
步骤④中继续通入N2的目的是
步骤 II:测定剩余的碘
向反应后的D装置加入蒸馏水,过滤,充分洗涤,并合并洗涤液和滤液,将其配成250.00mL溶液,取 25.00mL 用0.20 mol·L-1 Na2S2O3标准液滴定剩余的I2单质,已知反应如下:2S2O32-+I2=S4O62-+2I-。
(4)Na2S2O3标准液应装在
(5)滴定实验重复四次得到数据如下:
| 实验 | ① | ② | ③ | ④ |
| 消耗的标准液的体积/mL | 18.37 | 20.05 | 19.95 | 20.00 |
①若实验开始时,向D 装置中加入10.00 g土壤样品和10.16克I2(已知I2过量),则样品土壤中水的含量为
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某实验小组在探究 对氨法脱硫工艺的影响。
对氨法脱硫工艺的影响。
步骤Ⅰ.模拟氨法脱硫
在通风橱中选择合适的装置模拟工业过程中利用氨水吸收 (夹持装置省略)。
(夹持装置省略)。___________ 。
(2)装置B中使用多孔球泡的目的是___________ 。
(3)装置C中盛放的药品是___________ 。
(4)取2.00mL装置B中制得溶液[S(Ⅳ)含量以 计]于盛有
计]于盛有 标准碘溶液的碘量瓶中,调节pH后以淀粉为指示剂,用
标准碘溶液的碘量瓶中,调节pH后以淀粉为指示剂,用 溶液进行滴定,平均消耗
溶液进行滴定,平均消耗 溶液的体积为8.00mL。
溶液的体积为8.00mL。
①碘量瓶中 和
和 反应的离子方程式为
反应的离子方程式为___________ 。
②步骤Ⅰ中制得溶液
___________ 。
③若直接使用标准碘溶液滴定 ,则会导致测得
,则会导致测得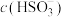
___________ (填“偏大”“偏小”或“无影响”)。
步骤Ⅱ.亚硫酸氢铵的氧化
取步骤Ⅰ制得溶液平均分成5份,分别添加 (HCl酸化)使溶液中
(HCl酸化)使溶液中 达到指定浓度,持续通入空气,反应180min后,测得各组
达到指定浓度,持续通入空气,反应180min后,测得各组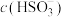 变化量及
变化量及 变化量如下表所示:
变化量如下表所示:
(5)实验组别1的目的是___________ 。
(6) 过高时,
过高时, 的氧化率[
的氧化率[ ]降低的原因为
]降低的原因为___________ 。
(7)进一步设计实验确定最佳 ,应调控
,应调控 的范围为___________(填标号)
的范围为___________(填标号)
 对氨法脱硫工艺的影响。
对氨法脱硫工艺的影响。步骤Ⅰ.模拟氨法脱硫
在通风橱中选择合适的装置模拟工业过程中利用氨水吸收
 (夹持装置省略)。
(夹持装置省略)。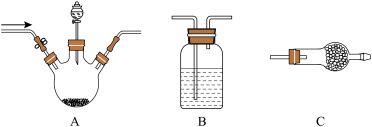
(2)装置B中使用多孔球泡的目的是
(3)装置C中盛放的药品是
(4)取2.00mL装置B中制得溶液[S(Ⅳ)含量以
 计]于盛有
计]于盛有 标准碘溶液的碘量瓶中,调节pH后以淀粉为指示剂,用
标准碘溶液的碘量瓶中,调节pH后以淀粉为指示剂,用 溶液进行滴定,平均消耗
溶液进行滴定,平均消耗 溶液的体积为8.00mL。
溶液的体积为8.00mL。①碘量瓶中
 和
和 反应的离子方程式为
反应的离子方程式为②步骤Ⅰ中制得溶液

③若直接使用标准碘溶液滴定
 ,则会导致测得
,则会导致测得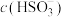
步骤Ⅱ.亚硫酸氢铵的氧化
取步骤Ⅰ制得溶液平均分成5份,分别添加
 (HCl酸化)使溶液中
(HCl酸化)使溶液中 达到指定浓度,持续通入空气,反应180min后,测得各组
达到指定浓度,持续通入空气,反应180min后,测得各组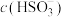 变化量及
变化量及 变化量如下表所示:
变化量如下表所示:| 组别 | 1 | 2 | 3 | 4 | 5 |
 | 0 |  | 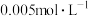 |  |  |
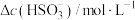 | 0.533 | 0.535 | 0.542 | 0.549 | 0.551 |
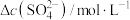 | 0.470 | 0.515 | 0.518 | 0.526 | 0.525 |
(6)
 过高时,
过高时, 的氧化率[
的氧化率[ ]降低的原因为
]降低的原因为(7)进一步设计实验确定最佳
 ,应调控
,应调控 的范围为___________(填标号)
的范围为___________(填标号)A.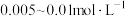 | B.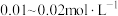 |
C.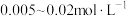 | D.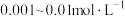 |
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】现用如下实验装置测定铜和氧化铜混合物中铜元素的含量。

试回答下列问题:
(1)A中盛装盐酸的仪器名称为___________________ 。
(2)A中可观察到的现象为__________________________________ 。
(3)B装置的作用是____________________________ 。
(4)在给D装置加热前,应该进行的一步操作是________ ,其目的是:________________ 。
(5)已知D装置中铜和氧化铜混合物的质量为10 g,经称量,反应前后E装置的质量分别为100.2 g和102.0 g,原混合物中铜元素的质量分数为________ (假设各装置中的反应或吸收都是完全的)。
(6)如不加F装置,会使实验结果_______ (填“偏低”或“偏高”)。

试回答下列问题:
(1)A中盛装盐酸的仪器名称为
(2)A中可观察到的现象为
(3)B装置的作用是
(4)在给D装置加热前,应该进行的一步操作是
(5)已知D装置中铜和氧化铜混合物的质量为10 g,经称量,反应前后E装置的质量分别为100.2 g和102.0 g,原混合物中铜元素的质量分数为
(6)如不加F装置,会使实验结果
您最近半年使用:0次
【推荐1】为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和 A中加热装置已略)。

实验过程:
①检查装置气密性后,在各仪器中添加相应试剂。
②打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
③打开活塞a,滴加一定量的浓盐酸,加热A。
④当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
⑤打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
⑥打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
⑦更换试管D,重复过程⑤,检验B溶液中的离子。
试回答下列问题:
(1)检验装置A气密性的具体操作是_______________________ 。
(2)C中发生反应的化学方程式为______________________________ 。
(3)B中的棉花通常会浸润____ 试剂;实验②中通入N2的作用是__________ 。
(4)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是________ (填“甲”、“乙”或“丙”)。
(5)进行实验过程⑥时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。
查阅资料:Fe2+(aq)+SO (aq)
(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)
提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:

① 溶液E和F分别为__________ 、__________ 。
② 请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因____________ 。

实验过程:
①检查装置气密性后,在各仪器中添加相应试剂。
②打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
③打开活塞a,滴加一定量的浓盐酸,加热A。
④当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
⑤打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
⑥打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
⑦更换试管D,重复过程⑤,检验B溶液中的离子。
试回答下列问题:
(1)检验装置A气密性的具体操作是
(2)C中发生反应的化学方程式为
(3)B中的棉花通常会浸润
(4)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程⑤ B溶液中含有的离子 | 过程⑦ B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO |
| 乙 | 既有Fe3+又有Fe2+ | 有SO |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+SO
 (aq)
(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:

① 溶液E和F分别为
② 请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某实验小组用下图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯):
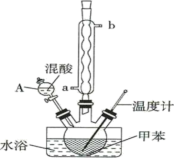
反应原理:
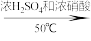
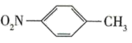 (对硝基甲苯)+
(对硝基甲苯)+  (邻硝基甲苯)
(邻硝基甲苯)
实验中可能用到的数据:
实验步骤:
①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40 mL。
②在三颈烧瓶中加入13 g甲苯(易挥发),按图所示装好药品和其他仪器。
③向三颈烧瓶中加入混酸。
④控制温度约为50℃,反应大约10 min,三颈烧瓶底有大量淡黄色油状液体出现。
⑤分离出一硝基甲苯,经提纯最终得到纯净的一硝基甲苯共15g。
请回答下列问题:
(1)冷凝管的作用是___________________ ;冷却水从冷凝管的__________ (填“a”或“b”)端进入。
(2)仪器A的名称是_______________ ,使用该仪器前必须进行的操作是__________________________ 。
(3)分离反应后产物的方案如下:

其中,操作1的名称为____________ ,操作2必需的玻璃仪器有酒精灯、温度计、锥形瓶牛角管(尾接管)和________________________ 、__________________________________________ 。
(4)本实验中甲苯的转化率为____________ (结果保留3位有效数字)。

反应原理:

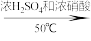
 (对硝基甲苯)+
(对硝基甲苯)+  (邻硝基甲苯)
(邻硝基甲苯)实验中可能用到的数据:
密度/ | 沸点/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 对硝苯甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40 mL。
②在三颈烧瓶中加入13 g甲苯(易挥发),按图所示装好药品和其他仪器。
③向三颈烧瓶中加入混酸。
④控制温度约为50℃,反应大约10 min,三颈烧瓶底有大量淡黄色油状液体出现。
⑤分离出一硝基甲苯,经提纯最终得到纯净的一硝基甲苯共15g。
请回答下列问题:
(1)冷凝管的作用是
(2)仪器A的名称是
(3)分离反应后产物的方案如下:

其中,操作1的名称为
(4)本实验中甲苯的转化率为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】磷化铝、磷化锌、磷化钙与水反应产生高毒的PH3气体(熔点为-132℃,还原性强、易自燃),可用于粮食熏蒸杀虫。卫生安全标准规定:当粮食中磷化物(以PH3计)的含量低于0.05mg·kg-1时算合格。可用以下方法测定粮食中残留的磷化物含量:
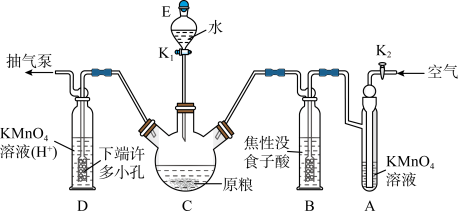
(操作流程)安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。
(实验装置)C中盛100g原粮,D中盛有20.00mL1.12×10-4mol•L-1KMnO4溶液(H2SO4酸化)。
请回答下列问题:
(1)仪器E的名称是___ ,该仪器可否用于分液操作___ ?(答“能”或“不能”)
(2)以磷化钙为例,写出磷化钙与水反应除了生成PH3之外,另一产物的电子式是___ ;检查整套装置气密性的方法是关闭___ 打开___ ,抽气泵缓慢抽气,若观察到___ (填字母)装置中有气泡产生则气密性良好。
(3)A中盛装KMnO4溶液的作用是___ ;通入空气的作用是___ 。焦性没食子酸可以吸收氧化性气体,若没有B装置,则实验中测得PH3含量将___ (填“偏低”、“偏高”或“不变”)
(4)D中PH3被氧化成磷酸,所发生反应的离子方程式为___ 。
(5)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5mol•L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为___ mg•kg-1。

(操作流程)安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。
(实验装置)C中盛100g原粮,D中盛有20.00mL1.12×10-4mol•L-1KMnO4溶液(H2SO4酸化)。
请回答下列问题:
(1)仪器E的名称是
(2)以磷化钙为例,写出磷化钙与水反应除了生成PH3之外,另一产物的电子式是
(3)A中盛装KMnO4溶液的作用是
(4)D中PH3被氧化成磷酸,所发生反应的离子方程式为
(5)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5mol•L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为
您最近半年使用:0次



