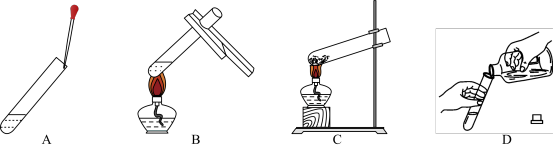
Ⅰ:利用如图装置可以验证元素性质的递变规律。
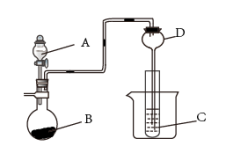
(1)仪器B的名称___________ ;干燥管D的作用除导气外还有___________ 。
(2)乙同学证明元素原子得电子能力Cl>C>Si,他在A中加入盐酸、B中加入大理石、C中加入硅酸钠溶液,观察到C中有白色胶状沉淀产生。
①丙同学认为乙不能证明得电子能力Cl>C,理由为___________ 。
②丁同学认为乙也不能证明得电子能力C>Si,原因是___________ 。
若想证明,丁认为应该在B与D之间增加一个装有___________ 溶液的装置。
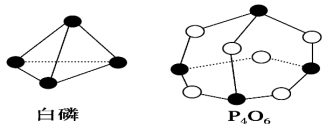
Ⅱ:已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P198,P-O360,O=O496。则1molP4(白磷)与O2反应生成1molP4O6(s)时___________ (填“吸收”或“放出”)___________ kJ热量。

(1)仪器B的名称
(2)乙同学证明元素原子得电子能力Cl>C>Si,他在A中加入盐酸、B中加入大理石、C中加入硅酸钠溶液,观察到C中有白色胶状沉淀产生。
①丙同学认为乙不能证明得电子能力Cl>C,理由为
②丁同学认为乙也不能证明得电子能力C>Si,原因是
若想证明,丁认为应该在B与D之间增加一个装有
Ⅱ:已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P198,P-O360,O=O496。则1molP4(白磷)与O2反应生成1molP4O6(s)时

更新时间:2021-06-06 15:45:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某一化学反应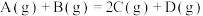
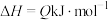 ,一定条件下反应过程中的能量变化如图所示。
,一定条件下反应过程中的能量变化如图所示。

请回答下列问题:
(1)Q_____ 0(填“>”“<”或“=”)。
(2)熵变
_____ 0(填“>”“<”或“=”)。
(3)该反应_____ 自发进行;若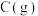 改为
改为 其他不变,该反应
其他不变,该反应_____ 自发进行。(填“能”、“不能”或“可能”)。
(4)反应物键能之和数值_____ 生成物键能之和(填“>”“<”或“=”)
(5)该反应_____ 氧化还原反应(填“是”“不是”或“可能是”)
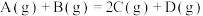
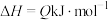 ,一定条件下反应过程中的能量变化如图所示。
,一定条件下反应过程中的能量变化如图所示。
请回答下列问题:
(1)Q
(2)熵变

(3)该反应
 改为
改为 其他不变,该反应
其他不变,该反应(4)反应物键能之和数值
(5)该反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】填空
(1)从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。已知该反应为放热反应,下图能正确表示该反应中能量变化的是___________ (填“A”或“B”)

(2)下图是甲烷燃料电池工作原理示意图,请回答下列问题:

①电池的负极是___________ (填“a”或“b”)电极,该极的电极反应式为:___________ 。
②电池工作一段时间后电解质溶液的pH___________ (填“增大”“减小”或“不变”)。
(1)从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。已知该反应为放热反应,下图能正确表示该反应中能量变化的是

(2)下图是甲烷燃料电池工作原理示意图,请回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】能源是现代文明的原动力,通过化学方法可使能量按人们所期望的形式转化,从而开辟新能源和提高能量转化率。请回答下列问题:
(1)能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。下列做法有助于能源“开源节流”的是_______ (填序号)。
(2)化学反应的本质是旧化学键的断裂,新化学键的形成。已知断开1 mol H−H键、1 mol N≡N键、1 mol N−H键分别需要吸收的能量为436 kJ、946 kJ、391 kJ。那么H2和N2反应生成NH3,该反应的热化学反应方程式为_______ 。化工生产中为了提高NH3产率可采取的措施有:_______ (写一点即可)。
(3)已知一定条件下,白磷转化为红磷释放能量,故红磷比白磷稳定性_______ (填“强”或“弱”)。
(4)化学电源在生产、生活中有着广泛的应用。根据构成原电池的本质判断,如下反应可以设计成原电池的是_______(填序号)。
(5)为了探究化学反应中的能量变化,某同学设计了如下两个实验。甲、乙两装置中硫酸浓度、锌片等完全相同。试比较大小关系(填“>”、“<”或“=”):
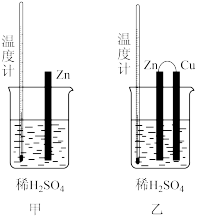
①产生气泡快慢:甲_______ 乙。
②温度计示数:甲_______ 乙。
(1)能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。下列做法有助于能源“开源节流”的是_______ (填序号)。
| A.大力开采煤、石油和天然气以满足人们日益增长的能源需求 |
| B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料 |
| D.减少资源消耗,增加资源的重复使用和循环再生 |
(3)已知一定条件下,白磷转化为红磷释放能量,故红磷比白磷稳定性
(4)化学电源在生产、生活中有着广泛的应用。根据构成原电池的本质判断,如下反应可以设计成原电池的是_______(填序号)。
| A.KOH + HCl=KCl + H2O | B.CH4 + 2O2 =CO2+2H2O |
| C.2H2O=2H2↑+O2↑ | D.Fe+CuSO4=FeSO4+Cu |

①产生气泡快慢:甲
②温度计示数:甲
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)鉴于 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(2)甲元素 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
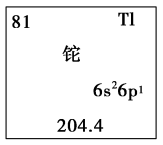
(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。
(1)鉴于
 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的(2)甲元素
 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。

| A.铊元素在元素周期表中的位置是第六周期第ⅡA族 |
B.铊原子的中子数为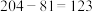 |
| C.铊原子有6个电子层,最外电子层上有3个电子 |
| D.铊元素的金属性比铝元素的强 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求完成下列填空:
(1)下列给定的物质中:①NaCl晶体;② ;③镁条;④氨气;⑤液态的HCl。属于非电解质的是
;③镁条;④氨气;⑤液态的HCl。属于非电解质的是___________ (填编号)。
(2)写出金属锂投入水中反应的化学方程式:___________ 。
(3)比较稳定性:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(1)下列给定的物质中:①NaCl晶体;②
 ;③镁条;④氨气;⑤液态的HCl。属于非电解质的是
;③镁条;④氨气;⑤液态的HCl。属于非电解质的是(2)写出金属锂投入水中反应的化学方程式:
(3)比较稳定性:

 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
(1)元素⑤在周期表中的位置描述为____________ ,元素⑧的元素符号__________________ 。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________ (填化学式)。
(3)元素②的单质的电子式______________ ,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________ (填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低 的顺序是___________________ (用化学式表示)。
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______ 。
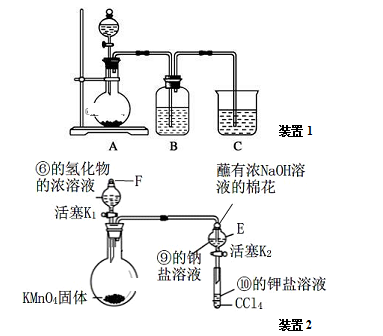
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______ (填“能”或“不能”)证明非金属性⑥>⑨>⑩。
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
| ⑩ | |||||||||||||||||
(1)元素⑤在周期表中的位置描述为
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是
(3)元素②的单质的电子式
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:

b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学是一门以实验为基础的学科,根据图回答问题。

(1)仪器a的名称是_______ 。
(2)实验室用高锰酸钾制氧气的化学方程式为_______ ,应选用的发生装置为_______ (填序号),若用C装置收集氧气,需待_______ 再开始收集,否则收集到的气体不纯。
(3)小明用大理石和稀盐酸制备并验证二氧化碳的性质,当看到G装置中出现_______ 的现象,说明二氧化碳能与水反应。
(4)小红认为小明的实验需控制好稀盐酸的浓度,防止制得的二氧化碳中混有HCl气体,因此提议先将制得的气体通过F装置以除去氯化氢气体,则气体应从_______ (填“m”或“n”)端通入,发生反应的化学方程式为_______ 。

(1)仪器a的名称是
(2)实验室用高锰酸钾制氧气的化学方程式为
(3)小明用大理石和稀盐酸制备并验证二氧化碳的性质,当看到G装置中出现
(4)小红认为小明的实验需控制好稀盐酸的浓度,防止制得的二氧化碳中混有HCl气体,因此提议先将制得的气体通过F装置以除去氯化氢气体,则气体应从
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硫酸镍(NiSO4)是电镀镍工业所用的主要镍盐,易溶于水。如图为某兴趣小组设计的在实验室中制备NiSO4·6H2O的装置,回答下列问题:

(1)实验室中配制浓H2SO4与浓HNO3混酸的操作为_________________
(2)图甲中仪器a的名称为_____ ,有同学认为将仪器a换作图乙中的仪器b效果更好,其理由为___________

(1)实验室中配制浓H2SO4与浓HNO3混酸的操作为
(2)图甲中仪器a的名称为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钠及其化合物在生产、生活中有着重要的用途。
(1)高压钠灯发光效率高、穿透力强、耗电少,寿命长。这种灯发出的光为_______ 色。
(2)如图所示实验装置用于验证Na2O2的某些性质,如证明过氧化钠可作供氧剂。

①A是实验室制取CO2的装置,写出A中发生反应的离子方程式:_______ 。
②填写表中空格:
③写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
④用_______ 检验F中收集到的气体,现象是_______ 。
(1)高压钠灯发光效率高、穿透力强、耗电少,寿命长。这种灯发出的光为
(2)如图所示实验装置用于验证Na2O2的某些性质,如证明过氧化钠可作供氧剂。

①A是实验室制取CO2的装置,写出A中发生反应的离子方程式:
②填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | 与CO2和水反应 | |
| D | NaOH溶液 |
③写出过氧化钠与二氧化碳反应的化学方程式:
④用
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是______ ,操作②的名称是_________ 。
(2)试剂a是________ (填化学式,下同),试剂b是_______ ,固体B是________ 。
(3)加入试剂a所发生反应的化学方程式为_______ 。加入试剂b所发生反应的离子方程式为______ 。
(4)该方案能否达到实验目的:_____ (填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)___ 。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____ 的质量。

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是
(2)试剂a是
(3)加入试剂a所发生反应的化学方程式为
(4)该方案能否达到实验目的:
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某小组以 和草酸
和草酸 的实验研究化学反应速率的影响因素,反应原理为:
的实验研究化学反应速率的影响因素,反应原理为:
Ⅰ.甲小组设计如下实验方案探究反应物浓度和溶液酸性对速率的影响:
【限选试剂和仪器】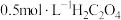 溶液、
溶液、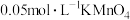 溶液(末酸化)、
溶液(末酸化)、 溶液、试管、胶头滴管、秒表
溶液、试管、胶头滴管、秒表
(1)表中
_______ ,
_______ 。
(2)为定量比较反应速率的快慢,本实验应测量_______ 。
(3)对比实验_______ 和_______ (填序号)可探究溶液酸性对反应速率的影响。
Ⅱ.乙小组利用色度传感器(检测溶液颜色的变化)探究草酸浓度对反应速率的影响,测得实验①③的溶液透光率-时间曲线如下所示。
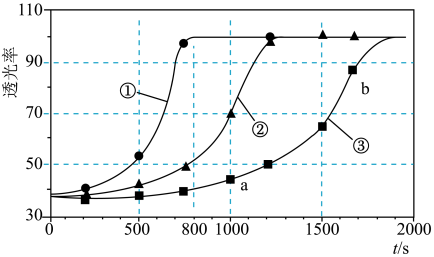
注:溶液透光率可表征溶液颜色的深浅。颜色越浅,透光率越大。
(4)实验①~③所用草酸的浓度由大到小的顺序为_______ (填序号)。
(5)a点和 点的速率大小关系:
点的速率大小关系:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(6)根据曲线,该小组推测 能作该反应的催化剂,并设计了如下实验:取与实验①浓度和体积均相同的反应物,再加入
能作该反应的催化剂,并设计了如下实验:取与实验①浓度和体积均相同的反应物,再加入_______ ,测量该条件下溶液透光率的变化情况,说明 能作该反应催化剂的判断依据是
能作该反应催化剂的判断依据是_______ 。
 和草酸
和草酸 的实验研究化学反应速率的影响因素,反应原理为:
的实验研究化学反应速率的影响因素,反应原理为:
Ⅰ.甲小组设计如下实验方案探究反应物浓度和溶液酸性对速率的影响:
【限选试剂和仪器】
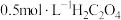 溶液、
溶液、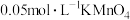 溶液(末酸化)、
溶液(末酸化)、 溶液、试管、胶头滴管、秒表
溶液、试管、胶头滴管、秒表| 序号 |  | 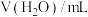 |  | 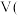 稀硫酸 稀硫酸 |
| Ⅰ | 2.0 | 1.0 | 1.0 | 1.0 |
| Ⅱ | 1.0 | 2.0 |  | 1.0 |
| Ⅲ | 2.0 |  | 1.0 | 2.0 |


(2)为定量比较反应速率的快慢,本实验应测量
(3)对比实验
Ⅱ.乙小组利用色度传感器(检测溶液颜色的变化)探究草酸浓度对反应速率的影响,测得实验①③的溶液透光率-时间曲线如下所示。

注:溶液透光率可表征溶液颜色的深浅。颜色越浅,透光率越大。
(4)实验①~③所用草酸的浓度由大到小的顺序为
(5)a点和
 点的速率大小关系:
点的速率大小关系:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(6)根据曲线,该小组推测
 能作该反应的催化剂,并设计了如下实验:取与实验①浓度和体积均相同的反应物,再加入
能作该反应的催化剂,并设计了如下实验:取与实验①浓度和体积均相同的反应物,再加入 能作该反应催化剂的判断依据是
能作该反应催化剂的判断依据是
您最近一年使用:0次